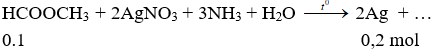Metyl fomat + AgNO3 | HCOOCH3 + 2AgNO3 + 3NH3 + H2O → 2Ag + 2NH4NO3 + NH4OCOOCH3 - Cân bằng phương trình hóa học
Có hàng nghìn phản ứng hóa học và để nhớ được các phương trình hóa học đó thật không dễ dàng. Bài học này giúp bạn cân bằng phản ứng hóa học HCOOCH3 + AgNO3 + NH3 + H2O một cách dễ dàng với đầy đủ điều kiện.
Metyl fomat + AgNO3 | HCOOCH3 + 2AgNO3 + 3NH3 + H2O → 2Ag + 2NH4NO3 + NH4OCOOCH3 - Cân bằng phương trình hóa học
-
Phản ứng hóa học:
HCOOCH3 + 2AgNO3 + 3NH3 + H2O
2Ag + 2NH4NO3 + NH4OCOOCH3
Điều kiện phản ứng
- Phản ứng xảy ra khi đun nóng.
Cách thực hiện phản ứng
- Cho HCOOCH3 vào dung dịch bạc nitrat trong amoniac, thấy có kết tủa (Ag) xuất hiện.
Hiện tượng nhận biết phản ứng
- Có kết tủa xuất hiện.
Bạn có biết
- Chỉ có este tạo bởi HCOOH mới có phản ứng với AgNO3/NH3 để tạo kết tủa Ag.
- Phản ứng này dung để phân biệt este tạo bởi HCOOH với các este khác.

-
Ví dụ minh họa
Ví dụ 1: Chất nào sao đây có thể tạo kết tủa với dung dịch AgNO3/NH3 ?
A. Metyl axetat.
B. Etyl axetat.
C. Metyl fomat.
D. But – 2 – in.
Hướng dẫn
Metyl fomat là este tạo bởi HCOOH nên có thể phản ứng với AgNO3/NH3 tạo kết tủa.
Đáp án C.
Ví dụ 2: Cho 0,1 mol metyl axetat phản ứng hoàn toàn với một lượng dư AgNO3/NH3. Sau phản ứng thu được bao nhiêu mol Ag?
A. 0,1.
B. 0,2.
C. 0,3.
D. 0,4.
Hướng dẫn
Đáp án B.
Ví dụ 3: HCOOCH3 có thể tham gia phản ứng với các chất nào sau đây?
A. Ag.
B. HCOOH.
C. AgNO3/NH3.
D. N2.
Hướng dẫn
metyl fomat là este tạo bởi HCOOH nên có thể phản ứng với AgNO3/NH3
Đáp án C.