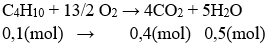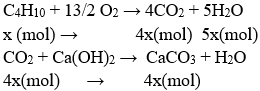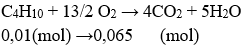2C4H10 + 13O2 → 8CO2 + 10H2O - Cân bằng phương trình hóa học
Có hàng nghìn phản ứng hóa học và để nhớ được các phương trình hóa học đó thật không dễ dàng. Bài học này giúp bạn cân bằng phản ứng hóa học C4H10 + O2 một cách dễ dàng với đầy đủ điều kiện.
2C4H10 + 13O2 → 8CO2 + 10H2O - Cân bằng phương trình hóa học
-
Phản ứng hóa học:
2C4H10 + 13O2
8CO2 + 10H2O
Điều kiện phản ứng
- Nhiệt độ
Cách thực hiện phản ứng
- Đốt cháy khí butan (C4H10) trong không khí thì thu được khí cacbonic và nước.
(Xét phản ứng xảy ra hoàn toàn và vừa đủ, không có chất dư)
Hiện tượng nhận biết phản ứng
- Trước khi đốt cháy khí butan (C4H10) trong không khí thì hỗn hợp phản ứng không màu. Sau khi đốt cháy thu được khí làm vẩn đục nước vôi trong.
Bạn có biết
- Phản ứng trên được gọi là phản ứng đốt cháy
- Tương tự butan (C4H10) các đồng đẳng của butan cũng tham gia phản ứng đốt cháy tương tự.
- Nếu thiếu oxi, phản ứng cháy của butan xảy ra không hoàn toàn: sản phẩm cháy ngoài CO2, H2O còn có C, CO...
- Khi đốt cháy butan, số mol H2O thu được sau phản ứng luôn lớn hơn số mol CO2.

-
Ví dụ minh họa
Ví dụ 1: Đốt cháy hoàn toàn 5,8 gam butan thu được bao nhiêu lít khí CO2 ở đktc? Bao nhiêu gam nước?
A. 8,96 lít và 9 gam
B. 8,96 lít và 18 gam
C. 4,48 lít và 5,4 gam
C. 2,24 lít và 7,2 gam
Hướng dẫn:
Số mol butan : nC4H10 = 5,8/58 = 0,1 (mol)
VCO2 = 0,4 . 22,4 = 8,96 (lít)
mH2O = 0,5 . 18 = 9 (gam)
Đáp án A.
Ví dụ 2: Đốt cháy hoàn toàn m gam butan. Dẫn toàn bộ sản phẩm vào dung dịch nước vôi trong dư thu được 10 gam kết tủa. Giá trị m = ?
A. 14,5 gam
B. 1,45 gam
C. 2,9 gam
D. 29 gam
Hướng dẫn:
Gọi số mol của butan phản ứng là x (mol)
mkết tủa = 4x . 100 = 10 (g) → x = 0,025 (mol)
→ mC4H10 = 0,025.58 = 1,45 (gam)
Đáp án B.
Ví dụ 3: Đốt cháy hoàn toàn 0,58 gam butan cần vừa đủ bao nhiêu thể tích khí oxi ở đktc?
A. 2,24 lít
B. 0,56 lít
C. 1,12 lít
D. 1,456 lít
Hướng dẫn:
Số mol butan : nC4H10 = 0,58/58 = 0,01 (mol)
VO2 = 0,065 .22,4 = 1,456 (lít)
Đáp án D.