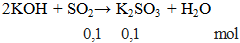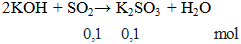2KOH + SO2 → K2SO3 + H2O - Cân bằng phương trình hóa học
Có hàng nghìn phản ứng hóa học và để nhớ được các phương trình hóa học đó thật không dễ dàng. Bài học này giúp bạn cân bằng phản ứng hóa học KOH + SO2 một cách dễ dàng với đầy đủ điều kiện.
2KOH + SO2 → K2SO3 + H2O - Cân bằng phương trình hóa học
Phản ứng hóa học:
2KOH + SO2 → K2SO3 + H2O
Điều kiện phản ứng
- Phản ứng xảy ra ngay điều kiện thường.
Cách thực hiện phản ứng
- Dẫn khí SO2 vào ống nghiệm chứa KOH và vài giọt chất chỉ thị.
Hiện tượng nhận biết phản ứng
- Quan sát sự chuyển màu của chỉ thị phù hợp trước và sau phản ứng.
Bạn có biết
- KOH phản ứng với SO2 tùy theo tỉ lệ về số mol mà sản phẩm thu được có thể là muối cabonat trung hòa hoặc muối axit hoặc hỗn hợp cả hai muối.
- KOH phản ứng với SO2 chỉ thu được muối K2SO3 khi T = 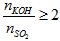

Ví dụ minh họa
Ví dụ 1:
Cho 2,24 lít khí SO2 ở đktc phản ứng với lượng dư dung dịch KOH thu được dung dịch X. Khối lượng muối tan có trong X là
A. 15,8 gam. B. 13,8 gam. C. 11,8 gam. D. 10,8 gam.
Hướng dẫn giải
Do KOH dư nên có phản ứng
mmuối = 0,1.158 = 15,8 gam.
Đáp án A.
Ví dụ 2:
Cho SO2 tác dụng với lượng dư dung dịch KOH thu được dung dịch X. Chất tan có trong dung dịch X là
A. K2SO3. B. K2SO3 và KHSO3. C. KHSO3. D. K2SO3 và KOH.
Hướng dẫn giải
Do KOH dư nên có phản ứng
2KOH + SO2 → K2SO3 + H2O
Chất tan có trong dung dịch X là K2SO3 và KOH dư.
Đáp án D.
Ví dụ 3:
Cho 2,24 lít khí SO2 ở đktc phản ứng với dung dịch chứa 0,3 mol KOH. Khối lượng muối tan có trong dung dịch sau phản ứng là
A. 15,8 gam. B. 13,8 gam. C. 11,8 gam. D. 10,8 gam.
Hướng dẫn giải
Có T = 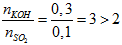
mmuối = 0,1.158 = 15,8 gam.
Đáp án A.