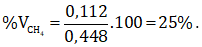C2H4 + Br2 | Etilen + Br2 | CH2=CH2 + Br2 → CH2Br–CH2Br - Cân bằng phương trình hóa học
Có hàng nghìn phản ứng hóa học và để nhớ được các phương trình hóa học đó thật không dễ dàng. Bài học này giúp bạn cân bằng phản ứng hóa học C2H4 + Br2 một cách dễ dàng với đầy đủ điều kiện.
C2H4 + Br2 | Etilen + Br2 | CH2=CH2 + Br2 → CH2Br–CH2Br - Cân bằng phương trình hóa học
-
Phản ứng hóa học:
CH2=CH2 + Br2 → CH2Br–CH2Br
Điều kiện phản ứng
- Phản ứng xảy ra ở điều kiện thường,
Cách thực hiện phản ứng
- Dẫn khí etilen từ từ qua dung dịch brom thấy màu nâu đỏ của dung dịch nhạt dần.
Hiện tượng nhận biết phản ứng
- Màu nâu đỏ của dung dịch nhạt dần.
Bạn có biết
- Phản ứng trên gọi là phản ứng cộng.
- Các đồng đẳng của etilen đều làm mất màu dung dịch brom.
- Phản ứng trên dung để phân biệt anken với ankan.

-
Ví dụ minh họa
Ví dụ 1: Dãy đồng đẳng nào sau đây tham gia phản ứng cộng với theo tỉ lệ 1:1?
A. Ankin.
B. Anken.
C. Ankan.
D. Ankađien.
Hướng dẫn
Trong phân tử anken chứa một liên kết pi, có thể tham gia phản ứng cộng với brom theo tỉ lệ 1:1.
Đáp án B.
Ví dụ 2: Để phân biệt etan và etilen có thể dùng
A. dung dịch Br2.
B. dung dịch AgNO3.
C. quỳ tím.
D. dung dịch NaOH.
Hướng dẫn
Để phân biệt etan và etilen có thể dùng dd Br2 (màu vàng nâu), do etilen có thể phản ứng cộng với dd Br2 (tạo sản phẩm không màu) còn etan thì không.
Đáp án A.
Ví dụ 3: Cho 0,448 lít hỗn hợp khí gồm metan và etilen đi qua dung dịch brom dư, thấy dung dịch nhạt màu và còn 0,112 lít khí thoát ra. Biết các thể tích khí đo ở đktc, thành phần % thể tích khí metan có trong hỗn hợp là
A. 25%.
B. 50%.
C. 60%.
D. 37,5%.
Hướng dẫn
Do dd brom dư, nên khí thoát ra là metan.
Đáp án A.