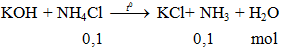KOH + NH4Cl -to→ KCl+ NH3 + H2O - Cân bằng phương trình hóa học
Có hàng nghìn phản ứng hóa học và để nhớ được các phương trình hóa học đó thật không dễ dàng. Bài học này giúp bạn cân bằng phản ứng hóa học KOH + NH4Cl một cách dễ dàng với đầy đủ điều kiện.
KOH + NH4Cl -to→ KCl+ NH3 + H2O - Cân bằng phương trình hóa học
Phản ứng hóa học:
KOH + NH4Cl -to→ KCl+ NH3 + H2O
Điều kiện phản ứng
- Phản ứng xảy ra khi đun nóng.
Cách thực hiện phản ứng
- Đun nóng muối NH4Cl với KOH.
Hiện tượng nhận biết phản ứng
- Có khí không màu, mùi khai bay ra.
Bạn có biết
- Các muối amoni khác như NH4NO3, (NH4)2SO4 … cũng phản ứng với KOH giải phóng amoniac.

Ví dụ minh họa
Ví dụ 1:
Hiện tượng xảy ra khi đun nóng muối NH4Cl với KOH là
A. Có khí màu nâu đỏ bay ra.
B. Có khí mùi trứng thối thoát ra.
C. Có khí màu vàng lục, mùi xốc thoát ra.
D. Có khí mùi khai thoát ra.
Hướng dẫn giải
KOH + NH4Cl 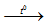
NH3 là khí có mùi khai.
Đáp án D.
Ví dụ 2:
Cho dung dịch KOH dư vào 100 ml NH4Cl 1 ml đun nóng nhẹ. Thể tích khí ở đktc thu được là
A. 1,12 lít. B. 2,24 lít. C. 3,36 lít. D. 4,48 lít
Hướng dẫn giải
V = 0,1.22,4 = 2,24 lít.
Đáp án B.
Ví dụ :3
Muối nào sau đây phản ứng với KOH không thu được amoniac?
A. NH4Cl. B. NH4NO3. C. (NH4)2SO4 . D. NaNO3.
Hướng dẫn giải
NaNO3 không phản ứng với KOH.
Đáp án D.