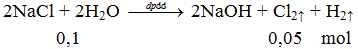Phản ứng điện phân dung dịch: 2NaCl + 2H2O -dpdd→ 2NaOH + Cl2↑ + H2↑ - Cân bằng phương trình hóa học
Có hàng nghìn phản ứng hóa học và để nhớ được các phương trình hóa học đó thật không dễ dàng. Bài học này giúp bạn cân bằng phản ứng điện phân dung dịch: 2NaCl một cách dễ dàng với đầy đủ điều kiện.
Phản ứng điện phân dung dịch: 2NaCl + 2H2O -dpdd→ 2NaOH + Cl2↑ + H2↑ - Cân bằng phương trình hóa học
Phản ứng hóa học:
2NaCl + 2H2O -dpdd→ 2NaOH + Cl2↑ + H2↑
Điều kiện phản ứng
- điện phân dung dịch
Cách thực hiện phản ứng
- điện phân dung dịch NaCl.
Hiện tượng nhận biết phản ứng
- Có khí vàng lục, mùi xốc thoát ra ở cực dương, khí không màu thoát ra ở cực âm.
Bạn có biết
- Nếu điện phân không có màng ngăn Cl2 thoát ra ở cực dương sẽ tác dụng với NaOH ở cực âm.

Ví dụ minh họa
Ví dụ 1:
Phương pháp nào sau đây dung để điều chế các kim loại hoạt động mạnh như K, Na?
A. điện phân nóng chảy muối clorua của chúng.
B. điện phân dung dịch muối clorua của chúng.
C. Cho Cu phản ứng với dung dịch muối clorua.
D. Nhiệt phân muối clorua.
Hướng dẫn giải
Phương pháp điện phân nóng chảy dung để điều chế các kim loại hoạt động mạnh như Na, K, Ca…
Đáp án A.
Ví dụ 2:
Thể tích khí ở dktc thoát ra ở cực dương khi điện phân dung dịch chứa 5,85 gam NaCl là
A. 1,12 lít. B. 2,24 lít. C. 3,36 lít. D. 4,48 lít.
Hướng dẫn giải
V = 0,05.22,4 = 1,12 lít.
Đáp án B.
Ví dụ 3:
Khi điện phân dung dịch NaCl, khí clo sinh ra ở
A. catot. B. cực âm. C. anot. D. màng ngăn.
Hướng dẫn giải
clo sinh ra ở cực dương hay anot
Đáp án C.