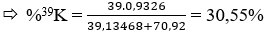2K + Br2 → 2KBr - Cân bằng phương trình hóa học
Có hàng nghìn phản ứng hóa học và để nhớ được các phương trình hóa học đó thật không dễ dàng. Bài học này giúp bạn cân bằng phản ứng hóa học K + Br một cách dễ dàng với đầy đủ điều kiện.
2K + Br2 → 2KBr - Cân bằng phương trình hóa học
Phản ứng hóa học:
2K + Br2 → 2KBr
Điều kiện phản ứng
- Nhiệt độ 150 - 250oC.
Cách thực hiện phản ứng
- Cho Kali tác dụng với dung dịch Br2 trong CCl4 thu được muối kalibrommua.
Hiện tượng nhận biết phản ứng
Kali phản ứng êm dịu với dung dịch nước brom.
Bạn có biết
Kali cũng cho phản ứng với halogen (Cl2; Br2,…) tạo thành muối.

Ví dụ minh họa
Ví dụ 1: Cho K tác dụng với dung dịch brom dư thu được 1,19 g muối. Khối lượng K tham gia phản ứng là
A. 0,39 g B. 3,9 g
C. 7,8 g D. 0,78 g
Đáp án A
Hướng dẫn giải:
Phương trình phản ứng: 2K + Br2 → 2KBr
NK = nKBr = 1,19/119 = 0,01 mol ⇒ mK = 0,01.39 = 0,39 g
Ví dụ 2: Cho Kali tác dụng với khí clo trong bình nhiệt độ cao. Phản ứng xảy ra với hiệu ứng nhiệt:
A. ΔH = 0 B. ΔH < 0
C. ΔH > 0 D. Không xác định
Đáp án B
Hướng dẫn giải:
Phản ứng đốt cháy K trong Cl2 tỏa nhiệt mạnh.
Ví dụ 3: Trong tự nhiên kali gồm ba đồng vị 39K chiếm 93,26% và đồng vị 40K chiếm 0,012% và đồng vị 41K. Brom là hỗn hợp hai đồng vị 79Br và 81Br với nguyên tử khối trung bình của brom là 79,92. Thành phần % khối lượng của 39K trong KBr là:
A. 30,56% B. 29,92%
C. 31,03% D. 30,55%
Đáp án D
Hướng dẫn giải:
%41K = 100% - (93,26% + 0,012%) = 6,728%
Khối lượng nguyên tử trung bình của K là MK = 39,13468