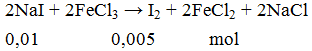2NaI + 2FeCl3 → I2 + 2FeCl2 + 2NaCl - Cân bằng phương trình hóa học
Có hàng nghìn phản ứng hóa học và để nhớ được các phương trình hóa học đó thật không dễ dàng. Bài học này giúp bạn cân bằng phản ứng hóa học NaI + FeCl3 một cách dễ dàng với đầy đủ điều kiện.
2NaI + 2FeCl3 → I2 + 2FeCl2 + 2NaCl - Cân bằng phương trình hóa học
Phản ứng hóa học:
2NaI + 2FeCl3 → I2 + 2FeCl2 + 2NaCl
Điều kiện phản ứng
- điều kiện thường.
Cách thực hiện phản ứng
- nhỏ FeCl3 vào ống nghiệm chứa NaI và vài giọt hồ tinh bột.
Hiện tượng nhận biết phản ứng
- sản phẩm sinh ra làm xanh hồ tinh bột.
Bạn có biết
- Các muối sắt (III) khác cungx phản ứng với NaI tương tự FeCl3.

Ví dụ minh họa
Ví dụ 1:
Chất nào sau không phản ứng với dung dịch NaI?
A. FeCl3. B. Cl2. C. O3. D. HI.
Hướng dẫn giải
HI không phản ứng.
Đáp án D.
Ví dụ 2:
Cho FeCl3 vào ống nghiệm đựng NaI có chứa sẵn hồ tinh bột. Hiện tượng quan sát được là
A. Dung dịch hiện màu vàng nâu.
B. Dung dịch hiện màu xanh.
C. Dung dịch có màu trắng.
D. Có kết tủa màu vàng nhạt.
Hướng dẫn giải
2NaI + 2FeCl3 → I2 + 2FeCl2 + 2NaCl
I2 sinh ra làm xanh hồ tinh bột.
Đáp án B.
Ví dụ 3:
Khối lượng Iot sinh ra khi cho FeCl3 phản ứng vừa đủ với 0,01 mol NaI là
A. 1,27g. B. 12,7g. C. 2,5g. D. 25,4g.
Hướng dẫn giải
m = 0,005.254 = 1,27g.
Đáp án A.