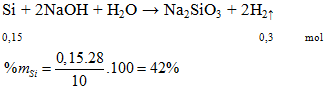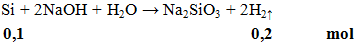Si + 2NaOH + H2O → Na2SiO3 + 2H2↑ - Cân bằng phương trình hóa học
Có hàng nghìn phản ứng hóa học và để nhớ được các phương trình hóa học đó thật không dễ dàng. Bài học này giúp bạn cân bằng phản ứng hóa học NaOH + Si một cách dễ dàng với đầy đủ điều kiện.
Si + 2NaOH + H2O → Na2SiO3 + 2H2↑ - Cân bằng phương trình hóa học
Phản ứng hóa học:
Si + 2NaOH + H2O → Na2SiO3 + 2H2↑
Điều kiện phản ứng
- điều kiện thường,
Cách thực hiện phản ứng
- cho silic tác dụng với dung dịch kiềm.
Hiện tượng nhận biết phản ứng
- Silic tan dần, có khí thoát ra.
Bạn có biết
- Silic tác dụng tương đối mạnh với dung dịch kiềm, giải phóng H2.

Ví dụ minh họa
Ví dụ 1:
Chất nào sau đây không tác dụng với NaOH?
A. Si. B. Al. C. ZnO. D. C.
Hướng dẫn giải
C không tác dụng với NaOH.
Đáp án D.
Ví dụ 2:
Cho hỗn hợp Si và than có khối lượng 10g tác dụng với lượng dư dung dịch NaOH đặc, đun nóng. Phản ứng giải phóng ra 6,72 lít khí H2 ở đktc. Biết rằng phản ứng xảy ra với H = 100%. Xác định thành phần % của Si trong hỗn hợp ban đầu.
A. 20%. B. 30%. C. 40%. D. 42%.
Hướng dẫn giải
C không phản ứng
Đáp án D.
Ví dụ 3:
Thể tích khí H2 ở đktc thoát ra khi cho 2,8g Si tác dụng hết với NaOH đặc, đun nóng là
A. 1,12 lít. B. 2,24 lít. C. 3,36 lít. D. 4,48 lít.
Hướng dẫn giải
V = 0,2.22,4 = 4,48 lít.
Đáp án D.