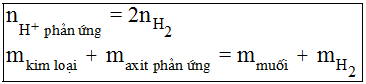Bài toán hỗn hợp kim loại tác dụng với axit hay, chi tiết
Bài toán hỗn hợp kim loại tác dụng với axit hay, chi tiết Hóa học lớp 12 với đầy đủ lý thuyết, phương pháp giải và bài tập có lời giải cho tiết sẽ giúp học sinh nắm được Bài toán hỗn hợp kim loại tác dụng với axit hay, chi tiết
Bài toán hỗn hợp kim loại tác dụng với axit hay, chi tiết
I. Phương pháp
1. Với các axit không có tính oxi hóa:
Phương trình tổng quát :
2M + 2nHCl → 2MCln + nH2
2M + nH2SO4 → M2(SO4)n + nH2
Điều kiện: Kim loại là kim loại đứng trước H trong dãy hoạt động hóa học.
K, Na, Ba, Ca, Mg, Al, Zn, Fe, Ni, Sn, Pb, H, Cu, Hg, Ag, Pt, Au
Đặc điểm:
- Muối thu được có hóa trị thấp (đối với kim loại có nhiều hóa trị)
- Sau phản ứng sinh ra khí H2
Ví dụ: Fe + 2HCl → FeCl2 + H2
Cu không phản ứng HCl
* Phương pháp chung
- Bảo toàn nguyên tố: nCl = nHCl = 2nH2 ; nSO4 = nH2SO4 = nH2
- Bảo toàn khối lượng: mkim loại + mHCl = mmuối + mH2 hoặc mmuối = mkim loại + mgốc axit
- Bảo toàn electron: ne kim loại cho = ne H nhận
- Khối lượng dung dịch tăng = khối lượng kim loại phản ứng – khối lượng khí H2
• Bài toán hỗn hợp kim loại tan hết trong 1 axit (HCl hoặc H2SO4) tạo khí H2
• Bài toán hỗn hợp kim loại tan hết trong hỗn hợp HCl và H2SO4 tạo khí H2
Nếu cho hỗn hợp kim loại kiềm, kiềm thổ tan hết trong hỗn hợp HCl và H2SO4
+) Kim loại tan trong axit trước, nếu axit hết kim loại mới tác dụng với nước
+) Khí H2 sinh ra có thể do kim loại tác dụng với axit và H2O
2. Với các axit có tính oxi hóa:
Kim loại + HNO3/H2SO4 đặc → muối + sản phẩm khử + H2O
- Kim loại tác dụng với HNO3 và H2SO4 đặc sinh ra muối có số oxi hóa cao nhất
- Hầu hết các kim loại đều tác dụng (trừ Au, Pt)
- Al, Fe, Cr bị thụ động hóa trong HNO3 đặc nguội và H2SO4 đặc nguội
a. Kim loại tác dụng với dung dịch HNO3
Sản phẩm khử :
+ NO2: khí màu nâu
+ NO: khí không màu, hóa nâu trong không khí
+ N2O: khí không màu, gây cười
+ N2: khí không màu
+ NH4NO3: muối tan trong dung dịch
Sản phẩm khử của N+5 tùy thuộc vào độ mạnh của kim loại và nồng độ của dung dịch axit. Thông thường thì dung dịch đặc tạo NO2, loãng tạo NO, kim loại có tính khử càng mạnh thì N bị khử xuống mức càng sâu.
Phương pháp giải:
nNO3 - tạo muối = ne cho
mmuối = mkim loại + mNO3 = mkim loại + 62. ne cho
- Bảo toàn nguyên tố H: nH+ = 2nH2 hay nH+ = 4nNH4+ +2nH2O
- Bảo toàn nguyên tố N: nHNO3 = nNO3 − trong muối + nN trong sản phẩm khử
nHNO3 phản ứng = 2nNO2 + 4nNO + 10nN2O + 12nN2 + 10nNH4NO3
- Nếu có hỗn hợp kim loại chứa Fe phản ứng với axit, sau phản ứng còn dư kim loại thì muối sắt thu được là muối Fe(II)
- Dung dịch chứa đồng thời ion H+ và NO3- có tính oxi hóa tương tự dung dịch axit HNO3
b. Kim loại tác dụng với dung dịch H2SO4
Sản phẩm khử :
+ SO2: khí mùi sốc (mùi hắc)
+ S: kết tủa vàng
+ H2S: khí mùi trứng thối
Phương pháp giải: sử dụng các định luật bảo toàn
Các công thức cần nhớ
2nSO42- = ne cho
mmuối = mkim loại + mSO4 = mkim loại + 96nSO2
- Bảo toàn nguyên tố S: nH2SO4 = nSO42- trong muối + nS trong sản phẩm khử

II. Ví dụ minh họa
Ví dụ 1: Hòa tan 14,8 gam hỗn hợp gồm Fe và Cu vào lượng dư dung dịch hỗn hợp HNO3 và H2SO4 đặc nóng. Sau phản ứng thu được 10,08 lít NO2 (đktc) và 2,24 lít SO2 (đktc). Khối lượng Fe trong hỗn hợp ban đầu là:
A. 5,6
B. 8,4
C. 18
D. 18,2
Ví dụ 2: Đun nóng m gam hỗn hợp Cu và Fe có tỉ lệ khối lượng tương ứng 7:3 với một lượng dung dịch HNO3. Khi các phản ứng kết thúc, thu được 0,75m gam chất rắn, dung dịch X và 5,6 lít hỗn hợp khí (đktc) gồm NO và NO2 (không có sản phẩm khử khác của N+5). Biết lượng HNO3 đã phản ứng là 44,1 gam. Giá trị của m là:
A. 448
B. 40,5
C. 33,6
D. 50,4
III. Bài tập vận dụng
Câu 1: Đốt cháy hoàn toàn 3,86g hỗn hợp gồm Fe, Al, Cu thu được 4,66g oxit. Cho toàn bộ lượng oxit này tác dụng với dung dịch axit H2SO4 20% (d = 1,14 g/ml). Vậy thể tích H2SO4 cần dùng tối thiểu là:
A. 21,1 ml
B. 21,5 ml
C. 23,4 ml
D. 19,6 ml
Câu 2: Hòa tan hỗn hợp gồm 0,1 mol Fe và a mol Cu vào dung dịch HNO3 loãng dư thu được 5,6 lít hỗn hợp NO và N2 (đktc) có tỷ khối hơi so với H2 là 14,5. Vậy a có giá trị là:
A. 0,6625
B. 0,6225
C. 0,0325
D. 0,165
Câu 3: Nung nóng 16,8 gam hỗn hợp Au, Ag, Cu, Fe, Zn với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X. Thể tích dung dịch HCl 2M vừa đủ để phản ứng với chất rắn X là:
A. 600ml
B. 200ml
C. 800ml
D. 400ml
Câu 4: Hòa tan hoàn toàn hỗn hợp gồm 0,01 mol Al; 0,05 mol Zn và 0,03 mol Fe cần vừa đủ 200ml dung dịch HCl 0,1M và H2SO4 a mol/l. Giá trị của a là?
A. 0,425
B. 0,5
C. 0,625
D. 0,75
Câu 5: Cho tan hoàn toàn 58 gam hỗn hợp gồm Fe, Cu, Ag trong dung dịch HNO3 2M thu được 0,15 mol NO; 0,05 mol N2O và dung dịch D. Cô cạn dung dịch D, khối lượng muối khan thu được là:
A. 120,4 gam
B. 89,8 gam
C. 116,9 gam
D. 110,7 gam
Câu 6: Khi cho 100 g hợp kim gồm có Fe, Cr và Al tác dụng với lượng dư dung dịch NaOH thu được 6,72 lít khí. Lấy bã rắn không tan cho tác dụng với một lượng dư dung dịch HCl (khi không có không khí) thu được 38,08 lít khí. Các thể tích đo ở đktc. Xác định thành phần % của hợp kim.
Câu 7: Cho 29 gam hỗn hợp Mg, Zn, Fe tác dụng hết với dung dịch H2SO4 loãng thấy thoát ra V lít khí (đktc). Cô cạn dung dịch sau phản ứng thu được 86,6 gam muối khan. Gía trị của V là:
A. 6,72 lít
B. 13,44 lít
C. 22,4 lít
D. 4,48 lít
Câu 8: Cho 13,33 gam hỗn hợp Al, Cu, Mg tác dụng với dung dịch H2SO4 loãng dư thu được dung dịch A, 7,728 lít khí (đktc) và 6,4 gam chất rắn không tan. Cô cạn dung dịch A thu được bao nhiêu gam muối khan?
A. 40,05 gam
B. 42,25 gam
C. 25,35 gam
D. 46,65 gam