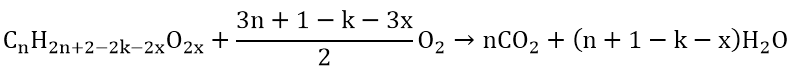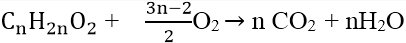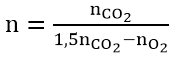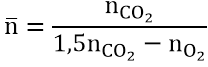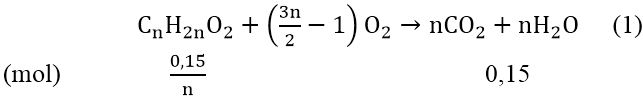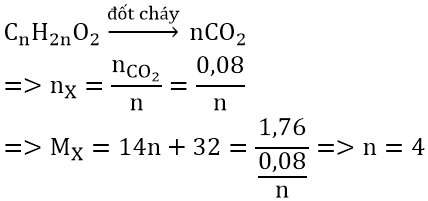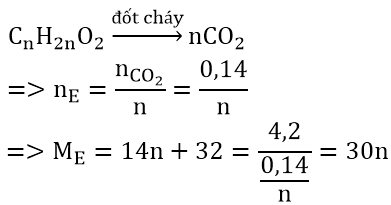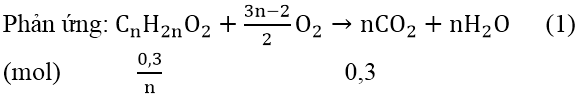Phương pháp giải Bài tập phản ứng đốt cháy este hay, chi tiết - Hoá 12
Phương pháp giải Bài tập phản ứng đốt cháy este hay, chi tiết Hóa học lớp 12 với đầy đủ lý thuyết, phương pháp giải và bài tập có lời giải cho tiết sẽ giúp học sinh nắm được Phương pháp giải Bài tập phản ứng đốt cháy este hay, chi tiết
Phương pháp giải Bài tập phản ứng đốt cháy este hay, chi tiết - Hoá 12
A. Phương pháp & Ví dụ
Lý thuyết và Phương pháp giải
CTTQ este: CnH2n+2-2k-2xO2x
PT tổng quát
TH este no, đơn chức
⇒ nH2O = nCO2 ; neste = 1,5nCO2 - nO2
⇒ Số nguyên tử C là
Trường hợp đốt cháy một hỗn hợp nhiều este thuộc cùng dãy đồng đẳng thì ta cũng kết luận tương tự như trên.
nhỗn hợp = 1,5nCO2 - nO2
ở đây : 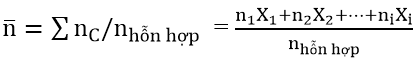
khác với axit cacboxylic giá trị n– trong este luôn lớn hơn 2.

Ví dụ minh họa
Bài 1: Đốt cháy hoàn toàn 3,7 gam một este đơn chức X thu được 3,36 lít khí CO2 (đktc) và 2,7 gam nước. Tìm công thức phân tử của X.
Hướng dẫn:
ta có: nCO2 = 3,36/22,4 = 0,15 (mol) và nH2O = 2,7/18 = 0,15 (mol)
Vì nCO2 = nH2O ⇒ este no,đơn chức
Gọi công thức este no, đơn chức là : CnH2nO2 (n ≥ 2)
Theo đề bài, ta có phương trình:
mX = (0,15/n).(14n + 32) = 3,7 ⇒ 2,1n + 4,8 = 3,7n ⇒ n = 3
Vậy công thức phân tử của X là : C3H6O2
Bài 2: Đốt cháy hoàn toàn 1,76 gam một este X thu được 3,52 gam CO2 và 1,44 gam H2O. Xác định công thức phân tử của X?
Hướng dẫn:
Ta có: nCO2 = 3,52/44 = 0,08 (mol); nH2O = 1,44/18 = 0,08(mol)
Do nCO2 = nH2O ⇒ X có độ bất bão hòa của phân tử ∆ = 1
X là este no, đơn chức ⇒ X dạng CnH2nO2
Vậy công thức phân tử của X là : C4H8O2
Bài 3: Đốt cháy hoàn toàn 4,2 gam một este E thu được 6,16 gam CO2 và 2,52 gam H2O. Xác định công thức phân tử , công thức cấu tạo , gọi tên E.
Hướng dẫn:
Ta có; nCO2 = 6,16/44 = 0,14(mol); nH2O = 2,52/18 = 0,14 (mol)
Do nCO2 = nH2O ⇒ ∆ = 1 ⇒ E là este no,đơn chức dạng: CnH2nO2
n = 2 ⇒ C2H4O2 ⇒ CTPT của E là HCOOCH3 (metyl fomiat)
Bài 4: Đốt cháy hoàn toàn một lượng hỗn hợp hai este, cho sản phẩm phản ứng cháy qua bình đựng P2O5 dư, khối lượng bình tăng thêm 6,21 gam, sau đó cho qua tiếp dung dịch Ca(OH)2 dư, thu được 34,5 gam kết tủa. Các este nói trên thuộc loại gì (đơn chức hay đa chức, no hay không no)?
Hướng dẫn:
Khối lượng tăng lên của bình P2O5 là khối lượng H2 O
P2O5 + 3H2O → 2H3PO4
Có kết tủa tạo thành là do CO2 hấp thụ
CO2 + Ca(OH)2 → CaCO3 + H2O
Ta có: nCaCO3 = 34,5/100 = 0,345 (mol)
nH2O = 6,21/18 = 0,345 (mol); nCO2 = nCaCO3 = 0,345 (mol)
Số mol H2O = số mol của CO2 ⇒ ∆ = 1
Do đó, hai este đều no, đơn chức
Bài 5: Đốt cháy hoàn toàn 7,4 gam este X đơn chức thu được 6,72 lít khí CO2 (đktc) và 5,4 gam nước. Xác định công thức phân tử của X.
Hướng dẫn:
Ta có : nCO2 = 6,72/22,4 = 0,3 (mol) và nH2O = 5,4/18 = 0,3 (mol)
Vì khi đốt cháy X thu được nH2O = nCO2 nên X là este no đơn chức
Gọi công thức của este no, đơn chức là : CnH2nO2 (n ≥ 2)
Theo đề bài, ta có: MX = (0,3/n).(14n + 32) = 7,4 ⇒ n = 3
Vậy công thức phân tử của X là : C3H6O2.
B. Trắc nghiệm
Câu 1. Đốt cháy hoàn toàn 1,1 gam hợp chất hữu cơ đơn chức X, thu được 2,2 gam CO2 và 0,9 gam H2O. X có khả năng tham gia phản ứng với NaOH. Số đồng phân của X là:
A. 3 B. 4 C. 5 D. 6
Đáp án hướng dẫn giải
Đáp án D
Ta có: = = 0,05 mol
mX = mO+ mC+ mH
⇒ nO = ![]() = 0,025 mol
= 0,025 mol
⇒ C: H: O = 0,05: 0,1: 0,025 = 2 : 4 : 1
X là hợp chất đơn chức tham gia phản ứng với NaOH
⇒ X có CTPT C4H8O2 là este hoặc axit
Các đồng phân:
HCOOC3H7; HCOOCH(CH3)CH3; CH3COOC2H5; C2H5COOCH3; C3H7COOH; CH3(CH3)CH2COOH.
Câu 2. Đốt cháy hoàn toàn 0,11 gam một este X (tạo nên từ một axit cacboxylic đơn chức và một ancol đơn chức) thu được 0,22 gam CO2 và 0,09 gam H2O. Số este đồng phân của X là:
A. 2 B. 5 C. 6 D. 4.
X tạo nên từ một axit cacboxylic đơn chức và một ancol đơn chức nên este X là este đơn chức mạch hở.
Mặt khác nCO2= nH2O= 0,005 mol
Đặt công thức este X là CnH2nO2 (n≥2), có số mol là a mol
CnH2nO2 + (3n-2)/2 O2 → nCO2+ nH2O
a → an mol
Ta có: mX= a.(14n + 32)= 0,11 gam ; nCO2 = an= 0,005 mol
Suy ra a= 0,00125 và n= 4.
Vậy công thức phân tử của este X là C4H8O2.
Các đồng phân của X là
HCOOCH2CH2CH3 ; HCOOCH(CH3)CH3 ; CH3COOCH2CH3 ; CH3CH2COOCH3.
Câu 3. Hỗn hợp X gồm vinyl axetat, metyl axetat và etyl fomat. Đốt cháy hoàn toàn 3,08 gam X, thu được 2,16 gam H2O. Phần trăm số mol của vinyl axetat trong X là:
A. 25% B. 27,92% C. 72,08% D. 75%.
Vinyl axetat (C4H6O2): CH3COOCH=CH2
Metyl axetat (C3H6O2): CH3COOCH3
Etyl fomat (C3H6O2): HCOOC2H5
Quy đổi hỗn hợp thành: C4H6O2 và C3H6O2
Ta có số mol của H2O: nH2O = 2,16/18 = 0,12 mol
Gọi x, y lần lượt là số mol của C4H6O2 và C3H6O2
Theo đề bài ta có hệ phương trình sau
Câu 4. Đốt cháy hoàn toàn 3,42 gam hỗn hợp gồm axit acrylic, vinyl axetat, metyl acrylat và axit oleic, rồi hấp thụ toàn bộ sản phẩm cháy vào dung dịch Ca(OH)2 (dư). Sau phản ứng thu được 18 gam kết tủa và dung dịch X. Khối lượng X so với khối lượng dung dịch Ca(OH)2 ban đầu đã thay đổi như thế nào?
A. Tăng 2,70 gam. B. Giảm 7,74 gam.
C. Tăng 7,92 gam. D. Giảm 7,38 gam.
Công thức chung của các chất trên là CnH2n-2O2
CnH2n – 2O2+ 1,5(n-1)O2 → nCO2 + (n-1)H2O
nCO2= nkết tủa = 0,18 mol
Gọi x là số mol của H2O => nO2 phản ứng = 3x/2
Bảo toàn khối lượng ta có: mhh+ mO2 = mCO2 + mH2O
=> 3,42 + 3x/2.32 = 44.0,18 + 18x => x = 0,15 mol
mCO2 + mH2O = 10,62 gam < m kết tủa
=> mdd giảm = 18 – 10,62 = 7,38 gam
Câu 5. Đốt cháy 6 gam este E thu được 4,48 lít CO2 (đktc) và 3,6 gam H2O. Biết E có phản ứng tráng gương với dung dịch AgNO3/NH3. Công thức cấu tạo của E là:
A. CH3COOCH2CH2CH3 B. HCOOCH2CH2CH3.
C. HCOOC2H5. D. HCOOCH3.
nCO2 = 0,2 mol; nH2O= 0,2 mol
=> nCO2 = nH2O=> Y là este no, đơn chức, mạch hở
Đặt CTTQ của Y là CnH2nO2
PT: CnH2nO2+ O2 → nCO2 + nH2O
14n+32 (g) n (mol)
6 (g) 0,2 (mol)
=> (14n +32).0,2 = 6n => n = 2
=> CTPT của Y: C2H4O2
=> CTCT của Y: HCOOCH3
Câu 6. Đốt cháy hoàn toàn 0,1 mol X chỉ chứa nhóm chức este ta thu được 4.48 lít CO2 (đktc) và 3,6 gam H2O. CTPT của este X có thể là:
A. C6H8O2 B. C4H8O4 C. C2H4O2 D. C3H6O2
Gọi CTPT Este:CnH2nO2 (n≥2)
nCO2 = 4,48/22,4 = 0,2 mol
Bảo toàn nguyên tố C: 0,2 = 0,1.n =>n = 2
=>Este: C2H4O2
C. Bài tập
Bài 1: Đốt cháy hoàn toàn một lượng hỗn hợp hai este X, Y, đơn chức, no, mạch hở cần 3,976 lít oxi (đktc) thu được 6,38 gam CO2. Cho lượng este này tác dụng vừa đủ với KOH thu được hỗn hợp hai ancol kế tiếp và 3,92 gam muối của một axit hữu cơ. Công thức cấu tạo của X, Y lần lượt.
Đáp án hướng dẫn giải
Đặt công thức chung của X, Y là CnH2nO2
CnH2nO2+ (3n/2-1) O2 → nCO2+ nH2O
Đặt nX = a mol ; nO2= a(1,5n-1) = 0,1775 mol; nCO2 = an = 0,145 mol
→ a = 0,04 mol và n = 3,625
Do cho lượng este này tác dụng vừa đủ với KOH thu được hỗn hợp hai ancol kế tiếp và 3,92 gam muối của một axit hữu cơ → Hai este đồng đẳng kế tiếp nhau → X và Y là C3H6O2 và C4H8O2
Đặt công thức chung của 2 etse là RCOOR’
RCOOR’ + KOH → RCOOK + R’OH
0,04 0,04 mol
→ MRCOOK= 3,92/ 0,04 = 98 → MR = 15→ R là CH3
→ X và Y là CH3COOCH3 và CH3COOC2H5
Đáp án C
Bài 2: Khi đốt cháy hoàn toàn este no, đơn chức thì nCO2 = nH2O đã phản ứng. Tên gọi của este.
Đáp án hướng dẫn giải
Gọi Công thức phân tử của este no, đơn chức là CnH2nO2
CnH2nO2 + (3n - 2)/2O2 → nCO2 + nH2O
Theo đề bài ta có: (3n - 2)/2 = n => n = 2
=> Công thức phân tử của este no đơn chức là C2H4O2
=> Công thức cấu tạo là : HCOOCH3: metyl fomiat
=> Đáp án A
Bài 3: Đốt cháy hoàn toàn 7,4 gam hỗn hợp hai este đồng phân, thu được 6,72 lít CO2(đktc) và 5,4 gam H2O. Xác định Công thức phân tử của hai este.
Đáp án hướng dẫn giải chi tiết
nH2O = nCO2 = 0,3 mol
Meste = 74
Công thức phân tử ⇒ C3H6O2
Bài 4: Hỗn hợp X gồm 2 este của 1 ancol no, đơn chức và 2 axit no, đơn chức đồng đẳng kế tiếp. Đốt cháy hòan toàn 0,1 mol X cần 6,16 lít O2 (đktc). Đun nóng 0,1 mol X với 50 gam dd NaOH 20% đến Phản ứng hòan toàn, rồi cô cạn dd sau Phản ứng được m gam chất rắn. Giá trị của m là bao nhiêu.
Đáp án hướng dẫn giải
Do X là hỗn hợp 2 este mạch hở của cùng một ancol no, đơn chức và hai axit no, đơn chức đồng đẳng kế tiếp nên các este trong X đều là este no, đơn chức, mạch hở.
Gọi công thức chung của 2 este là CnH2nO2
*Xét phản ứng đốt cháy X: nO2 = 6,16 : 22,4 = 0,275 mol
CnH2nO2 + (3n-2)/2 O2 → nCO2 + nH2O
0,1 0,275
→0,1.(3n−2)/2 = 0,275 → n =2,5 => 2 este là HCOOCH3 (a mol) và CH3COOCH3 (b mol)
+ nX = a + b = 0,1
+ Số C trung bình: n = (2a + 3b)/0,1 = 2,5
Giải hệ thu được: a = b = 0,05
*Xét phản ứng của X với NaOH:
mNaOH = 50.20% = 10 gam => nNaOH = 0,25 mol
Do nNaOH > neste => NaOH dư
Vậy chất rắn thu được gồm:
HCOONa: 0,05 mol
CH3COONa: 0,05 mol
NaOH dư: 0,25 - 0,1 = 0,15 mol
=> m chất rắn = 0,05.68 + 0,05.82 + 0,15.40 = 13,5 gam
Bài 5: Đốt cháy hoàn toàn m gam este đơn chức X cần 11,2 lít khí oxi (đktc) thu được 24,8 gam hỗn hợp CO2 và nước có tỉ khối so với H2 là 15,5. Công thức phân tử của X là:
Đáp án hướng dẫn giải chi tiết
Đặt nCO2= x mol; nH2O= y mol
Ta có: mhỗn hợp= 44x + 18y = 24,8 gam;
Mhh = 15,5.2 = 31
nhỗn hợp= x + y= 24,8/31= 0,8 mol
Giải hệ trên ta có x = 0,4 và y= 0,4
Do nCO2= nH2O nên este X là este no, đơn chức, mạch hở có công thức là CnH2nO2
CnH2nO2 + (3n - 2)/2O2 → nCO2+ nH2O
a → a.(3n-2)/2 an mol
Ta có nCO2 = an = 0,4 mol;
nO2 = a(3n-2)/2 = 0,5 mol
Suy ra a = 0,1, n = 4.
Vậy công thức phân tử của X là C4H8O2.
Bài 6: Đốt cháy hoàn toàn 9,12 gam este X (công thức CnH10O2), thu được H2O và 10,752 lít CO2 (đktc). Mặt khác, cho 9,12 gam X tác dụng với dung dịch KOH vừa đủ, sau phản ứng thu được ancol etylic và m gam muối. Giá trị của m là
Đáp án hướng dẫn giải
Ta có nCO2 = 10,752/22,4 = 0,48 mol
Bảo toàn C có nC(X) = nCO2
=> 9,12/(12n + 42).n = 0,48 => n = 6 ⟹ X là C6H10O2
Thủy phân X trong KOH thu được ancol C2H5OH
=> Công thức cấu tạo của X là C3H5COOC2H5
C3H5COOC2H5 + KOH → C3H5COOK + C2H5OH
0,08 mol → 0,08 mol
=> mmuối = 0,08.124 = 9,92 gam
Bài 7: Đốt cháy hoàn toàn m gam hỗn hợp các este no, đơn chức, mạch hở. Sản phẩm cháy được dẫn vào bình đựng dung dịch Ca(OH)2 dư, thấy khối lượng bình tăng 24,8 gam. Khối lượng kết tủa tạo ra tương ứng là bao nhiêu?
Đáp án hướng dẫn giải
Este no, đơn chức, mạch hở có công thức phân tử là CnH2nO2 khi đốt cháy hoàn toàn cho:
Phương trình phản ứng
CnH2nO2 + (1,5n - 1)O2 → nCO2 + nH2O
Vậy nCO2 = nH2O = a gam
m↑ = mCO2+ mH2O
<=>12,4 = 44.a + 18.a
=> a = 0,2 mol
nCaCO3 = nCO2= 0,2
=>mCaCO3 = 20 gam