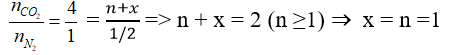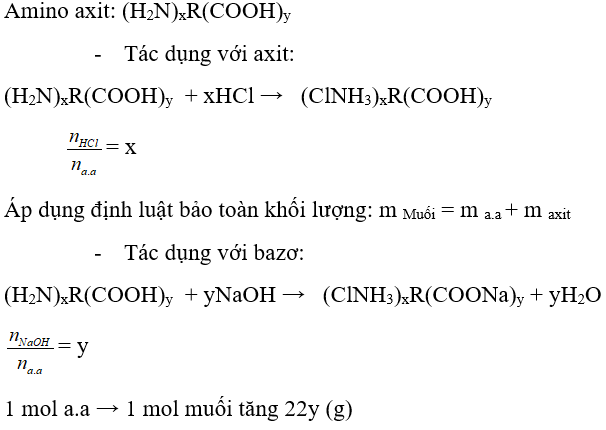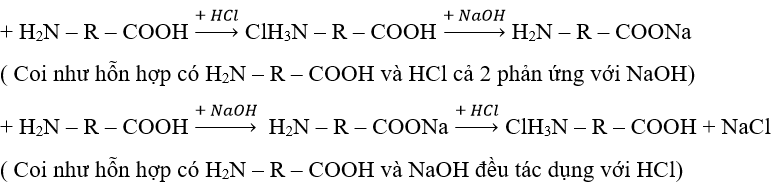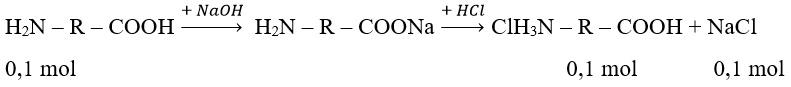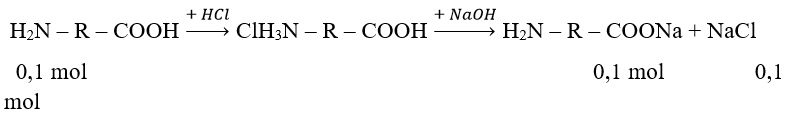4 dạng bài tập về Amino axit trong đề thi Đại học có giải chi tiết - Hoá 12
4 dạng bài tập về Amino axit trong đề thi Đại học có giải chi tiếtHóa học lớp 12 với đầy đ ủ lý thuyết, phương pháp giải và bài tập có lời giải cho tiết sẽ giúp học sinh nắm được 4 dạng bài tập về Amino axit trong đề thi Đại học có giải chi tiết
4 dạng bài tập về Amino axit trong đề thi Đại học có giải chi tiết - Hoá 12
Công thức chung của amino axit: (H2N)x – R – (COOH)y
- Lưỡng tính: Vừa mang tính axit; vừa mang tính bazơ
Dạng 1: Bài tập đốt cháy amino axit
Phương pháp :
CxHyOzNt + (x + y/4 - z/2) O2 → xCO2 + y/2H2O + 1/2N2
Hoặc có thể viết: (H2N)a – CxHy – (COOH)b
Chú ý :
CTTQ amino axit đơn chức có 1 nhóm -NH2; 1 nhóm –COOH: CnH2n+1O2N
Ví dụ 1: Đốt cháy hoàn toàn 8,7 g amino axit A (chứa 1 nhóm -COOH) thì thu được 0,3 mol CO2; 0,25mol H2O và 11,2 lít N2 (đktc). Công thức cấu tạo của A là:
A. CH3- CH2 (NH2)-COOH
B. CH3- CH2 (NH2)-COOH
C. CH3 – CH2 – CH2(NH2) - COOH
D. Cả A và B
Hướng dẫn giải :
CTPT: CxHyO2Nt , nN2 = 0,05 mol
mO (A) = mA – mC – mH – mN = 8,7 – 0,3.12 – 0,25.2 – 0,05.2.14 = 3,2
⇒ nO(A) = 0,2
A chỉ chứa 1 nhóm -COOH
⇒ nA = nO : 2 = 0,1 mol
nCO2 = x.nA = 0,1x = 0,3 ⇒ x =3
nH2O = (y/2).nA= 0,05y = 0,25 ⇒ y = 5
nN2 = (t/2).nA = 0,05t = 0,05 ⇒ t = 1
⇒ CTPT C3H5O2N
CTCT A: CH3- CH2(NH2)-COOH ; H2N- CH2 – CH2 - COOH
→ Đáp án D
Ví dụ 2 : Amino axit X chứa một nhóm amin bậc I trong phân tử. Đốt cháy hoàn toàn một lượng X thu được VCO2 : VN2 = 4:1. Công thức cấu tạo của X là:
A. HOOC – CH2CH(NH2)COOH
C. H2NCH2COOH
B. H2NCH2CH2COOH
D. H2NCH2CH2CH2COOH
Hướng dẫn giải :
Công thức của aminoaxit X có dạng: H2N – CxHy(COOH)n
Phản ứng: H2N – CxHy(COOH)n → (n + x)CO2 + 1/2 N2
Ta có :
Vậy X là: H2N – CH2COOH
→ Đáp án C

Dạng 2: Dẫn xuất amino axit
Phương pháp :
Đối với công thức CxHyOzNt có các dạng:
- Amino axit NH2 – R – COOH
- Este của amino axit NH2RCOOR’
- Muối amoni của NH3 hoặc amin (bậc I): RCOONH4 ( RCOOH + NH3 ) hoặc RCOONH3R’ (RCOOH + R’NH2 )
- Hợp chất nitro R-NO2
Ví dụ 1 : Ứng với C3H7NO2 có bao nhiêu đồng phân?
A. 2 B. 3 C. 5 D.6
Hướng dẫn giải :
+ Amino axit: H2N – CH2 – CH2 – COOH; CH3 – CH(NH2) – COOH
+ Este của amino axit: H2N – CH2 – COOCH3
+ Muối: CH2 = CH – COONH4; HCOONH3CH=CH2
+ Hợp chất nitro: CH3 – CH2 – CH2 – NO2
→ Đáp án D
Ví dụ 2 : Hợp chất X mạch hở có công thức phân tử C4H9NO2. Cho 10,3 gam X phản ứng vừa đủ với dung dịch NaOH sinh ra khí Y và dung dịch Z. Khí Y nặng hơn không khí và làm giấy quì tím ẩm chuyển thành màu xanh. Dung dịch Z có khả năng làm mất màu nước Brom. Cô cạn Z thu m gam muối khan. Giá trị m là?
A. 10,8 B. 9,4 C. 8,2 D. 9,6
Hướng dẫn giải :
X tác dụng NaOH tạo khí Y nên X : R1COOH3NR2
Dung dịch Z làm mất màu nước Brom nên R1 có liên kết đôi C=C, suy ra R1 ≥ 27 (1)
Khí Y làm giấy quỳ tím ẩm hóa xanh nên Y : R2NH2 và MY > 29 =>R2 + 16 > 29
⇒ R2 >13 (2)
Ta có : MX = R1 + R2 + 67 = 103 suy ra R1 + R2 = 42 (3)
Từ (1), (2), (3) R1= 27 : CH2=CH- và R2 = 15 : CH3-
CH2=CH-COOH3NCH3 + NaOH → CH2=CH-COONa + CH3NH2 + H2O
0,1mol → 0,1 mol
Giá trị m = 0,1.94 = 9,4 gam
→ Đáp án B
Dạng 3: Amino axit tác dụng với axit hoặc bazơ
Phương pháp :
Ví dụ 1 : X là một amino axit. Khi cho 0,01 mol X tác dụng với HCl thì dùng hết 80ml dung dịch HCl 0,125M và thu được 1,835g muối khan. Còn khi cho 0,01mol X tác dụng với dung dịch NaOH thì cần dùng 25g dung dịch NaOH 3,2%. Công thức cấu tạo của X là:
A. H2N – C3H6 – COOH
B. H2N – C2H4 – COOH
C. H2N – C3H5(COOH)2
D.(H2N)2C3H5 – COOH
Hướng dẫn giải :
nHCl = 0,01 = na.a⇒ X có 1 nhóm –NH2
nNaOH = 0,02 mol = 2nX ⇒X có 2 nhóm –COOH
X có dạng: H2N – R – (COOH)2
nmuối = nHCl = 0,01 ⇒ H2N – R – (COONa)2 = 1,835 : 0,01 ⇒R =41(-C3H5)
→ Đáp án D
Ví dụ 2 : Cho 10,3 gam aminoaxit X tác dụng với HCl dư thu được 13,95 gam muối. Mặt khác, cho 10,3 gam amino axit X tác dụng với NaOH (vừa đủ) thu được 12,5 gam muối. Vậy công thức của aminoaxit là:
A. H2N-C3H6-COOH
B. H2N-(CH2)4CH(NH2)-COOH
C. H2N-C2H4-COOH
D. HOOC-(CH2)2-CH(NH2)-COOH
Hướng dẫn giải :
X + HCl:
Áp dụng định luật bảo toàn khối lượng: mHCl = mmuối – mX = 3,65
nHCl = n -NH2 =0,1 mol
X + NaOH:
nNaOH = n–COOH = (mmuối – ma.a)/22 = 0,1
n–NH2 = n –COOH ⇒ Dựa vào đáp án amino axit đơn chức chỉ chứa 1 nhóm – COOH và 1 nhóm – NH2
⇒ na.a = nHCl = 0,1 ⇒ MX = 10,3 : 0,1 = 103 ⇒ X là: H2N – C3H6 –COOH
→ Đáp án A
Dạng 4: Amino axit tác dụng với axit sau đó lẫy hỗn hợp tác dụng với bazơ và ngược lại
Phương pháp :
Ví dụ 1: Cho 0,1 mol amino axit X tác dụng vừa đủ với 100ml NaOH 1M thu được chất hữu cơ Y. Cho Y tác dụng với dung dịch HCl thu được 18,4g muối. Vậy công thức của amino axit X là:
A. H2N – CH2 – CH2 – COOH
B. CH3 – CH(NH2) – COOH
C. H2N – CH2 – COOH
D. HOOC – CH2 – CH2 – CH(NH2) – COOH
Hướng dẫn giải :
nNaOH = na.a ⇒ X chỉ chứa 1 nhóm –COOH ( kết hợp với đáp án X chỉ có 1 –NH2)
Muối gồm: ClH3N – R – COOH (0,1 mol); NaCl (0,1 mol)
⇒ m(ClH3N – R – COOH) = 18,4 – 0,1.58,5 = 12,55
⇒ M (ClH3N – R – COOH) = 12,55 : 0,1 = 125,5
⇒ R = 28 ( - CH2 – CH2 - )
⇒ X là: H2N – CH2 – CH2 – COOH
→ Đáp án A
Ví dụ 2 : Cho amino axit X tác dụng vừa đủ với 16,6 ml dung dịch HCl 20% (d = 1,1 g/ml) thu được muối Y. Y tác dụng vừa đủ với 400 ml dung dịch NaOH 0,5M thu được dung dịch Z. Cô cạn cẩn thận dung dịch Z thu được 15,55 gam muối khan. Công thức của X là :
A. H2N-C2H4-COOH
B. H2N-CH2-COOH
C. H2N-C3H6-COOH
D. H2N-C3H4-COOH
Hướng dẫn giải :
nHCl = 0,1 mol; nNaOH = 0,2 mol
⇒ na.a = 0,2 – 0,1 = 0,1
m (H2N – R – COONa) = 15,55 – 0,1.58,5 = 9,7
M (H2N – R – COONa) = 9,7 : 0,1 = 97
R = 14 (-CH2-)
→ Đáp án A