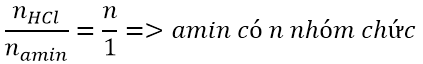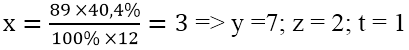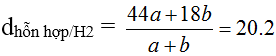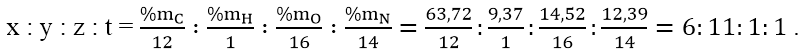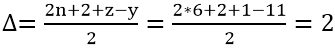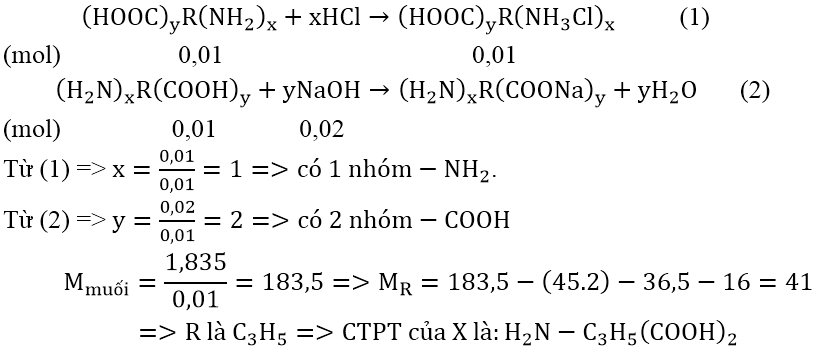Cách xác định công thức của Amin, Amino Axit hay, chi tiết - Hoá 12
Cách xác định công thức của Amin, Amino Axit hay, chi tiết Hóa học lớp 12 với đầy đủ lý thuyết, phương pháp giải và bài tập có lời giải cho tiết sẽ giúp học sinh nắm được Cách xác định công thức của Amin, Amino Axit hay, chi tiết
Cách xác định công thức của Amin, Amino Axit hay, chi tiết - Hoá 12
A. Phương pháp & Ví dụ
Lý thuyết và Phương pháp giải
Amin có tính bazo, tác dụng được với axit tạo muối.
Tùy theo số nhóm chức amin mà tác dụng với axit theo tỉ lệ xác định.
Ví dụ:
+) Amin bậc 1, đơn chức: RNH2 + HCl → RNH3Cl
+) Amin bậc 1, đa chức: R(NH2)n + nHCl → R(NH3Cl)n
Như vậy nếu biết số nhóm chức amin,ta suy ra tỉ lệ mol giữa axit với amin. Ngược lại từ tỉ lệ mol giữa axit và amin.
- Tương tự ở aminoaxit, sự có mặt nhóm amino làm cho nó tác dụng được với axit.

Ví dụ minh họa
Bài 1: Thủy phân polipeptit A người ta thu được:
Amino axit X có 40,4%C; 7,9%H; 15,7 %N và MX = 89
Amino axit Y có 54,9%C; 10 %H; 10,7 %N và MY = 131
Amino axit Z có 46,4%C; 5,8 %H; 27 %N và MZ = 155
Xác định công thức phân tử của X, Y, Z
Hướng dẫn:
Công thức phân tử của X là CxHyOzNt.
Ta có:
Công thức phân tử của X là C3H7O2N, là α-amoni axit nên có công thức cấu tạo: CH3-CH(NH2)-COOH.
Tương tự đối với Y: C6H13O2N
Công thức cấu tạo CH3-CH2-CH2-CH2-CH(NH2)-COOH
Đối với Z: C6H9N3O2 ⇒ CTCT: H2N-C4H3-CH(NH2)-COOH
Bài 2: Đốt cháy hoàn toàn 1,52 gam chất X cần 0,56 lit oxi (đkc), thu được hh khí gồm CO2, N2 và hơi nước. Sau khi ngưng tụ hơi nước hỗn hợp khí còn lại có khối lượng là 1,6 gam và có tỷ khối hơi đối với hiđro là 20. CTĐGN của X là
A. C2H6O5N2.
B. C3H8O5N2.
C. C3H10O3N2.
D. C4H10O5N2.
Hướng dẫn:
Sau khi ngưng tụ hơi nước hỗn hợp khí còn lại là CO2 (a mol) và N2 (b mol)
Ta có mhỗn hợp khí = mCO2 + mN2 = 44a + 28b = 1,6
a = 0,03 mol; b = 0,01 mol.
- Đặt X là CxHyOzNt
nC = nCO2 = 0,03 mol.
nN = 2 × nN2 = 2 × 0,01 = 0,02 mol.
mH2O = mX + mO2 - mCO2 - mH2O = 1,52 + 0,025 × 32 - 0,03 × 44 - 0,01 × 28 = 0,72 gam.
nH = 2 × nH2O = 2 × 0,72/18 = 0,08 mol.
nH2O = nO trong CO2 + nO trong H2O = 0,03 × 2 + 0,04 - 0,025 × 2 = 0,05 mol.
Ta có x : y : z : t = nC : n :H nO : nN = 0,03 : 0,08 : 0,05 : 0,02 = 3 : 8 : 5 : 2
Vậy CTĐGN là C3H8O5N2
Đáp án B
Bài 3: Hợp chất hữu cơ X có thành phần theo khối lượng: C chiếm 63,72%; H chiếm 9,37%; O chiếm 14,52%; còn lại là nito. Xác định công thức phân tử của X biết khối lượng mol của X bé hơn 120. Viết công thức cấu tạo của X biết X mạch hở không phân nhánh, không làm mất màu dung dịch brom.
Hướng dẫn:
Ta có: %C = 63,72%; %H = 9,37%; %O = 14,52% ⇒ %N = 12,39%
Lập tỉ lệ :
Công thức đơn giản là C6H11ON, M < 120 ⇒ CTPT là C6H11ON.
Độ bất bão hòa của X là :
X mạch hở không làm mất màu dung dịch brom nên mạch hidrocacbon phải no, vậy 2 liên kết sẽ thuộc nhóm –C≡N.
Vậy có thể có các đồng phân là :
CH2(OH)-CH2-CH2-CH2-C≡N
CH3-CH(OH)-CH2-CH2-CH2-C≡N
CH3-CH2-CH(OH)-CH2-2-C≡N
CH3-CH2-CH2-CH(OH)-CH2-C≡N
CH3-CH2-CH2-CH2-CH(OH)-C≡N
Bài 4: X là một amino axit. Khi cho 0,01 mol X tác dụng với HCl thì dùng hết 80 ml dung dịch HCl 0,125M và thu được 1,835 gam muối khan. Còn khi cho 0,01 mol X tác dụng với dung dịch NaOH thì cần dùng 25 gam dung dịch NaOH 3,2%. Hãy đề xuất công thức cấu tạo của X.
Hướng dẫn:
Gọi công thức tổng quát của X là : (H2N)xR(COOH)y
B. Bài tập trắc nghiệm
Bài 1: Đốt cháy hoàn toàn m gam một amin mạch hở đơn chức, sau phản ứng thu được 5,376 lít CO2; 1,344 lít N2 và 7,56 gam H2O (các thể tích đo ở đktc). CTPT của amin là:
A. C3H7N
B. C2H5N
C. CH5N
D. C2H7N.
Bài 2: X là một α-amino axit no chỉ chứa một nhóm -NH2 và một nhóm -COOH, cho 14,5 gam X tác dụng với dung dịch HCl dư, ta thu được 18,15 gam muối X. xác định công thức phân tử của X.
A. NH2–C6H12–COOH.
B. NH2–C5H10–COOH.
C. NH2–C4H8–COOH.
D. NH2–C3H6–COOH.
Bài 3: X là hợp chất hữu cơ chứa C, H, N ; trong đó nitơ chiếm 15,054% về khối lượng. X tác dụng với HCl tạo ra muối có dạng RNH3Cl. Công thức của X là :
A. CH3–C6H4–NH2.
B. C6H5–NH2.
C. C6H5–CH2–NH2.
D. C2H5–C6H4–NH2.
Bài 4: Đốt cháy hoàn toàn một amin đơn chức thì thu được CO2 và nước theo tỉ lệ mol nCO2 : nH2O = 8 : 9 . CTPT của amin là
A. C4H8N.
B. C3H7N.
C. C3H6N.
D. C4H9N.
Bài 5: Đốt cháy hoàn toàn 17,4 gam một amino axit có 1 nhóm –COOH được 0,6 mol CO2, 0,5 mol H2O và 0,1 mol N2. Công thức phân tử của amino axit là:
A. C3H5O2N.
B. C3H7O2N.
C. C3H5O4N.
D. C3H6O4N2.
Bài 6: Đốt cháy hoàn toàn một amin, no, đơn chức, mạch hở. Sản phẩm cháy sau khi ngưng tụ hơi nước có tỉ khối so với H2 là 19,333. Công thức phân tử của amin là:
A. CH3NH2
B. C2H5NH2
C. C3H7NH2
D. C4H9NH2
Bài 7: Đốt cháy hoàn toàn 2 amin no đơn chức mạch hở đồng đẳng liên tiếp thu được CO2 và H2O theo tỉ lệ số mol là 1 : 2. Hãy xác định công thức phân tử của hai amin ?
A. CH5N và C2H7N.
B. C2H7N và C3H9N.
C. C3H9N và C4H11N.
D. C4H11N và C5H13N.
C. Bài tập ví dụ minh họa
Ví dụ 1. Khi đốt cháy hoàn toàn một amin đơn chức X, thu được 8,4 lít khí CO2, 1,4 lít khí N2 (các thể tích khí đo ở đktc) và 10,125 gam H2O. Công thức phân tử của X là (cho H = 1, O = 16)
Đáp án hướng dẫn giải chi tiết
Gọi công thức phân tử của amin đơn chức là CxHyN
Ta có phương trình tổng quát:
C_xH_yN_t+(x+\frac y4)O_2\rightarrow xCO_2+\frac y2H_2O+\frac t2N_2
nCO2 = 8,4/22,4 = 0,375 mol
nH2O= 10,125/18 = 0,5625 mol
nN2 = 1,4/22,4 = 0,0625 mol
namin = 2nN2 = 0,125 mol
x = nCO2/namin= 0,375/0,125 = 3; y = 2nH2O/namin = 2.0,5625/0,125 = 9
Vậy công thức hóa học của amin là: C3H9N
Ví dụ 2: Đốt cháy hoàn toàn m gam một amin đơn chức X bằng lượng không khí vừa đủ thu được 1,76 gam CO2; 1,26 gam H2O và N2 (đktc). Tìm CTPT của X.
Đáp án hướng dẫn giải chi tiết
Đặt Công thức tổng quát của amin đơn chức là CxHyN
Ta có n_{CO_2} = 0,04(mol); n_{H_2O} = 0,07(mol)
⇒ x : y = nH: nC = 7 : 2⇒ X là C2H7N
Vậy Công thức cấu tạo của X là C2 H5 NH2
Ví dụ 3: Đốt cháy hoàn toàn 5,4 gam một amin X đơn chức, bậc 1 trong lượng vừa đủ không khí (O2 chiếm 20% thể tích, còn lại là N2). Dẫn sản phẩm khí qua bình đựng nước vôi trong dư thu được 24 gam kết tủa và có 41,664 lít (đktc) một chất khí duy nhất thoát ra. X là:
Đáp án hướng dẫn giải chi tiết
2C_nH_{2n+3}N\hspace{0.278em}\hspace{0.278em}\hspace{0.278em}+\hspace{0.278em}\frac{6n+3\hspace{0.278em}}2O_2\hspace{0.278em}\rightarrow\hspace{0.278em}2nCO_2\hspace{0.278em}+\hspace{0.278em}(2n+3)H_2O+\hspace{0.278em}N_2
Ca(OH)2 dư nên n_{CO_2} = n_{CaCO_3} = 0,24 ⇒ nC = 0,24
Trong X đặt nH = a và nN = b ⇒ n_{H_2O} = 0,5a và n_{N_2}sản phẩm = 0,5b mol
mX = a + 14b + 0,24.12 = 5,4 (1)
nN2 tổng = 1,86 ⇒ nN2 không khí = 1,86 – 0,5b
nN2 tổng = 1,86 ⇒ nN2 không khí = 1,86 – 0,5b
=> nO2 = nN2/4 = 0,465 - 0,125b
Bảo toàn O: 2nO2 = 2nCO2+ nH2O
⇒2. (0,465 – 0,125b) = 0,24.2 + 0,5a (2)
(1) và (2) ⇒ a = 0,84 và b = 0,12
⇒ nc : nH : nN = 0,24 : 0,84 : 0,12 = 2 : 7 : 1
X đơn chức nên X là C2H7 N