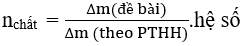Bài toán sắt tác dụng với dung dịch muối hay, chi tiết
Bài toán sắt tác dụng với dung dịch muối hay, chi tiết Hóa học lớp 12 với đầy đủ lý thuyết, phương pháp giải và bài tập có lời giải cho tiết sẽ giúp học sinh nắm được Bài toán sắt tác dụng với dung dịch muối hay, chi tiết
Bài toán sắt tác dụng với dung dịch muối hay, chi tiết
1. Phương pháp
- Vận dụng ý nghĩa của dãy điện thế cực chuẩn: Cr, Fe, Cu có thể đẩy kim loại yếu hơn ra khỏi muối như Ag, Hg…
Fe + Cu2+ → Fe2+ + Cu
Fedư + 2Ag+ → Fe2+ + 2Ag
Fe + 3Ag+dư → Fe3+ + 3Ag
- Với dạng bài tập: từ kim loại mạnh, tạo thành kim loại yếu hơn, có sự thay đổi về khối lượng nên vận dụng phương pháp tăng giảm khối lượng.
* Phương pháp tăng giảm khối lượng: Từ độ tăng( giảm) theo đề và tăng (giảm) theo PTHH ta tìm được số mol của các chất
Nếu gặp trường hợp một kim loại tác dụng với hỗn hợp muối ( hoặc ngược lại ) thì phản ứng nào có khoảng cách giữa 2 kim loại xa hơn thì sẽ xảy ra trước. Khi phản ứng này kết thúc thì mới xảy ra các phản ứng khác.
Ví dụ: Cho hỗn hợp Fe và Cu vào dung dịch AgNO3 thì Fe phản ứng trước, Cu phản ứng sau (vì nếu còn Fe thì không thể tồn tại muối của Cu )
* Phương pháp tăng giảm khối lượng vẫn có thể áp dụng trong trường hợp bài tập vừa có phản ứng tăng, vừa có phản ứng giảm:
Cho Fe và Zn tác dụng với Cu(NO3)2 thì độ tăng khối lượng:
Δm = |mFe + mZn - mCu| (không cần tính riêng theo từng phản ứng)

2. Ví dụ minh họa
Ví dụ 1: Ngâm 15 gam hỗn hợp Fe và Cu trong dung dịch CuSO4 dư. Phản ứng xong thu được 16 gam chất rắn. Thành phần phần trăm khối lượng của mỗi kim loại trong hỗn hợp ban đầu tương ứng là:
A. 53,34% và 46,66%
B. 46,67% và 53,33%
C. 40% và 60%
D. 60% và 40%
Ví dụ 2: Hòa tan hoàn toàn 28g Fe vào dung dịch AgNO3 dư thì khối lượng chất rắn thu được là bao nhiêu?
A. 108g
B. 10,8 g
C. 162 g
D. 21,6g
3. Bài tập vận dụng
Câu 1: Cho 1,12 gam bột Fe và 0,24 gam bột Mg tác dụng với 250 ml dung dịch CuSO4 khuấy nhẹ cho đến khi phản ứng thực hiện xong. Khối lượng kim loại có trong bình phản ứng là 1,88 gam. Tính nồng độ mol của dung dịch CuSO4 trước phản ứng.
A. 0,1M
B. 0,15M
C. 0,12M
D. 0,2M
Câu 2: Cho một hỗn hợp gồm có 1,12 gam Fe và 0,24 gam Mg tác dụng với 250 ml dung dịch CuSO4. Phản ứng thực hiện xong, người ta thu được kim loại có khối lượng là 1,88 gam. Tính nồng độ mol của dung dịch CuSO4 đã dùng.
A. 0,1M
B. 0,12M
C. 0,2M
D. 0,05M
Câu 3: Cho m1 gam Al vào 100 ml dung dịch gồm Cu(NO3)2 0,3M và AgNO3 0,3M. Sau khi các phản ứng xảy ra hoàn toàn thì thu đựơc m2 gam chất rắn X. Nếu cho m2 gam X tác dụng với lượng dư dung dịch HCl thì thu được 0,336 lít khí (đktc). Giá trị của m1 và m2 lần lượt là:
A. 8,10 và 5,43
B. 1,08 và 5,16
C. 0,54 và 5,16
D. 1,08 và 5,43.
A. 3,32g
B. 4,4g
C. 4,08g
D. 5,4g
Câu 5: Cho m g bột Fe vào 200ml dung dịch 2 muối AgNO3 0,15M và Cu(NO3)2 0,1 M, sau 1 thời gian thu được 3,84g hỗn hợp kim loại và dung dịch X. Cho 3,25g bột Zn vào dung dịch X, sau khi phản ứng xảy ra hoàn toàn thu được 3,895g hỗn hợp kim loại và dung dịch Y. Giá trị của m là:
A. 0,56
B. 1,435
C. 2,8
D. 2,24
Câu 6: Cho đinh sắt vào 200ml dung dịch CuSO4 sau phản ứng thấy khối lượng đinh sắt tăng thêm 1,6g. Tính nồng độ CuSO4 ban đầu?
A. 0,2M
B. 0,5M
C. 1M
D. 0,4M