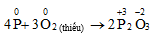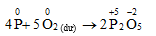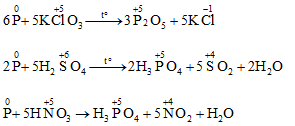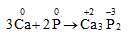Tính chất hóa học của Photpho (P) - điều chế, ứng dụng, cách nhận biết, tính chất vật lí
Với Tính chất hóa học của Photpho (P) sẽ trình bày chi tiết, đầy đủ tính chất hóa học của Photpho (P), tính chất vật lí, cách điều chế, cách nhận biết và ứng dụng của Photpho (P). Hi vọng với bài học này học sinh sẽ nắm vững được kiến thức trọng tâm về Tính chất hóa học của Photpho (P).
Photpho (P): tính chất hóa học, tính chất vật lí, nhận biết, điều chế, ứng dụng
I. Định nghĩa
- Photpho là một phi kim
- Kí hiệu: P
- Cấu hình electron: 1s22s22p63s23p3 hay [Ne]3s23p3
- Số hiệu nguyên tử: Z = 15
- Khối lượng nguyên tử: 31
- Vị trí trong bảng tuần hoàn:
+ Ô, nhóm: ô số 15, nhóm VA
+ Chu kì: 3
- Độ âm điện: 2,19
II. Tính chất hóa học
Nhận xét:
- Để đơn giản trong phản ứng hóa học người ta sử dụng kí hiệu P
- P vừa có tính khử vừa có tính oxi hóa
1. Tính khử
a. Khử phi kim mạnh hơn:O2, Cl2, S...
- Khử O2 :
Photpho trắng tác dụng với oxi ở điều kiện thường, phản ứng tỏa năng lượng ở dạng ánh sáng → gây ra hiện tượng phát quang hóa học
Photpho đỏ chỉ tác dụng với oxi ở nhiệt độ cao
- Khử : 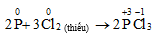
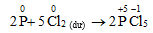
b. Khử một số hợp chất có tính oxi hóa mạnh
2. Tính oxi hóa
* P oxi hóa các kim loại hoạt động tạo ra photphua kim loại

III. Tính chất vật lí & nhận biết
- Photpho có 2 dạng thù hình là photpho trắng và photpho đỏ
|
Photpho trắng (P4) |
Photpho đỏ (P4)n |
|
|
Tính chất vật lí |
- Là chất rắn màu trắng, mềm, nhiệt độ nóng chảy thấp (44,1oC), dễ bay hơi → kém bền. - Có cấu trúc mạng tinh thể phân tử |
- Là bột màu đỏ thẫm, bền hơn photpho trắng (có nhiệt độ sôi, nhiệt độ nóng chảy cao hơn) - Có cấu trúc polime |
|
Độ tan |
- Không tan trong nước - tan được trong một số dung môi hữu cơ: CS2, benzen,… - Rất độc, gây bỏng nặng |
- Không tan trong các dung môi thông thường - Không độc, không gây bỏng da |
IV. Trạng thái tự nhiên
- Trong tự nhiên, nguyên tố P chỉ có ở dạng hợp chất
+ Ở cơ thể sống: người, động vật, thực vật,…
+ Ở vỏ trái đất: quặng apatit (3Ca3(PO4)2.CaF2 ); quặng photphorit ( Ca3(PO4)2)
V. Điều chế
Quặng than cốc cát
VI. Ứng dụng
- Điều chế H3PO4
- Sản xuất diêm
- Điều chế bom cháy, lựu đạn khói
VII. Các hợp chất quan trọng của photpho
- Axit photphoric ( H3PO4 )
- Muối của H3PO4
- Phân lân