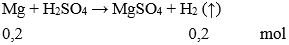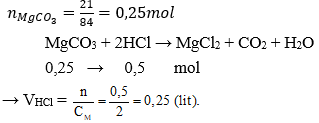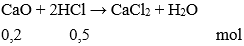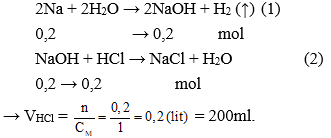Hoá học lớp 9 Bài 3: Tính chất hóa học của axit
Lý thuyết tổng hợp Hoá học lớp 9 Bài 3: Tính chất hóa học của axit chọn lọc năm 2021 – 2022 mới nhất gồm tóm tắt lý thuyết và hơn 500 bài tập ôn luyện Hoá 9. Hy vọng bộ tổng hợp lý thuyết Hoá học 9 sẽ giúp học sinh củng cố kiến thức, ôn tập và đạt điểm cao trong các bài thi trắc nghiệm môn Hoá lớp 9.
Bài 3: Tính chất hóa học của axit
A. Lý thuyết
I. Tính chất hóa học của axit
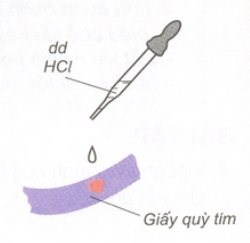
1. Axit làm đổi màu chất chỉ thị màu
- Dung dịch axit làm đổi màu quỳ tím thành đỏ.
Ví dụ:
- Trong hóa học, quỳ tím là chất chỉ thị màu để nhận biết dung dịch axit.
2. Axit tác dụng với kim loại
- Dung dịch axit tác dụng được với nhiều kim loại tạo thành muối và giải phóng khí hiđro.
Ví dụ:
3H2SO4 (dd loãng) + 2Al → Al2(SO4)3 + 3H2 (↑)
2HCl + Fe → FeCl2 + H2 (↑)
- Các kim loại Hg, Cu, Ag, Au, Pt …không tác dụng với HCl, H2SO4 loãng.
Chú ý: Axit HNO3 và H2SO4 đặc tác dụng được với nhiều kim loại nhưng không giải phóng khí hiđro.
Ví dụ:
H2SO4 + Cu(OH)2 → CuSO4 + 2H2O
HCl + NaOH → NaCl + H2O
Phản ứng của axit với bazơ được gọi là phản ứng trung hòa.
4. Axit tác dụng với oxit bazơ: Axit + oxit bazơ → muối + H2O
Ví dụ:
6HCl + Fe2O3 → FeCl3 + 3H2O
H2SO4 + MgO → MgSO4 + H2O
Ngoài ra, axit còn tác dụng với muối.
Ví dụ:
MgCO3 + 2HCl → MgCl2 + CO2 ↑ + H2O
Na2SO3 + 2HCl → 2NaCl + SO2 ↑ + H2O
II. Axit mạnh và axit yếu
Dựa vào tính chất hóa học, axit được phân làm 2 loại:
+ Axit mạnh như HCl, H2SO4, HNO3,…
+ Axit yếu như H2S, H2CO3,…

B. Bài tập trắc nghiệm
Câu 1: Chất tác dụng với dung dịch HCl tạo thành chất khí nhẹ hơn không khí là
A. Mg
B. CaCO3
C. MgCO3
D. Na2SO3
Đáp án: A
Mg + 2HCl → MgCl2 + H2 ↑
Khí H2 nhẹ hơn không khí.
Câu 2: Dãy gồm các kim loại tác dụng được với dung dịch H2SO4 loãng là:
A. Fe, Cu, Mg.
B. Zn, Fe, Cu.
C. Zn, Fe, Al.
D. Fe, Zn, Ag
Đáp án: C
Cu, Ag không phản ứng với H2SO4 loãng → đáp án C thỏa mãn.
Câu 3: Dãy oxit tác dụng với dung dịch HCl tạo thành muối và nước là
A. CO2, SO2, CuO.
B. SO2, Na2O, CaO.
C. CuO, Na2O, CaO.
D. CaO, SO2, CuO.
Đáp án: C
Oxit bazơ + axit → muối + nước
CuO, Na2O, CaO là oxit bazơ (thỏa mãn).
A. Zn
B. Na2SO3
C. FeS
D. Na2CO3
Đáp án: B
Na2SO3 + 2HCl → 2NaCl + SO2 ↑ + H2O
SO2 là khí có mùi hắc, nặng hơn không khí
SO2 làm đục nước vôi trong theo phản ứng:
SO2 + Ca(OH)2 → CaSO3↓ + H2O
Câu 5: MgCO3 tác dụng với dung dịch HCl sinh ra:
A. Chất khí cháy được trong không khí
B. Chất khí làm vẫn đục nước vôi trong.
C. Chất khí duy trì sự cháy và sự sống.
D. Chất khí không tan trong nước.
Đáp án: B
MgCO3 + 2HCl → MgCl2 + CO2 ↑ + H2O
CO2 là khí không cháy, không duy trì sự cháy, sư sống.
Khí CO2 tan ít trong nước và làm đục nước vôi trong theo phản ứng:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Câu 6: Cho phản ứng: BaCO3 + 2X → H2O + Y + CO2
X và Y lần lượt là:
A. H2SO4 và BaSO4
B. HCl và BaCl2
C. H3PO4 và Ba3(PO4)2
D. H2SO4 và BaCl2
Đáp án: B
BaCO3 + 2HCl → BaCl2 + CO2 + H2O
A. 44,8 lít
B. 4,48 lít
C. 2,24 lít
D. 22,4 lít
Đáp án: B
nMg = 4,8 : 24 = 0,2 mol
→ Vkhí = 0,2.22,4 = 4,48 lít.
Câu 8: Cho 21 gam MgCO3 tác dụng với một lượng vừa đủ dung dịch HCl 2M.
Thể tích dung dịch HCl đã dùng là:
A. 2,5 lít
B. 0,25 lít
C. 3,5 lít
D. 1,5 lít
Đáp án: B
Câu 9: Cho 0,2 mol Canxi oxit tác dụng với 500ml dung dịch HCl 1M. Khối lượng muối thu được là:
A. 2,22 g
B. 22,2 g
C. 23,2 g
D. 22,3 g
Đáp án: B
nHCl = 0,5.1 = 0,5 mol
Có 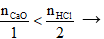
Theo PTHH có số mol muối = số mol CaO = 0,2 mol
→ mmuối = 0,2. (40 + 71) = 22,2 gam.
Câu 10: Hòa tan hết 4,6 gam Na vào H2O được dung dịch X. Thể tích dung dịch HCl 1M cần để phản ứng hết với dung dịch X là:
A. 100 ml
B. 200 ml
C. 300 ml
D. 400 ml
Đáp án: B
nNa = 4,6 : 23 = 0,2 mol
Các PTHH xảy ra: