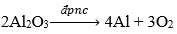Hoá học lớp 9 Bài 18: Nhôm
Lý thuyết tổng hợp Hoá học lớp 9 Bài 18: Nhôm chọn lọc năm 2021 – 2022 mới nhất gồm tóm tắt lý thuyết và hơn 500 bài tập ôn luyện Hoá 9. Hy vọng bộ tổng hợp lý thuyết Hoá học 9 sẽ giúp học sinh củng cố kiến thức, ôn tập và đạt điểm cao trong các bài thi trắc nghiệm môn Hoá lớp 9.
Bài 18: Nhôm
A. Lý thuyết
I. TÍNH CHẤT VẬT LÍ
Nhôm là kim loại màu trắng bạc, có ánh kim, dẻo, dẫn điện và dẫn nhiệt tốt. Nhôm là kim loại nhẹ (D = 2,7 g/cm3), mềm, nóng chảy ở 660°c.
II. TÍNH CHẤT HÓA HỌC
1. Nhôm có những tính chất hóa học của kim loại
a) Phản ứng với oxi và một số phi kim
Nhôm phản ứng với oxi tạo thành oxit và phản ứng với nhiều phi kim khác như S, Cl2 tạo thành muối.
Ví dụ:
Chú ý: Ở điều kiện thường, nhôm phản ứng với oxi tạo thành lớp Al2O3 mỏng bền vững, lớp oxit này bảo vệ đồ vật bằng nhôm, không cho nhôm tác dụng oxi trong không khí, nước.
b) Phản ứng với axit (HCl, H2SO4 loãng,…) giải phóng H2.
Ví dụ:
2Al + 6HCl → 2AlCl3 + 3H2
Chú ý: Nhôm không tác dụng với H2SO4 đặc nguội và HNO3 đặc, nguội,
c) Phản ứng với dung dịch muối của kim loại yếu hơn.
Ví dụ:
2Al + 3Cu(NO3)2 → 2Al(NO3)3 + 3Cu
2. Nhôm có tính chất hóa học nào khác?
Nhôm phản ứng với dung dịch kiềm.
Ví dụ:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
III. ỨNG DỤNG
Nhôm và hợp kim của nhôm được sử dụng rộng rãi trong đời sống: đồ dùng gia đình, dây dẫn điện, vật liệu xây dựng....
Đuyra (hợp kim của nhôm) nhẹ và bền được dùng trong công nghiệp chế tạo máy bay, ô tô, tàu vũ trụ…
IV. SẢN XUẤT NHÔM
Nguyên liệu: quặng bôxit có thành phần chủ yếu là Al2O3.
Phương trình hóa học:

B, Bài tập trắc nghiệm
Câu 1: Nhôm là kim loại
A. dẫn điện và nhiệt tốt nhất trong số tất cả kim loại.
B. dẫn điện và nhiệt đều kém.
C. dẫn điện tốt nhưng dẫn nhiệt kém.
D. dẫn điện và nhiệt tốt nhưng kém hơn đồng.
Đáp án: D
Nhôm là kim loại dẫn điện và nhiệt tốt nhưng kém hơn đồng.
Thứ tự dẫn điện, dẫn nhiệt: Ag, Cu, Au, Al, Fe,…
Câu 2: Người ta có thể dát mỏng được nhôm thành thìa, xoong, chậu, giấy gói bánh kẹo là do nhôm có tính :
A. dẻo
B. dẫn điện
C. dẫn nhiệt
D. ánh kim
Đáp án: A
Người ta có thể dát mỏng được nhôm thành thìa, xoong, chậu, giấy gói bánh kẹo là do nhôm có tính dẻo
Câu 3: Một kim loại có khối lượng riêng là 2,7 g/cm3, nóng chảy ở 660oC. Kim loại đó là:
A. sắt
B. nhôm
C. đồng
D. bạc
Đáp án: B
Một kim loại có khối lượng riêng là 2,7 g/cm3, nóng chảy ở 660oC => kim loại là Al
Câu 4: Nhôm bền trong không khí là do
A. nhôm nhẹ, có nhiệt độ nóng chảy cao.
B. nhôm không tác dụng với nước.
C. nhôm không tác dụng với oxi.
D. có lớp nhôm oxit mỏng bảo vệ.
Đáp án: D
Nhôm bền trong không khí là do có lớp nhôm oxit mỏng bảo vệ.
Câu 5: Một kim loại có những tính chất (vật lí và hóa học) như sau:
- Hợp kim của nó với các kim loại khác, được ứng dụng trong công nghệ chế tạo máy bay, tên lửa.
- Phản ứng mãnh liệt với axit clohiđric.
- Phản ứng với dung dịch kiềm, giải phóng khí hiđro
- Nhẹ, dẫn điện và dẫn nhiệt tốt. Đó là kim loại:
A. kẽm
B. vàng
C. nhôm
D. chì
Đáp án: C
Vì là kim loại phản ứng với dung dịch kiềm, giải phóng khí hiđro và nhẹ dẫn điện, dẫn nhiệt tốt
=> kim loại đó là Al
Câu 6: X là kim loại nhẹ, dẫn điện tốt , phản ứng mạnh với dung dịch HCl, tan trong dung dịch kiềm và giải phóng H2. X là:
A. Al
B. Mg
C. Cu
D. Fe
Đáp án: A
Câu 7: Giải thích tại sao để điều chế Al người ta điện phân Al2O3 nóng chảy mà không điện phân AlCl3 nóng chảy là:
A. AlCl3 nóng chảy ở nhiệt độ cao hơn Al2O3.
B. AlCl3 không nóng chảy mà thăng hoa.
C. Điện phân AlCl3 tạo ra Cl2 rất độc.
D. Điện phân Al2O3 cho ra Al tinh khiết hơn.
Đáp án: B
Để điều chế Al người ta điện phân Al2O3 nóng chảy mà không điện phân AlCl3 nóng chảy vì AlCl3 không nóng chảy mà thăng hoa.
Câu 8: Trong công nghiệp người ta điều chế nhôm bằng cách
A. Khử Al2O3 bằng khí CO.
B. Khử Al2O3 bằng khí H2.
C. dùng Na tác dụng với dung dịch AlCl3.
D. điện phân nóng chảy Al2O3/criolit.
Đáp án: D
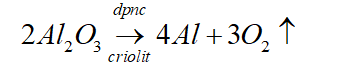
Câu 9: Nguyên liệu chính để sản xuất nhôm là:
A. criolit
B. quặng boxit
C. điện
D. than chì.
Đáp án: B
Nguyên liệu chính để sản xuất nhôm là quặng boxit (Al2O3)
Câu 10: Khi điện phân Al2O3 nóng chảy người ta thêm criolit (Na3AlF6) với mục đích:
1. Làm hạ nhiệt độ nóng chảy của Al2O3.
2. Làm cho tính dẫn điện cao hơn.
3. Để thu được F2 ở anot thay vì là O2.
4. Tạo hỗn hợp nhẹ hơn Al để bảo vệ Al.
Các lý do nêu đúng là:
A. Chỉ có 1
B. 1 và 2
C. 1 và 3
D. 1, 2 và 4
Đáp án: D
Khi điện phân Al2O3 nóng chảy người ta thêm criolit (Na3AlF6) với mục đích:
1. Làm hạ nhiệt độ nóng chảy của Al2O3.
2. Làm cho tính dẫn điện cao hơn.
4. Tạo hỗn hợp nhẹ hơn Al để bảo vệ Al.
Câu 11: Cho các kim loại: Cu, Zn, Fe, Mg, Ag, Al. Những kim loại nào không tác dụng với dd HNO3 đặc nguội?
A. Fe, Mg, Ag, Al.
B. Cu, Mg, Ag, Al.
C. Fe, Al.
D. Tất cả các kim loại
Đáp án: C
2 kim loại không phản ứng với dung dịch HNO3 đặc nguội là Fe và Al
Câu 12: Cho các phát biểu về phản ứng nhiệt nhôm, phát biểu đúng là
A. Nhôm chỉ có thể khử các oxit kim loại đứng sau H trong dãy hoạt động hóa học.
C. Nhôm chỉ có thể khử các oxit kim loại đứng trước và đứng sau Al trong dãy hoạt động hóa học với điều kiện kim loại đó dễ bay hơi.
D. Nhôm khử tất cả các oxit kim loại.
Đáp án: B
Phát biểu đúng là: Nhôm chỉ có thể khử các oxit kim loại đứng sau Al trong dãy hoạt động hóa học.
Câu 13: Chỉ dùng 1 chất để phân biệt 3 kim loại sau: Al, Ba, Mg?
A. Dung dịch HCl
B. Nước
C. Dung dịch NaOH
D. Dung dịch H2SO4
Đáp án: B
Để phân biệt 3 kim loại Al, Ba, Mg ta dùng nước. Cho nước vào 3 mẫu kim loại, kim loại tốt trong nước và sủi bọt khí là Ba, 2 kim loại không tan trong nước là Al và Mg.
Ba + 2H2O → Ba(OH)2 + H2 ↑
- Lấy dung dịch Ba(OH)2 vừa thu được đổ vào mẫu 2 kim loại còn lại, kim loại nào tan, sủi bọt khí là Al, kim loại không có hiện tượng gì là Mg
2Al + Ba(OH)2 + 2H2O → Ba(AlO2)2 + 3H2 ↑
Câu 14: Chỉ dùng nước nhận biết được 3 chất rắn riêng biệt nào?
A. Al, Fe, Cu
B. Al, Na, Fe
C. Fe, Cu, Zn
D. Ag, Cu, Fe
Đáp án: B
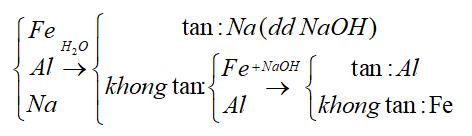
Câu 15: Có 3 lọ không nhãn, mỗi lọ đựng một trong các chất rắn sau: Cu, Mg, Al. Thuốc thử để nhận biết 3 chất trên là:
A. Lần lượt NaOH và HCl.
B. Lần lượt là HCl và H2SO4 loãng.
C. Lần lượt NaOH và H2SO4 đặc nóng.
D. Tất a, b, c đều đúng.
Đáp án: A
Dể nhận biết 3 chất rắn trên thì ta dùng lần lượt dung dịch NaOH và HCl.
- Cho dung dịch NaOH vào 3 ống nghiệm đựng chất rắn, chất rắn nào tan và sủi bọt khí là Al, 2 ống không hiện tượng là Cu và Mg
PTHH: 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2 ↑
- Cho dung dịch HCl vào 2 chất rắn còn lại, chất rắn nào tan và sủi bọt khí là Mg, chất rắn không hiện tượng là Cu
PTHH: Mg + 2HCl → MgCl2 + H2↑
Câu 16: Trong vỏ Trái Đất có nhiều quặng nhôm hơn sắt nhưng giá mỗi tấn nhôm cao hơn nhiều so với giá mỗi tấn sắt. Lí do vì:
A. Chuyển vận quặng nhôm đến nhà máy xử lí tốn kém hơn vận chuyển quặng sắt
C. Nhôm có nhiều công dụng hơn sắt nên nhà sản xuất có thể có lợi nhuận nhiều hơn
D. Quặng nhôm ở sâu trong lòng đất trong khi quặng sắt từng thấy ngay trên mặt đất
Đáp án: B
Nguyên liệu để sản xuất nhôm là quặng bôxit có thành phần chủ yếu là Al2O3. Sử dụng phương pháp điện phân hỗn hợp nóng chảy của nhôm oxit và criolit nên tốn kém hơn khi điều chế sắt
Câu 17: Trong các kim loại sau: Cu, Fe, Pb, Al người ta thường dùng kim loại nào để làm vật liệu dẫn điện hay dẫn nhiệt?
A. Chỉ có Cu
B. Cu và Al
C. Fe và Al
D. Chỉ có Al
Đáp án: B
Trong thực tế người ta thường sử dụng 2 kim loại để làm vật liệu dẫn điện và dẫn nhiệt là Cu và Al.
Câu 18: Kim loại nhôm có độ dẫn điện tốt hơn kim loại:
A. Cu, Ag
B. Ag
C. Fe, Cu
D. Fe
Đáp án: D
Kim loại dẫn điện tốt nhất là Ag sau đó đến Cu, Au, Al, Fe,..
Câu 19: Công thức hóa học của nhôm là:
A. Al.
B. Cu.
C. Fe.
D. Zn.
Đáp án: A
Câu 20: Tên gọi của Al2O3 và Al(OH)3 lần lượt là:
A. Nhôm oxit và nhôm (III) hidroxit.
B. Nhôm (III) oxit và nhôm hidroxit.
C. Nhôm oxit và nhôm hidroxit.
D. Nhôm (III) oxit và nhôm (III) hidroxit.
Đáp án: C
Al2O3: nhôm oxit
Al(OH)3: nhôm hiđroxit
Câu 21: Sản phẩm khi đốt cháy nhôm trong khí oxi (O2) là:
A. AlO.
B. Al2O3.
C. Al3O2.
D. Al2O2.
Đáp án: B
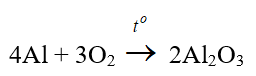
Câu 22: Cho phản ứng: Al + Cl2 ->…. Tổng hệ số tối giản của phương trình là:
A. 4
B. 3
C. 7
D. 9
Đáp án: C
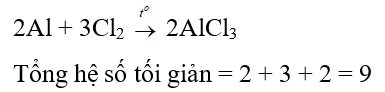
Câu 23: Nhôm không tác dụng được với:
A. HCl.
B. H2SO4 loãng.
C. NaOH.
D. NaCl.
Đáp án: D
Al không phản ứng được với NaCl
Câu 24: Kim loại nào dưới đây tan được trong dung dịch kiềm :
A. Mg
B. Al
C. Fe
D. Ag
Đáp án: B
Do oxit và hidroxit của nhôm có tính lưỡng tính do đó nhôm có thể tan trong dd kiềm
Câu 25: Hi đroxit nào sau đây vừa tác dụng được với dung dịch ba zơ vừa tác dụng được với dung dịch axit?
A. Fe(OH)2
B. Fe(OH)3
C. Al(OH)3
D. Mg(OH)2
Đáp án: C
Hi đroxit vừa tác dụng được với dung dịch ba zơ vừa tác dụng được với dung dịch axit Al(OH)3
Câu 26: Quặng nào sau đây chứa thành phần chính là Al2O3:
A. Boxit.
B. Pirit.
C. Đolomit.
D. Apatit.
Đáp án: A
Thành phần chính của quặng boxit là Al2O3
Thành phần chính của quặng Pirit là FeS2
Thành phần chính của quặng Đolomit là: MgCO3. CaCO3
Thành phần chính của quặng Apatit là: Ca3(PO4)2
Câu 27: Nguyên liệu sản xuất nhôm là quặng :
A. Hematit
B. Manhetit
C. Boxit
D. Pirit
Đáp án: C
Quặng Boxit: Al2O3.nH2O
Quặng Pirit(Pirit sắt): FeS2
Quặng Hematit: Fe2O3
Quặng Manhetit: Fe3O4
Câu 28: Nguyên liệu để sản xuất nhôm là quặng bôxit. Thành phần chính của quặng bôxit là:
A. Fe2O3
B. Al2O3
C. NaAlO2
D. AlCl3
Đáp án: B
Thành phần chính của quặng bôxit là Al2O3
Câu 29: Hợp chất nào của nhôm dưới đây tan nhiều được trong nước ?
A. Al2O3
B. Al(OH)3
C. AlCl3
D. AlPO4
Đáp án: C
AlCl3 là muối dễ tan trong nước
Câu 30: Hợp chất nào dưới đây của nhôm tan nhiều trong nước?
A. AlCl3
B. Al2O3
C. Al(OH)3
D. AlPO4
Đáp án: A
Hợp chất dưới đây của nhôm tan nhiều trong nước: AlCl3
Câu 31: Không được dùng chậu nhôm để chứa nước vôi trong , do
A. nhôm tác dụng được với dung dịch axit.
B. nhôm tác dụng được với dung dịch bazơ.
C. nhôm đẩy được kim loại yếu hơn nó ra khỏi dung dịch muối.
D. nhôm là kim loại hoạt động hóa học mạnh
Đáp án: B
Al + Ca(OH)2 + H2O → H2 + Ca(AlO2)2
Câu 32: Kim loại vừa tác dụng với dung dịch HCl vừa tác dụng với dung dịch KOH là:
A. Fe
B. Cu
C. Al
D. Mg
Đáp án
Kim loại vừa tác dụng với dung dịch HCl vừa tác dụng với dung dịch KOH là: Al
Đáp án: C
Câu 33: Kim loại nào sau đây có tính chất hóa học lưỡng tính?
A. Fe
B. Na
C. Al
D. Ba
Đáp án
Kim loại có tính chất hóa học lưỡng tính Al
Đáp án: C