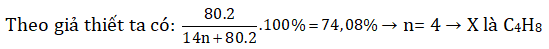Cách giải Bài tập Etilen, Axetilen cộng H2, Br2 hay, chi tiết
Cách giải Bài tập Etilen, Axetilen cộng H2, Br2 hay, chi tiết Hóa học lớp 9 với đầy đủ lý thuyết, phương pháp giải và bài tập có lời giải cho tiết sẽ giúp học sinh nắm được Cách giải Bài tập Etilen, Axetilen cộng H2, Br2 hay, chi tiết.
Cách giải Bài tập Etilen, Axetilen cộng H2, Br2 hay, chi tiết
Lý thuyết và Phương pháp giải
I. Cơ sở lý thuyết:
- Liên kết π là liên kết kém bền vững, nên chúng dễ bị đứt ra để tạo thành liên kết với các nguyên tử khác.
- Khi có mặt chất xúc tác như Ni, Pt, Pd ở nhiệt độ thích hợp, hidrocacbon không no cộng hidro hoặc brom vào liên kết pi.
- PTHH của phản ứng tổng quát:
CnH2n+2-2k + kH2 → CnH2n+2 (1)
(k là số liên kết trong phân tử)
CnH2n+2-2k + kBr2 → CnH2n+2-2kBr2k (2)
II. Phương pháp giải:
-Xác định PTHH tổng quát.
-Dựa vào PTHH tổng quát tính số mol H2 hoặc Br2 phản ứng.
(Có thể áp dụng định luật bảo toàn khối lượng để lập hệ phương trình giải toán)
Chú ý:
- Độ giảm số mol của hỗn hợp luôn luôn bằng số mol H2 hoặc Br2 tham gia phản ứng.
- Tổng số mol hidrocacbon sản phẩm và số mol hidrocacbon nguyên liệu (dư) luôn luôn bằng số mol hidrocacbon nguyên liệu ban đầu.

Bài tập vận dụng
Bài 1: Dẫn 1,68 lít hỗn hợp khí X gồm 2 hidrocacbon vào bình đựng dung dịch brom (dư). Sau khi pư xảy ra hoàn toàn , có 4 gam brom đã pư và còn lại 1,12lít khí. Nếu đốt cháy hoàn toàn 1,68 lít X thì sinh ra 2,8 lít khí CO2 .CTPT của 2 hidrocacbon là (biết các khí đều đo ở điều kiện tiêu chuẩn)
A. CH4 và C2H4 B. CH4 và C3H4
C. CH4 và C3H6 D. C2H6 và C3H6
Hướng dẫn:
nX = 1,68/22,4 = 0,075 mol; nBr2 = 0,025 mol
n Khí còn lại = 1,12/22,4 = 0,05 mol → nkhí pư với Br2 = nX - n khí còn lại = 0,075 - 0,05 = 0,025 mol
→ nkhí pư với Br2 = nBr2 = 0,025 mol
→ Khí phản ứng với Br2 là anken → nanken = 0,025 mol
Khí còn lại là ankan, nankan = 0,05 mol
nCO2 = 2,8/22,4 = 0,125 mol
→ Đốt cháy hoàn toàn 0,075mol X thì sinh ra 0,125 mol khí CO2
→ Số C trung bình của X là: 0,125/0,075 = 1,67
→ Trong X phải chứa CH4 → nCH4 = 0,05 mol
Bảo toàn nguyên tố C: 0,05.1 + 0,025.n = 0,125 (n là số nguyên tử C trong anken)
→ n = 3 → anken đó là C3H6
→ Đáp án C
Bài 2: Cho hiđrocacbon X phản ứng với brom (trong dung dịch) theo tỉ lệ mol 1:1, thu được chất hữu cơ Y (chứa 74,08% Br về khối lượng). Khi X phản ứng với HBr thì thu được 2 sản phẩm hữu cơ khác nhau . Tên gọi của X là
A. But-1-en B. But-2-en
C. Propilen D. xiclopropan
Hướng dẫn:
X phản ứng với Br2 theo tỉ lệ 1:1 nên CTTQ của X là CnH2n
CnH2n + Br2 → CnH2nBr2
→ Chất hữu cơ Y là CnH2nBr2
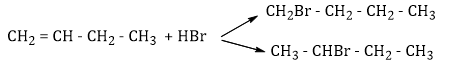
Khi X phản ứng với HBr cho 2 sản phẩm hữu cơ khác nhau → X là but-1-en
Bài 3: Cho H2 và 1 anken có thể tích bằng nhau qua niken nung nóng ta thu được hỗn hợp A . Biết tỉ khối hơi của A với H2 là 23,2. Hiệu suất phản ứng hiđro hóa là 75%. Công thức phân tử của anken là
A. C2H4 B. C3H6 C. C4H8 D. C5H10
Hướng dẫn:
Trong cùng 1 điều kiện thì tỉ lệ thể tích cũng chính là tỉ lệ về số mol
Theo giả thiết ta chọn: nH2 = nCnH2n = 1 mol
CnH2n + H2 → CnH2n+2
Theo phương trình , số mol khí giảm chính là số mol của H2
H% = 75% → nH2(pư) = 0,75 mol
→ Số mol khí sau phản ứng là: n khí sau pư = nH2(sau pư) + nCnH2n(sau pư) + nCnH2n+2 = 1 + 1 - 0,75 = 1,25 mol
Áp dụng định luật bảo toàn khối lượng ta có: mA = mH2 + mCnH2n = 2+14n
→ MA = mA/nA → 23.2,2 = mA/1,25 → mA = 58 → 2 + 14n = 58 → n = 4 → anken là C4H8
→ Đáp án C