Trắc nghiệm Hóa học 9 Bài 44 có đáp án năm 2021 - 2022
Để giúp học sinh có thêm tài liệu tự luyện môn Hóa học lớp 9 năm 2021 đạt kết quả cao, chúng tôi biên soạn Trắc nghiệm Hóa học 9 Bài 0 có đáp án mới nhất gồm các câu hỏi trắc nghiệm đầy đủ các mức độ nhận biết, thông hiểu, vận dụng, vận dung cao.
Trắc nghiệm Hóa học 9 Bài 44: Rượu etylic
Bài 1: Cho rượu etylic 80o tác dụng với natri dư. Số phản ứng hóa học xảy ra là
A. 1
B. 2.
C. 3
D. 4.
Lời giải
Rượu etylic 80o gồm C2H5OH và H2O => Na phản ứng với H2O trước, sau đó phản ứng với C2H5OH
=> có 2 phản ứng xảy ra
2Na + 2H2O → 2NaOH + H2 ↑
2C2H5OH + 2Na → 2C2H5ONa + H2↑
Đáp án: B
Bài 2: Dãy gồm tất cả các chất đều có khả năng tác dụng với rượu etylic là
A. KOH, Na, CH3COOH, O2.
B. Na, C2H4, CH3COOH, O2.
C. Na, K, CH3COOH, O2.
D. Ca(OH)2, K, CH3COOH, O2.
Lời giải
Dãy gồm tất cả các chất đều có khả năng tác dụng với rượu etylic là: Na, K, CH3COOH, O2.
2C2H5OH + 2Na → 2C2H5ONa + H2↑
2C2H5OH + 2K → 2C2H5OK + H2↑
C2H5OH + CH3COOH 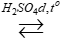 CH3COOC2H5 + H2O
CH3COOC2H5 + H2O
C2H5OH + 3O2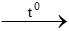 2CO2 + 3H2O
2CO2 + 3H2O
Đáp án: C
Bài 3: Thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 13,8 gam rượu etylic nguyên chất là
A. 5,60
B. 22,4
C. 8,36
D. 20,16
Lời giải
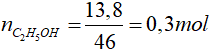
C2H5OH + 3O2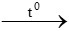 2CO2 + 3H2O
2CO2 + 3H2O
0,3 mol → 0,9 mol
⇒ VO2 = 0,9.22,4 = 20,16
Đáp án: D
Bài 4: Cho 23 gam rượu etylic nguyên chất tác dụng với natri dư. Thể tích khí H2 thoát ra (đktc) là
A. 2,8 lít
B. 5,6 lít.
C. 8,4 lít
D. 11,2 lít.
Lời giải
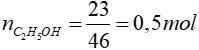
2C2H5OH + 2Na → 2C2H5ONa + H2↑
0,5 mol → 0,25 mol
⇒ VH2 = 0,25.22,4 = 5,6
Đáp án: B
Bài 5: Cho 11,2 lít khí etilen (đktc) tác dụng với nước có axit sunfuric (H2SO4) làm xúc tác, thu được 9,2 gam rượu etylic. Hiệu suất phản ứng là
A. 50%. B. 30%.
C. 60%. D. 40%.
Lời giải
Số mol khí etilen là: 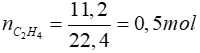
PTHH: C2H4 + H2O 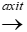 C2H5OH
C2H5OH
0,5 mol → 0,5 mol
=> khối lượng rượu etylic thu được theo lí thuyết là: m = 0,5.46 = 23 gam
Đề bài cho khối lượng rượu etylic thu được thực tế là 9,2 gam
Vì tính theo chất sản phẩm => Hiệu suất phản ứng
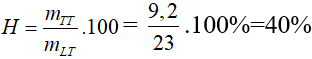
Đáp án: D

Bài 6: Cần bao nhiêu thể tích rượu nguyên chất cho vào 60 ml dung dịch rượu 40o thành rượu 60o?
A. 30 ml
B. 40 ml
C. 50 ml
D. 60 ml.
Lời giải
Thể tích rượu nguyên chất trong dung dịch lúc đầu là
Độ rượu = 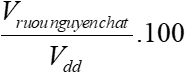
=> Vrượu nguyên chất = 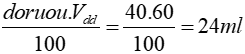
Thể tích dung dịch rượu nguyên chất sau khi pha là: 24 + x (ml)
Thể tích dung dịch rượu lúc sau là: 60 + x (ml)
Thay vào công thức tính độ rượu lúc sau, ta có:
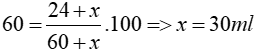
Vậy nếu ta thêm 30 ml rượu nguyên chất vào 60 ml rượu 40o thì sẽ thành rượu 60o
Đáp án: A
Bài 7: Khí CO2 sinh ra khi lên men rượu một lượng glucozơ được dẫn vào dung dịch Ca(OH)2 dư tạo được 40 gam kết tủa. Khối lượng ancol etylic thu được là
A. 18,4 gam
B. 16,8 gam
C. 16,4 gam
D. 17,4 gam.
Lời giải
Ta có: 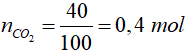
PTHH: C6H12O6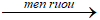 2CO2 + 2C2H5OH
2CO2 + 2C2H5OH
=> nrượu = nCO2 => mrượu = 0,4 . 46 = 18,4
Đáp án: A
Bài 8: Lên men hoàn toàn m gam glucozơ thành ancol etylic. Toàn bộ khí CO2 sinh ra trong quá trình này được hấp thụ hết vào dung dịch Ca(OH)2 dư tạo ra 40 gam kết tủa. Nếu hiệu suất của quá trình lên men là 75% thì giá trị của m là
A. 60
B. 58
C. 30
D. 48
Lời giải
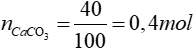
CO2 + Ca(OH)2 → CaCO3↓ + H2O
⇒ nCO2 = nCaCO3 = 0,4 mol
C6H12O6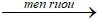 2CO2 + 2C2H5OH
2CO2 + 2C2H5OH
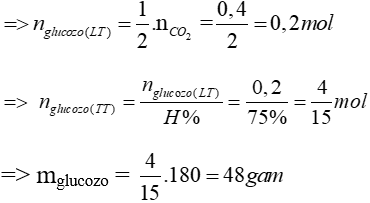
Đáp án: D
Bài 9: Công thức tính độ rượu là
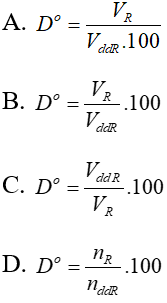
Lời giải
Đáp án: B
Bài 10: Hòa tan hết 80 ml rượu etylic vào nước để được 400 ml dung dịch rượu. Độ rượu là
A. 80o
B. 40o
C. 20o
D. 46o
Lời giải
Công thức tính độ rượu là 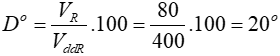
Đáp án: C
Bài 11: Số mol rượu etylic có trong 200 ml rượu C2H5OH 46o (D = 0,8 g/ml) là
A. 0,8 mol
B. 1,6 mol
C. 3,2 mol
D. 0,4 mol
Lời giải
Công thức tính độ rượu là
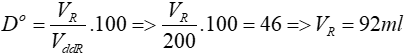
Ta có: mR = VR . DR = 92.0,8 = 73,6 gam
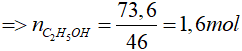
Đáp án: B
Bài 12: Lên men 18 gam glucozơ thu được 50 ml rượu C2H5OH Do (D = 0,8 g/ml). Giá trị Do là
A. 10o
B. 11,5o
C. 22,5o
D. 23o
Lời giải
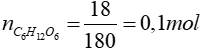
PTHH: C6H12O6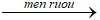 2C2H5OH + 2CO2
2C2H5OH + 2CO2
0,1 mol → 0,2 mol
⇒ mC2H5OH = 0,2.46 = 9,2 gam
Ta có: 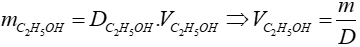
=> độ rượu 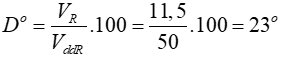
Đáp án: D
Bài 13: Thể tích ancol etylic 92o cần dùng là bao nhiêu để điều chế được 2,24 lít C2H4 (đktc). Cho biết hiệu suất phản ứng đạt 62,5% và D = 0,8 g/ml.
A. 8 ml
B. 10 ml
C. 12,5 ml
D. 3,9 ml
Lời giải
C2H5OH → C2H4 + H2O
nC2H4 = 0,1 (mol) = nC2H5OH nguyên chất lý thuyết
Trên thực tế hiệu suất phản ứng là 62,5%
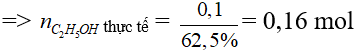
=>mC2H5OH= 7,36 gam
D = 0,8 g/ml => thể tích C2H5OH nguyên chất cần dùng là
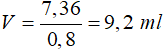
Độ của rượu được tính bằng số ml rượu nguyên chất trong 100 ml dung dịch rượu.
Áp dụng điều này => cứ 100ml dung dịch rượu 92 độ có 92 ml rượu nguyên chất.
Vậy để có 9,2 ml rượu nguyên chất cần thể tích dd rượu là V = 10ml.
Đáp án: B
Bài 14: Cho 10 ml dung dịch ancol etylic 46o tác dụng với Na dư. Xác định thể tích H2 tạo thành? (biết khối lượng riêng của ancol etylic là 0,8 g/ml)
A. 2,128 lít
B. 0,896 lít
C. 3,360 lít
D. 4,256 lít
Lời giải
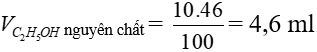
mC2H5OH nguyên chất = V.D = 4,6.0,8 = 3,68 (g)
VH2O = 104,6 =5,4 ml => mH2O = 5,4.1 = 5,4 g
Sơ đồ phản ứng
C2H5OH 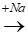 H2
H2
H2O 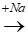 H2
H2
⇒ nH2 = 0,5.nC2H5OH + 0,5.nH2O = 0,19 mol
=> V = 0,19.22,4 = 4,256 lít
Đáp án: D
Bài 15: Cho 10,1 gam dung dịch rượu etylic tác dụng với kim loại Na dư thu được 2,8 lít H2 (đktc). Biết khối lượng riêng của rượu etylic là 0,8 g/ml và của nước là 1 g/ml. Xác định độ rượu đem tham gia phản ứng?
A. 92,74o
B. 96o
C. 73,92o
D. 97,24o
Lời giải
Vì dung dịch rượu gồm rượu etylic và nước nên ta gọi:
nH2O x xmol và nC2H5OH = y mol
PTHH:
2Na + 2H2O → 2NaOH + H2↑ (1)
x mol → 0,5.x mol
2Na + 2C2H5OH → 2C2H5ONa + H2↑
y mol → 0,5.y mol
Ta có hệ phương trình:
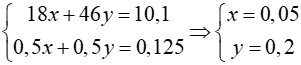
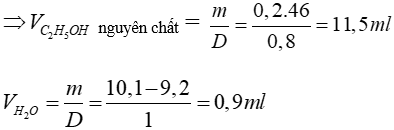
=> Vdd rượu = VH2O + VC2H5OH = 0,9 + 11,5 = 12,4 ml
=> Độ rượu 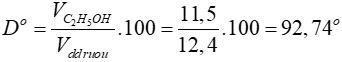
Đáp án: A
Bài 16: Công thức cấu tạo của rượu etylic là
A. CH2–CH3–OH.
B. CH3–O–CH3.
C. CH2–CH2–OH2.
D. CH3–CH2–OH.
Lời giải
Công thức cấu tạo của rượu etylic là CH3–CH2–OH.
Đáp án: D
Bài 17: Tính chất vật lí của rượu etylic là
A. chất lỏng không màu, nhẹ hơn nước, tan vô hạn trong nước, hòa tan được nhiều chất như iot, benzen,…
B. chất lỏng màu hồng , nhẹ hơn nước, tan vô hạn trong nước, hòa tan được nhiều chất như: iot, benzen,…
C. chất lỏng không màu, không tan trong nước, hòa tan được nhiều chất như: iot, benzen,…
D. chất lỏng không màu, nặng hơn nước, tan vô hạn trong nước, hòa tan được nhiều chất như: iot, benzen,…
Lời giải
Tính chất vật lí của rượu etylic là chất lỏng không màu, nhẹ hơn nước, tan vô hạn trong nước, hòa tan được nhiều chất như iot, benzen,…
Đáp án: A
Bài 18: Độ rượu là
A. số ml rượu etylic có trong 100 ml hỗn hợp rượu với nước.
B. số ml nước có trong 100 ml hỗn hợp rượu với nước.
C. số gam rượu etylic có trong 100 ml hỗn hợp rượu với nước.
D. số gam nước có trong 100 gam hỗn hợp rượu với nước.
Lời giải
Độ rượu là số ml rượu etylic có trong 100 ml hỗn hợp rượu với nước.
Đáp án: A
Bài 19: Trên một chai rượu có nhãn ghi 25o có nghĩa là
A. cứ 1 lít nước thì có 0,25 lít ancol nguyên chất
B. cứ 1 kg dung dịch thì có 0,25 kg ancol nguyên chất
C. cứ 1 lít dung dịch thì có 0,25 kg ancol nguyên chất
D. cứ 1 lít dung dịch thì có 0,25 lít ancol nguyên chất
Lời giải
Trên một chai rượu có nhãn ghi 25o có nghĩa là cứ 1 lít dung dịch thì có 0,25 lít ancol nguyên chất.
Đáp án: D
Bài 20: Cho rượu etylic nguyên chất tác dụng với kali dư. Số phản ứng hóa học xảy ra là
A. 1
B. 2
C. 3
D. 4.
Lời giải
Rượu etylic nguyên chất là C2H5OH => chỉ xảy ra 1 phản ứng với K
2C2H5OH + 2K → 2C2H5OK + H2 ↑
Đáp án: A


