Trắc nghiệm Hóa học 9 Bài 35 có đáp án năm 2021 - 2022
Để giúp học sinh có thêm tài liệu tự luyện môn Hóa học lớp 9 năm 2021 đạt kết quả cao, chúng tôi biên soạn Trắc nghiệm Hóa học 9 Bài 35 có đáp án mới nhất gồm các câu hỏi trắc nghiệm đầy đủ các mức độ nhận biết, thông hiểu, vận dụng, vận dung cao.
Trắc nghiệm Hóa học 9 Bài 35: Cấu tạo phân tử hợp chất hữu cơ
Bài 1: Phân tử hợp chất hữu cơ A có 2 nguyên tố. Đốt cháy hoàn toàn 3 gam chất A thu được 5,4 gam nước. Biết khối lượng mol của A là 30 gam. Công thức phân tử của A là
A. C2H6 B. C3H8
C. C2H4 D. CH3
Lời giải
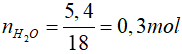
Hợp chất hữu có A có 2 nguyên tố, khi đốt cháy thu được nước => A chứa C và H
nH = 2.nH2O = 0,6 mol
Vì A chỉ chứa C và H => mA = mC + mH = 3 - 0,6 = 2,4 gam
=> nC = 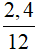 = 0,2 mol
= 0,2 mol
=> nC : nH = 0,2 : 0,6 = 1 : 3
=> Công thức đơn giản nhất của A là (CH3)n
M = 30 => n = 2
=> CTPT của A là C2H6
Đáp án: A
Bài 2: Vitamin A là một chất dinh dưỡng thiết yếu cho con người. Trong thực phẩm, vitamin A tồn tại ở dạng chính là retinol (chứa C, H, O) trong đó thành phần % khối lượng H và O tương ứng là 10,49% và 5,594%. Biết CTPT của retinol là:
A. C18H30O
B. C22H26O
C. C21H18O
D. C20H30O
Lời giải
Vì A chỉ chứa C, H và O
=> %mC = 100% - %mH - %mO = 100% - 10,49% - 5,594% = 83,916%
=> x : y : z = 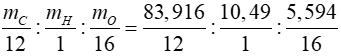
= 6,993 : 10,49 : 0,349 = 20 : 30 : 1
Vì renitol chứa một nguyên tử O => z = 1
=> x = 20 và y = 30
=> CTPT của retinol là C20H30O
Đáp án: D
Bài 3: Một hợp chất hữu cơ Y khi đốt cháy hoàn toàn thu được CO2 và H2O có số mol bằng nhau. Đồng thời số mol oxi tối thiểu cần dùng bằng 4 lần số mol của Y. Biết trong Y chỉ chứa 1 nguyên tử O. Công thức phân tử của Y là
A. C2H6O
B. C4H8O
C. C3H6O
D. C3H8O.
Lời giải
Gọi CTPT của Y có dạng CxHyO
Vì đầu bài chỉ cho các tỉ lệ, không cho số mol cụ thể => giả sử đốt cháy 1 mol Y
CxHyO + 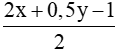 O2
O2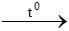 xCO2 +
xCO2 + 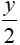 H2O
H2O
1 mol →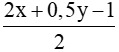 mol → x mol →
mol → x mol →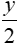 mol
mol
Phản ứng thu được số mol CO2 và H2O bằng nhau => x =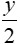 (1)
(1)
Số mol oxi cần dùng bằng 4 lần số mol của Y =>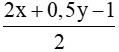 =4 (2)
=4 (2)
Thay (1) vào (2) ta có: 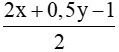 = 4 => 1,5y – 1 = 8 => y = 6
= 4 => 1,5y – 1 = 8 => y = 6
Thay y = 6 vào (1) => x = 3
=> CTPT của Y là C3H6O
Đáp án: C
Bài 4: Đốt cháy hoàn toàn 0,42 gam hợp chất hữu cơ X rồi dẫn toàn bộ sản phẩm cháy (chỉ gồm CO2 và H2O) lần lượt qua bình (1) đựng H2SO4 đặc dư, bình (2) đựng dung dịch KOH dư. Kết thúc thí nghiệm thấy khối lượng bình (1) và bình (2) tăng lần lượt là 0,54 gam và 1,32 gam. Biết rằng 0,42 gam X chiếm thể tích hơi bằng thể tích của 0,192 gam O2 ở cùng điều kiện nhiệt độ và áp suất. Công thức phân tử của X là
A. C5H10O
B. C5H10
C. C4H6O
D. C3H2O2.
Lời giải
Cho hỗn hợp sản phẩm qua bình (1) đựng H2SO4 đặc, dư => H2O bị giữ lại
=>mH2O = 0,54 gam => nH2O = 0,03 mol => nH (trong X) = 2.nH2O = 0,06
Cho qua bình (2) đựng KOH dư => CO2 bị giữ lại
=>mCO2 = 1,32 gam => nCO2 = 0,03 mol => nC = nCO2 = 0,03
Vì đốt cháy X chỉ thu được CO2 và H2O => X gồm C, H và có thể có O
Ta có: mC + mH = 0,03.12 + 0,06 = 0,42 = mX
=> trong X không chứa O
=> nC : nH = 0,03 : 0,06 = 1 : 2
=> CTĐGN của X là CH2 => CTPT của X có dạng (CH2)n
0,42 gam X chiếm thể tích hơi bằng thể tích của 0,192 gam O2
=> nX = 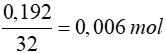
=> MX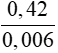 = 70 => 14n = 70 => n = 5
= 70 => 14n = 70 => n = 5
=> CTPT X là C5H10
Đáp án: B
Bài 5: Có bao nhiêu CTPT hợp chất hữu cơ X (chứa C, H, O) có tỉ khối hơi so với H2 bằng 30?
A. 1 B. 3
C. 2 D. 4
Lời giải
Tỉ khối hơi so với H2 bằng 30 => M = 30.2 = 60
Gọi CTPT của X có dạng CxHyOz
=> M = 12x + y + 16z = 60 (1)
=> 16z < 60 => z < 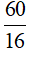 < 3,75
< 3,75
TH1: z = 1, thay vào (1) => 12x + y = 44 (2)
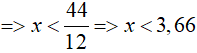
+) x = 1, thay vào (2) => y = 44 – 12 = 32 (loại)
+) x = 2, thay vào (2) => y = 44 – 12.2 = 20 (loại)
+) x = 3, thay vào (2) => y = 8 (thỏa mãn X là C3H8O)
TH2: z = 2, thay vào (1) => 12x + y = 28 (3)
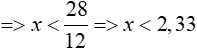
+) x = 1 => y = 28 – 12 = 16 (loại)
+) x = 2 => y = 28 – 12.2 = 4 (thỏa mãn X là C2H4O2)
TH3: z = 3, thay vào (1) => 12x + y = 12 => loại vì x và y đều ≥ 1
Vậy có 2 CTPT thỏa mãn đầu bài
Đáp án: C

Bài 6: Axit axetic có công thức là C2H4O2. Phần trăm nguyên tố C trong phân tử axit axetic là
A. 30%. B. 40%.
C. 50%. D. 60%
Lời giải
Khối lượng mol của C2H4O2 là:
MC2H4O2 = 12.2 + 4 + 16.2 = 60
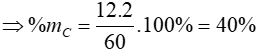
Đáp án: B
Bài 7: Công thức đơn giản nhất của hợp chất hữu cơ A là CH2Cl. Biết MA = 99. CTPT của A là
A. CH2Cl2
B. C2H4Cl2
C. CHCl3
D. C2H2Cl3
Lời giải
+) CTĐGN là CH2Cl => CTPT: (CH2Cl)n
+) Vì MA = 99 => (12 + 2 + 35,5).n = 99 => n = 2
=> CTPT: C2H4Cl2
Đáp án: B
Bài 8: Hợp chất hữu cơ A gồm 3 nguyên tố C, H, O trong đó %mC = 48,65% và %mH = 8,11%. Biết khối lượng mol phân tử của A là 74. Xác định CTPT của A
A. C2H4O2
B. C2H4O
C. C3H6O
D. C3H6O2
Lời giải
Gọi công thức đơn giản nhất là CxHyOz
%mO = 100% - %mC - %mH = 43,24%
Ta có:
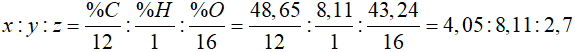
=> x : y : z = 1,5 : 3 : 1 = 3 : 6 : 2
=> CTĐGN của A là C3H6O2
=> CTPT của A dạng (C3H6O2)n
MA = 74 = (12.3 + 6 + 16.2).n => n = 1
=> CTPT: C3H6O2
Đáp án: D
Bài 9: Một hợp chất X chứa 3 nguyên tố C, H, O có tỉ lệ khối lượng mC : mH : mO = 21 : 2 : 4. Hợp chất X có công thức đơn giản nhất trùng với CTPT. CTPT X là:
A. C7H8O
B. C8H10O
C. C6H6O2
D. C7H8O2.
Lời giải
Gọi CTPT của X là CxHyOz
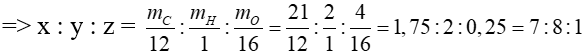
=> CTPT của X là C7H8O (vì CTPT trùng với CTĐGN)
Đáp án: A
Bài 10: Hiđrocacbon X có 83,33% khối lượng Cacbon. Số đồng phân cấu tạo của X là:
A. 4 B. 3
C. 2 D. 1
Lời giải
X là hiđrocacbon => X chỉ chứa C và H
Gọi CTPT của X có dạng CxHy (y ≤ 2x + 2)
=> %mH = 100% - %mC = 100% - 83,33% = 16,67%
=> x : y = 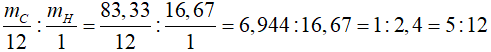
=> CTPT của X có dạng: (C5H12)n hay C5nH12n
Vì y ≤ 2x + 2 => 12n ≤ 5n + 7 => n ≤ 1 => n = 1
=> CTPT của X là C5H12
Ta có: ∆ = 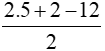 = 0 => C5H12 là hiđrocacbon no, mạch hở
= 0 => C5H12 là hiđrocacbon no, mạch hở
Các CTCT của X là:

Đáp án: B


