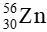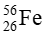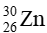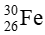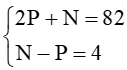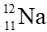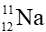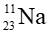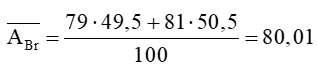Trắc nghiệm Hóa 10 Bài 3: Nguyên tố hóa học
Bộ 15 bài tập trắc nghiệm Hóa 10 Bài 3: Nguyên tố hóa học có đáp án đầy đủ gồm các câu hỏi trắc nghiệm đầy đủ các mức độ nhận biết, thông hiểu, vận dụng, vận dung cao sách Chân trời sáng tạo giúp học sinh ôn luyện trắc nghiệm Hóa 10 Bài 3.
Trắc nghiệm Hóa 10 Bài 3: Nguyên tố hóa học - Chân trời sáng tạo
Câu 1. Tổng số hạt trong nguyên tử nguyên tố X là 82. Trong hạt nhân, số hạt mang điện ít hơn số hạt không mang điện là 4. Kí hiệu nguyên tử X là:
(Cho số hiệu nguyên tử của Cr = 24; Mn = 25; Fe = 26; Zn = 30)
A.
B.
C.
D.
Đáp án: B
Giải thích:
Gọi số hạt proton, neutron, electron trong một nguyên tử X lần lượt là P, N, E.
Ta có: P = E
Tổng số hạt trong nguyên tử X là: P + N + E = 2P + N = 82 (1)
Số hạt mang điện trong hạt nhân nguyên tử là: P
Số hạt không mang điện trong hạt nhân nguyên tử là: N
Trong hạt nhân, số hạt mang điện ít hơn số hạt không mang điện là 4 nên N – P = 4 (2)
Từ (1) và (2) ta có hệ phương trình:
Giải hệ phương trình ta được P = 26; N = 30
Vì số hiệu nguyên tử Z = số p ⇒ Z = 26
⇒ X có kí hiệu hóa học là Fe.
Số khối: A = P + N = 26 + 30 = 56
Kí hiệu nguyên tử của X là
Câu 2. Công thức tính số khối (A) là
A. Số khối (A) = số proton (P) + số electron (E)
B. Số khối (A) = số neutron (N) + số electron (E)
C. Số khối (A) = số proton (P) × 2
D. Số khối (A) = số proton (P) + số neutron (N)
Đáp án: D
Giải thích:
Câu 3. Nguyên tử potassium (K) có 19 electron; 19 proton và 20 neutron. Số khối nguyên tử của K là
A. 20
B. 19
C. 39
D. 58
Đáp án: C
Giải thích:
Câu 4. Số hiệu nguyên tử của một nguyên tố là
A. điện tích hạt nhân nguyên tử của nguyên tố đó
B. số đơn vị điện tích hạt nhân nguyên tử của nguyên tố đó
C. tổng số proton và neutron trong nguyên tử của nguyên tố đó
D. tổng số proton và electron trong nguyên tử của nguyên tố đó
Đáp án: B
Giải thích:
Câu 5. Khẳng định đúng là
A. Số đơn vị điện tích hạt nhân (Z) = số proton (P) = số electron (E)
B. Số đơn vị điện tích hạt nhân (+Z) = số proton (P) = số electron (E)
C. Số đơn vị điện tích hạt nhân (Z) = số proton (P) = số neutron (N)
D. Số đơn vị điện tích hạt nhân (Z) = số neutron (N) = số electron (E)
Đáp án: A
Giải thích:
Số đơn vị điện tích hạt nhân (Z) = số proton (P) = số electron (E).
Điện tích hạt nhân = + Z.
Câu 6. Nguyên tử nitơ (nitrogen) có 7 proton. Số đơn vị điện tích hạt nhân của nguyên tử này là
A. + 7
B. 7
C. + 14
D. 14
Đáp án: B
Giải thích:
Câu 7. Nguyên tố hóa học là
A. tập hợp các nguyên tử có cùng số hạt neutron;
B. tập hợp các nguyên tử có cùng điện tích hạt nhân;
C. tập hợp các nguyên tử có cùng số hạt neutron và proton;
D. tập hợp các nguyên tử có cùng số số khối A.
Đáp án: B
Giải thích:
Câu 8. Kí hiệu nguyên tử 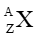
A. kí hiệu hóa học của nguyên tố (X);
B. số hiệu nguyên tử (Z);
C. số khối (A);
D. Cả A, B và C đều đúng.
Đáp án: D
Giải thích:
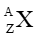 cho biết kí hiệu hóa học của nguyên tố (X); số hiệu nguyên tử (Z); số khối (A).
cho biết kí hiệu hóa học của nguyên tố (X); số hiệu nguyên tử (Z); số khối (A).Câu 9. Một nguyên tử sodium (Na) có 11 electron; 11 proton và 12 neutron. Kí hiệu của nguyên tử này là
A.
B.
C.
D.
Đáp án: C
Giải thích:
Một nguyên tử sodium (Na) có:
- Số hiệu nguyên tử Z = số đơn vị điện tích hạt nhân = số p = 11
- Số khối A = P + N = số p + số n = 11 + 12 = 23
Kí hiệu nguyên tử là 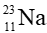
Câu 10. Cho kí hiệu nguyên tử 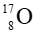
A. Kí hiệu hóa học của nguyên tố là O;
B. Số hiệu nguyên tử là 8;
C. Số proton trong một hạt nhân nguyên tử là 8;
D. Số neutron trong một hạt nhân nguyên tử là 8.
Đáp án: B
Giải thích:
Kí hiệu nguyên tử 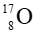
- Kí hiệu hóa học của nguyên tố là O;
- Số hiệu nguyên tử Z = 8 ⇒ số proton (P) là 8.
- Số khối A = 17 mà A = P + N ⇒ N = A – P = 17 – 8 = 9 ⇒ số neutron là 9.
Vậy khẳng định: Số neutron trong một hạt nhân nguyên tử là 8 là khẳng định sai.
Câu 11. Cho nguyên tử iron (Fe) có kí hiệu nguyên tử là 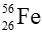
A. 26; 26; 56
B. 26; 26; 30
C. 30; 30; 26
D. 30; 26; 26
Đáp án: B
Giải thích:
Kí hiệu nguyên tử là
Ta có: số e = số p = Z = 26
Số n = N = A – P = 56 – 26 = 30
Vậy số e, p, n lần lượt là: 26; 26; 30
Câu 12. Nguyên tử aluminium có 13 electron. Điện tích hạt nhân của nguyên tử này là
A. 13
B. 27
C. + 13
D. + 27
Đáp án: C
Giải thích:
Số đơn vị điện tích hạt nhân (Z) = số electron (E) = 13.
Điện tích hạt nhân = + Z = + 13.
Câu 13. Nguyên tố bromine có 2 đồng vị 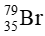
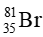
A. 79,5;
B. 79,1;
C. 80,01;
D. 35.
Đáp án: C
Giải thích:
Thành phần phần trăm về số lượng nguyên tử của đồng vị 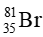
100% − 49,5% = 50,5%
Nguyên tử khối trung bình của bromine là:
Câu 14. Lithium có 2 đồng vị là 7Li và 6Li. Nguyên tử khối trung bình của Li là 6,93. Phần trăm số nguyên tử của đồng vị 7Li là:
A. 93%;
B. 7%;
C. 78%;
D. 22%.
Đáp án: A
Giải thích:
Gọi phần trăm số nguyên tử của đồng vị 7Li là x%
⇒ phần trăm số nguyên tử của đồng vị 6Li là (100 − x)%
Ta có: 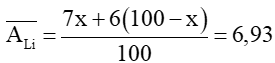
Phần trăm số nguyên tử của đồng vị 7Li là 93%.
Câu 15. Nguyên tử của nguyên tố magnesium (Mg) có 12 proton và 12 neutron. Nguyên tử khối của Mg là
A. 12 amu
B. 24 amu
C. 36 amu
D. 6 amu
Đáp án: B
Giải thích:
Do khối lượng của các electron rất nhỏ không đáng kể nên có thể coi nguyên tử khối có giá trị bằng số khối.
Do đó, nguyên tử khối của Mg = AMg = P + N = 12 + 12 = 24 (amu).
Các câu hỏi trắc nghiệm Hóa 10 sách Chân trời sáng tạo có đáp án, chọn lọc khác: