Sách bài tập Hóa học 10 Bài 15 Chân trời sáng tạo: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
Với giải sách bài tập Hóa học 10 Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng sách Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập trong SBT Hóa học 10 Bài 15.
Giải sách bài tập Hóa học lớp 10 Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng - Chân trời sáng tạo
Bài 15.1 trang 63 SBT Hóa học 10. Cho phương trình hóa học:
2KMnO4(aq) + 10FeSO4(aq) + 8H2SO4 (aq) → 5Fe2(SO4)3 (aq) + K2SO4 (aq) + 2MnSO4 (aq) + 8H2O (l)
Với cùng một lượng các chất tham gia phản ứng, chất phản ứng hết nhanh nhất là:
Lời giải:
Đáp án đúng là: B.
Giả sử khối lượng KMnO4; FeSO4; H2SO4 tham gia phản ứng bằng nhau và bằng 100 gam.
Ta có:
2KMnO4(aq) + 10FeSO4(aq) + 8H2SO4 (aq) → ….
………………..…….. mol
Tiếp tục lấy số mol từng chất chia cho hệ số trong phản ứng của chất đó, thấy:
là nhỏ nhất, vậy FeSO4 hết trước.
Bài 15.2 trang 63 SBT Hóa học 10. Đối với phản ứng: , phát biểu nào sau đây đúng?
A. Tốc độ tiêu hao chất B bằng 3/2 tốc độ tạo thành chất C.
B. Tốc độ tiêu hao chất B bằng 2/3 tốc độ tạo thành chất C.
C. Tốc độ tiêu hao chất B bằng 3 tốc độ tạo thành chất C.
D. Tốc độ tiêu hao chất B bằng 1/3 tốc độ tạo thành chất C.
Lời giải:
Đáp án đúng là: A.
Dựa vào tỉ lệ các chất trong phản ứng xác định được: Tốc độ tiêu hao chất B bằng 3/2 tốc độ tạo thành chất C.
Lời giải:
Đáp án đúng là: C.
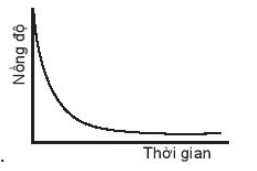
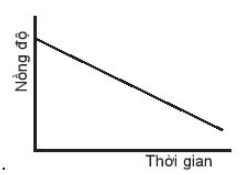
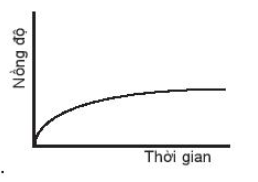
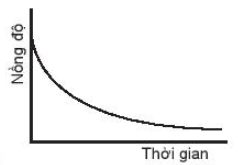
Nồng độ chất tham gia giảm dần theo thời gian.
Vậy biểu đồ nào C không biểu diễn sự phụ thuộc nồng độ chất tham gia với thời gian.
A. Đường cong số (1)
B. Đường cong số (2)
C. Đường cong số (3)
D. Đường cong số (2) hoặc 3 đều đúng
Lời giải:
Đáp án đúng là: C.
Đường cong (1) là của nước do nồng độ tăng dần theo thời gian.
Trong hai đường cong (2) và (3) đường cong (3) là của hydrogen do nồng độ giảm theo thời gian và dựa vào tỉ lệ phản ứng thấy nồng độ hydrogen giảm nhiều hơn so với nồng độ oxygen.
Lời giải:
Đáp án đúng là: D.
Tốc độ phản ứng của H2 là:
Lời giải:
Đáp án đúng là: D.
Theo định luật tác dụng khối lượng, tốc độ phản ứng được viết dưới dạng:
Khi nồng độ của CHCl3 giảm 4 lần, nồng độ Cl2 giữ nguyên ta có:
Vậy khi nồng độ của CHCl3 giảm 4 lần, nồng độ Cl2 giữ nguyên thì tốc độ phản ứng sẽ giảm 4 lần.
Bài 15.7 trang 64 SBT Hóa học 10. Cho phương trình hóa học của phản ứng:
Lời giải:
Biểu thức tốc độ của phản ứng là:
.
Khi nồng độ CO tăng 2 lần, ta có:
, vậy tốc độ phản ứng tăng 2 lần.
Lời giải:
Theo phương trình hoá học, vì bỏ qua sự thay đổi thể tích dung dịch sau phản ứng:
Tốc độ trung bình của phản ứng tính theo MgCl2 trong 40 giây là:
Vậy, tốc độ trung bình của phản ứng tính theo HCl và MgCl2 là bằng nhau.
a. Tính tốc độ trung bình của mỗi phản ứng.
b. Phản ứng nào diễn ra với tốc độ nhanh nhất? Phản ứng nào diễn ra với tốc độ chậm nhất?
Lời giải:
a) Tốc độ trung bình của mỗi phản ứng
|
Phản ứng |
Lượng chất phản ứng (mol) |
Thời gian (s) |
Tốc độ phản ứng (mol/s) |
|
1 |
2 |
30 |
0,067 |
|
2 |
5 |
120 |
0,042 |
|
3 |
1 |
90 |
0,011 |
|
4 |
3,2 |
90 |
0,036 |
|
5 |
5,9 |
30 |
0,197 |
b) Phản ứng 5 xảy ra với tốc độ nhanh nhất và phản ứng 3 xảy ra với tốc độ chậm nhất.
Sau 1 phút, khối lượng MgCl2 được tạo ra 2 gam.
a. Tính tốc độ trung bình (mol/s) của phản ứng (1).
Lời giải:
a) Tính tốc độ trung bình (mol/s) của phản ứng (1):
(mol/s)
b) Tốc độ trung bình của phản ứng (2) tương đương (1), thì khối lượng NaCl là:
Bài 15.11 trang 65 SBT Hóa học 10. Cho phản ứng tert – butyl chloride (tert-C4H9Cl) với nước:
Lời giải:
Công thức tính tốc độ phản ứng theo chất tham gia:
Tốc độ phản ứng sau 4s theo tert-butyl chloride:
(M/s)
Lời giải:
Biểu thức tốc độ phản ứng:
Theo kết quả thực nghiệm 1:
Từ thực nghiệm 2, tính được nồng độ chất A, từ thực nghiệm 3, tính được nồng độ chất B:
Bài 15.13 trang 66 SBT Hóa học 10. Xét phản ứng phân hủy khí N2O5 xảy ra như sau:
Lời giải:
Phản ứng phân huỷ khí N2O5, xảy ra như sau:
a) Biểu thức tính tốc độ trung bình của phản ứng là:
b) Theo hệ số cân bằng của phương trình, ta có
- Tốc độ tạo thành NO2 = 4 lần tốc độ tạo thành
O2 = 9,0 × 10-6 × 4= 3,6 × 10-5 (M/s).
- Tốc độ phân huỷ = 2 lần tốc độ tạo thành
O2 = 9,0 × 10-6 × 2= 1,8 × 10-5 (M/s).
|
Thời gian (s) |
SO2 (M) |
O2 (M) |
SO3 (M) |
|
300 |
0,0270 |
0,0500 |
0,0072 |
|
720 |
0,0194 |
0,0462 |
0,0148 |
Tính tốc độ trung bình của phản ứng trong khoảng thời gian trên.
Lời giải:
Phương trình hoá học của phản ứng:
Tốc độ trung bình của phản ứng được tính trong khoảng thời gian t1 = 300 (s)
đến
Tốc độ trung bình của phản ứng: