Vận dụng quy tắc octet để giải thích sự hình thành liên kết trong các phân tử F2, CCl4
Lời giải câu hỏi 3 trang 50 Hóa học 10 sách Kết nối tri thức hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập Hóa học 10.
Giải Hóa học 10 Kết nối tri thức Bài 10: Quy tắc octet
Câu hỏi 3 trang 50 Hóa học 10: Vận dụng quy tắc octet để giải thích sự hình thành liên kết trong các phân tử F2, CCl4 và NF3.
Lời giải:
- Sự hình thành liên kết trong phân tử F2
Khi hình thành liên kết hóa học trong phân tử F2, nguyên tử fluorine có 7 electron hóa trị, mỗi nguyên tử fluorine cần thêm 1 electron để đạt cấu hình electron bão hòa theo quy tắc octet nên mỗi nguyên tử fluorine góp chung 1 electron.
Phân tử Fe được biểu diễn 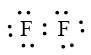
Xung quanh mỗi nguyên tử fluorine đều có 8 electron.
- Sự hình thành liên kết hóa học trong phân tử CCl4
Nguyên tử C có 4 electron hóa trị, nguyên tử Cl có 7 electron hóa trị. Mỗi nguyên tử Cl cần thêm 1 electron và nguyên tử C cần thêm 4 electron để đạt cấu hình electron bão hòa theo quy tắc octet.
Phân tử CCl4 được biểu diễn 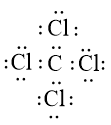
Xung quanh mỗi nguyên tử C và Cl đều có 8 electron.
- Sự hình thành liên kết hóa học trong phân tử NF3
Nguyên tử N có 5 electron hóa trị, nguyên tử F có 7 electron hóa trị. Mỗi nguyên tử F cần thêm 1 electron và nguyên tử N cần thêm 3 electron để đạt cấu hình electron bão hòa theo quy tắc octet.
Phân tử NF3 được biểu diễn 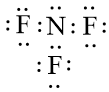
Xung quanh mỗi nguyên tử N và F đều có 8 electron.
Xem thêm các bài giải sách giáo khoa Hóa học 10 bộ sách Kết nối tri thức hay, chi tiết khác:


