Giải Hoá 10 (Kết nối tri thức) Bài 18: Ôn tập chương 5
Hoidap.vietjack.com trân trọng giới thiệu: lời giải bài tập Hoá lớp 10 Bài 18: Ôn tập chương 5 sách Kết nối tri thức hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hoá 10 Bài 18. Mời các bạn đón xem:
Giải bài tập Hóa lớp 10 Bài 18: Ôn tập chương 5
I. Hệ thống hóa kiến thức
Hệ thống hóa kiến thức trang 89 Hóa học 10: Hoàn thành các nội dung còn thiếu sau đây:
Chất phản ứng ⟶ Sản phẩm, > 0 (phản ứng …?... nhiệt)
Tính biến thiên enthalpy của phản ứng theo nhiệt tạo thành (ở điều kiện chuẩn):
Lời giải:
Chất phản ứng ⟶ Sản phẩm, > 0 (phản ứng thu nhiệt)
< 0 (phản ứng tỏa nhiệt)
Tính biến thiên enthalpy của phản ứng theo nhiệt tạo thành (ở điều kiện chuẩn):
Tính biến thiên enthalpy của phản ứng (mà các chất đều ở thể khí) theo năng lượng liên kết (ở điều kiện chuẩn):
II. Luyện tập
A. thu nhiệt, P đỏ bền hơn P trắng.
B. thu nhiệt, P trắng bền hơn P đỏ.
C. toả nhiệt, P đỏ bền hơn P trắng.
D. toả nhiệt, P trắng bền hơn P đỏ.
Lời giải:
Đáp án đúng là: A
> 0 ⇒ Phản ứng thu nhiệt.
= (P, trắng) - (P, đỏ) > 0
⇒ (P, trắng) > (P, đỏ)
⇒ P trắng có mức năng lượng cao hơn tức là kém bền hơn P đỏ.
Câu hỏi 2 trang 89 Hóa học 10: Cho biết biến thiên enthalpy của phản ứng sau ở điều kiện chuẩn:
CO (g) + O2 (g) ⟶ CO2 (g) = -283,0 kJ
Biết nhiệt tạo thành chuẩn của CO2: (CO2 (g)) = –393,5 kJ/mol.
Nhiệt tạo thành chuẩn của CO là
Lời giải:
Đáp án đúng là: A
= (CO2(g)).1 – [(CO(g)) + (O2(g)).]
⇒ - 283 = - 393,5.1 – [(CO(g)) + 0. ]
⇒ (CO(g)) = - 110,5 kJ
Lời giải:
Đáp án đúng là: A
Khối lượng của glucose trong 500 mL dung dịch glucose 5% là
mglucose = = 25,5 gam
Oxi hóa 180 gam (1mol) glucose toả ra nhiệt lượng là 2 803,0 kJ.
⇒ Oxi hóa 25,5 gam glucose toả ra nhiệt lượng là kJ
Vậy năng lượng tối đa từ phản ứng oxi hóa hoàn toàn glucose mà bệnh nhân đó có thể nhận được là +397,09 kJ.
Câu hỏi 4 trang 90 Hóa học 10: Cho giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:
Biến thiên enthalpy của phản ứng C3H8(g) ⟶ CH4(g) + C2H4(g) có giá trị là
Lời giải:
Đáp án đúng là: C
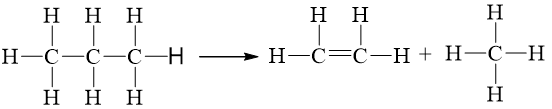
2.Eb(C – C) + 8.Eb(C – H) = 2.346 + 8.418 = 4036 kJ
1.Eb(C = C) + 8.Eb(C – H) = 1.612 + 8.418 = 3956 kJ
⇒ = 4036 – 3956 = +80 kJ
CH4(g) + 2O2(g) ⟶ CO2(g) + 2H2O(l) = – 890,3 kJ
Lời giải:
= -
⇒ – 890,3 = [(– 393,5) + (– 285,8.2)] – [ + 0.2]
⇒ = – 74,8 kJ/mol
C2H5OH(l) + 3O2(g) ⟶ 2CO2(g) + 3H2O(l) = – 1 365 kJ
C57H110O6(s) + O2(g) ⟶ 57 CO2(g) + 55H2O(l) = – 35 807 kJ
Lời giải:
Đốt cháy 46 gam (1mol) C2H5OH tỏa ra lượng nhiệt là 1 365 kJ
⇒ Đốt cháy 1000 gam (1 kg) C2H5OH tỏa ra lượng nhiệt là kJ.
Đốt cháy 890 gam (1mol) C57H110O6 tỏa ra lượng nhiệt là 35 807 kJ.
⇒ Đốt cháy 1000 gam (1kg) C57H110O6 tỏa ra lượng nhiệt là kJ.
So sánh:
Nhiệt tỏa ra khi đốt cháy hoàn toàn 1 kg tristearin có trong mỡ lợn > khi đốt cháy hoàn toàn 1 kg cồn.
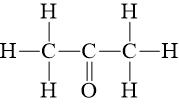
Câu hỏi 7 trang 90 Hóa học 10: Biết CH3COCH3 có công thức cấu tạo:
CH3COCH3(g) + 4O2(g) ⟶ 3CO2(g) + 3H2O(g)
Lời giải:
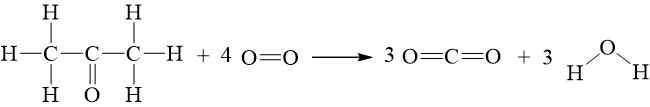
2.Eb(C – C) + 6.Eb(C – H) + 1.Eb(C = O) + 4.Eb(O = O)
= 2.346 + 6.418 + 1.732 + 4. 494 = 5908 kJ
6.Eb(C = O) + 6.Eb(O – H) = 6.732 + 6.459 = 7146 kJ
⇒ = 5908 – 7146 = - 1238 kJ
C3H8(g) + 5O2(g) ⟶ 3CO2(g) + 4H2O(1) = –2 220 kJ
C4H10(g) + O2(g) ⟶ 4CO2(g) + 5H2O (1) = –2 874 kJ
Lời giải:
Gọi x là số mol của propane trong bình gas.
⇒ 2x là số mol của butane trong bình gas.
Khối lượng 12 kg khí gas bằng 44x + 58.2x = 12.1000 (gam) ⇒ x = 75 (mol)
1 mol propane cháy tỏa ra 2 220 kJ nhiệt lượng.
1 mol butane cháy tỏa ra 2 874 kJ nhiệt lượng.
Tổng nhiệt lượng tỏa ra khi đốt cháy hoàn toàn một bình gas 12kg là:
75.2220 + 2.75.2874 = 597600 kJ
Số ngày mà hộ gia đình sử dụng hết bình gas là
≈ 48 ngày