Giải Hoá 10 (Kết nối tri thức) Bài 1: Thành phần của nguyên tử
Hoidap.vietjack.com trân trọng giới thiệu: lời giải bài tập Hoálớp 10 Bài 1: Thành phần của nguyên tử sách Kết nối tri thức hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hoá 10 Bài 1. Mời các bạn đón xem:
Giải bài tập Hóa lớp 10 Bài 1: Thành phần của nguyên tử
Video giải bài tập Hóa lớp 10 Bài 1: Thành phần của nguyên tử
Lời giải:
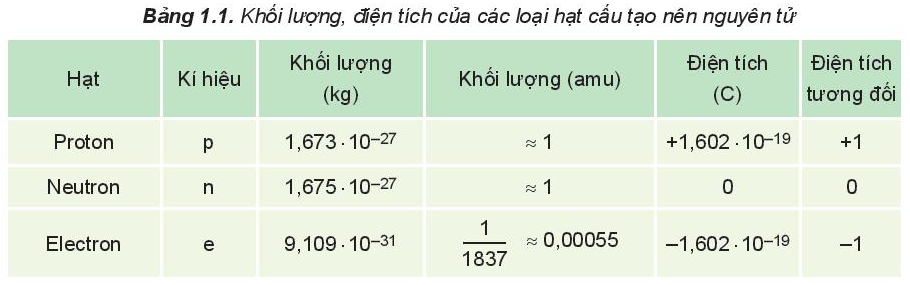
Nguyên tử gồm hạt nhân ở tâm (chứa proton mang điện tích dương và neutron không mang điện) và vỏ nguyên tử (chứa các electron mang điện tích âm)
- Lịch sử phát hiện ra hạt electron:
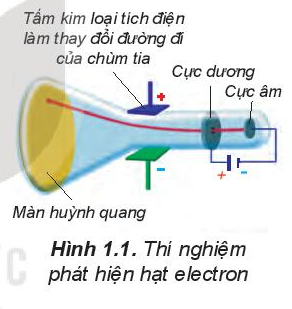
Năm 1897, J.J. Thomson (Tôm-xơn, người Anh) thực hiện thí nghiệm phóng điện qua không khí loãng đã phát hiện ra chùm tia phát ra từ cực âm và bị hút lệch về phía cực dương của điện trường, chứng tỏ chúng mang điện tích âm. Đó chính là chùm các hạt electron.
- Lịch sử phát hiện ra hạt nhân nguyên tử và hạt proton:
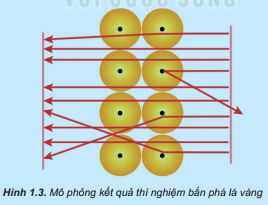
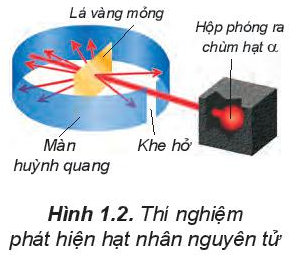
Năm 1911, E. Rutherford (Rơ-dơ-pho, người Niu Di-lân) thực hiện thí nghiệm bắn phá lá vàng rất mỏng bằng chùm hạt α (alpha). Ông sử dụng màn huỳnh quang bao quanh lá vàng để quan sát vị trí va chạm của hạt α. Kết quả thí nghiệm cho thấy hầu hết các hạt α đều xuyên thẳng qua lá vàng. Chứng tỏ nguyên tử có cấu tạo rỗng, ở tâm chứa một hạt nhân mang điện tích dương và có kích thước rất nhỏ so với kích thước nguyên tử.
Năng 1918, E Rutherford và các cộng sự khi dùng hạt α bắn phá nitrogen đã phát hiện ra hạt proton.
- Lịch sử phát hiện ra hạt neutron:
Năm 1932, J.Chadwick (chat-uých, người Anh), cộng sự của Rutherford, đã phát hiện ra hạt neutron khi bắn phá beryllium bằng các hạt α.
I. Các loại hạt cấu tạo nên nguyên tử
Câu hỏi 1 trang 14 Hóa học 10: Nguyên tử chứa những hạt mang điện là
Lời giải:
Đáp án đúng là: C
Hạt proton mang điện tích dương, hạt electron mang điện tích âm.
Hạt neutron không mang điện.
Lời giải:
Nhận xét về đường đi của các hạt α:
+ Hầu hết các hạt α đều xuyên thẳng qua lá vàng một số ít hạt đi lệch hướng ban đầu và một số rất ít hạt bị bật lại phía sau khi gặp lá vàng.
+ Chứng tỏ nguyên tử có cấu tạo rỗng, ở tâm có một hạt nhân có kích thước rất nhỏ so với nguyên tử. Hạt nhân nguyên tử mang điện tích dương và có khối lượng lớn.
II. Kích thước và khối lượng của nguyên tử
Lời giải:
Ta có tỉ lệ:
⇒ Kích thước của nguyên tử vàng lớn hơn gấp khoảng 10000 lần hạt nhân của nó.
a) Khối lượng hạt nhân với khối lượng nguyên tử.
b) Khối lượng hạt nhân với khối lượng vỏ nguyên tử.
Lời giải:
a) Khối lượng của hạt nhân nitrogen là
= 7.1,673.10-27 + 7.1,675.10-27 = 2,3436.10-26 (kg)
Nguyên tử trung hòa về điện ⇒ số hạt electron = số hạt proton = 7
Khối lượng nguyên tử nitrogen là
= 2,3436.10-26 + 7.9,109.10-31 = 2,3442.10-26 (kg)
⇒ mhn ≈ mnt
b) Khối lượng của vỏ nguyên tử nitrogen là
me = 7.9,109.10-31 = 6,3763.10-30 (kg)
⇒ mhn ≫ me (khối lượng hạt nhân lớn hơn rất nhiều so với khối lượng vỏ nguyên tử).
III. Điện tích hạt nhân và số khối
Lời giải:
Hạt nhân của nguyên tử aluminium có điện tích bằng +13.
⇒ Số đơn vị điện tích hạt nhân (Z) = 13 = số proton = số electron.
Ta có:
Số khối A = số proton + số neutron
⇔ 27 = 13 + số neutron
⇔ Số neutron = 14
Em có thể trang 16 Hóa học 10: Vận dụng phương pháp mô hình để mô tả cấu tạo nguyên tử.
Lời giải:
Ví dụ: Mô hình nguyên tử Li như sau:
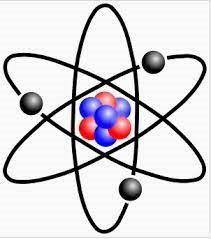
Với quả cầu màu đen là hạt electron, quả cầu màu xanh là hạt neutron, quả cầu màu đỏ là hạt proton.
Từ mô hình nguyên tử Li xác định được thành phần cấu tạo của nguyên tử Li:
+ Lớp vỏ gồm 3 electron.
+ Hạt nhân gồm 3 proton và 4 neutron.