Giải Hoá 10 (Chân trời sáng tạo) Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA
Hoidap.vietjack.com trân trọng giới thiệu: lời giải bài tập Hoá lớp 10 Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA sách Chân trời sáng tạo hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hoá 10 Bài 17. Mời các bạn đón xem:
Giải bài tập Hóa lớp 10 Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA
Nhóm halogen gồm những nguyên tố nào? Halogen có những tính chất và ứng dụng trong lĩnh vực nào?
Lời giải:
- Nhóm halogen gồm: fluorine (F), chlorine (Cl), bromine (Br), iodine (I), astatine (At), tennessine (Ts).
- Tính chất vật lí của các nguyên tố halogen:
+ Các halogen ít tan trong nước, tan nhiều trong dung môi hữu cơ không phân cực như hexane (C6H14), carbon tetrachloride (CCl4), …
Từ fluorine đến iodine:
+ Trạng thái tập hợp của đơn chất ở 20oC thay đổi: fluorine và chlorine ở thể khí, bromine ở thể lỏng, iodine ở thể rắn.
+ Màu sắc đậm dần: fluorine có màu lục nhạt, chlorine có màu vàng lục, bromine có màu nâu đỏ, iodine có màu đen tím.
+ Nhiệt độ nóng chảy và nhiệt độ sôi tăng dần.
- Tính chất hóa học: Tính chất hóa học đặc trưng của halogen là tính oxi hóa mạnh, tính oxi hóa giảm dần từ fluorine đến iodine.
- Ứng dụng: Các halogen có ứng dụng rất quan trọng trong đời sống và sản xuất. Ví dụ:
+ Fluorine: được sử dụng trong sản xuất các chất dẻo ma sát thấp; một số hợp chất của fluorine được sử dụng trong sản xuất nhôm, thuốc trừ sâu, kem đánh răng …
+ Chlorine: được sử dụng làm chất tẩy trắng và khử trùng nước; một lượng lớn chlorine được dùng để sản xuất các dung môi.
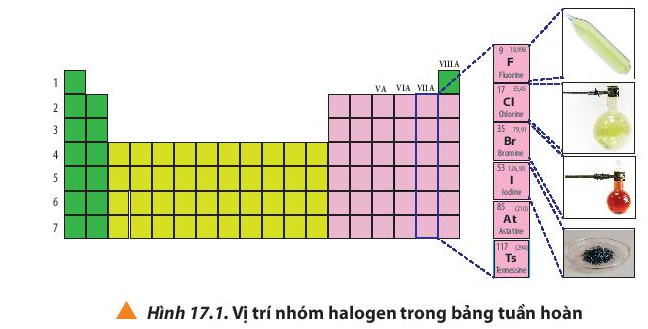
1. Vị trí của nhóm halogen trong bảng tuần hoàn
Lời giải:
Nhóm halogen thuộc nhóm VIIA trong bảng tuần hoàn các nguyên tố hóa học.
2. Trạng thái tự nhiên của các halogen
Câu hỏi 2 trang 106 Hóa học 10: Hãy kể tên một số chất chứa nguyên tố halogen
Lời giải:
Một số chất chứa nguyên tố halogen:
- Fluorite: CaF2
- Fluorapatite: Ca5(PO4)3F
- Cryolite: Na3AlF6
- Quặng halite: NaCl (thường gọi là muối mỏ)
- Sylvite: KCl
- Quặng bromargyrite: AgBr
- Iodargyrite: AgI
Lời giải:
Halogen trong tự nhiên chỉ tồn tại ở dạng hợp chất, chủ yếu tồn tại dưới dạng muối của các ion halide (F-, Cl-, Br-, I-)
Lời giải:
Cứ mỗi lít nước biển chứa khoảng 35 gam muối, phần lớn là sodium chloride (NaCl).
Khoảng 71% bề mặt Trái Đất được bao phủ bởi biển và đại dương ⇒ hàm lượng nguyên tố chlorine có nhiều nhất trong tự nhiên.
3. Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố halogen. Đặc điểm cấu tạo phân tử halogen.
Lời giải:
Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố halogen có dạng: ns2np5
Cụ thể cấu hình electron lớp ngoài cùng:
+ F: 2s22p5
+ Cl: 3s23p5
+ Br: 4s24p5
+ I: 5s25p5
Lời giải:
Do có 7 electron ở lớp ngoài cùng, chưa đạt cấu hình bền vững như khí hiếm, nên ở trạng thái tự do, hai nguyên tử halogen góp chung một cặp electron để hình thành phân tử halogen.
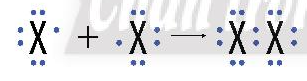
Với X là kí hiệu các nguyên tố halogen.
Công thức cấu tạo của phân tử halogen: X-X
4. Tính chất vật lí của các halogen
Lời giải:
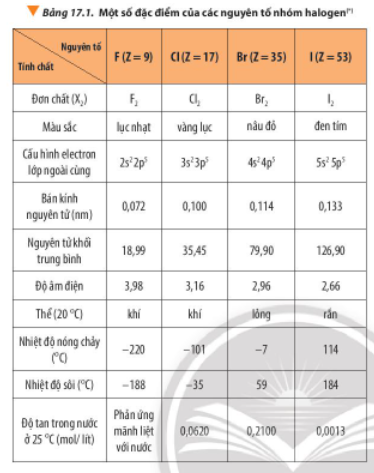
Theo chiều tăng dần của điện tích hạt nhân nguyên tử (từ F2 đến I2)
- Màu sắc của các đơn chất halogen đậm dần.
- Trạng thái ở điều kiện thường: Từ thể khí chuyển sang thể lỏng và thể rắn.
- Nhiệt độ nóng chảy và nhiệt độ sôi tăng dần.
Lời giải:
Nhiệt độ nóng chảy và nhiệt độ sôi của đơn chất halogen bị ảnh hưởng bởi tương tác van der Waals giữa các phân tử. Từ fluorine đến iodine, khối lượng phân tử và bán kính nguyên tử tăng, làm tăng tương tác van der Waals, dẫn đến nhiệt độ nóng chảy và nhiệt độ sôi tăng.
Lời giải:
Dựa vào quy luật biến đối trạng thái của các nguyên tố halogen theo chiều tăng dần điện tích hạt nhân: Từ thể khí chuyển sang thể lỏng và thể rắn. Ta có thể dự đoán astatine tồn tại ở thể rắn.
5. Tính chất hóa học của các halogen
Lời giải:
Halogen có cấu hình electron lớp ngoài cùng là ns2np5, nên nguyên tử có xu hướng nhận thêm 1 electron hoặc dùng chung electron với nguyên tử khác để đạt cấu hình electron bền vững của khí hiếm tương ứng.
Sơ đồ tổng quát: X + 1e → X-
Lời giải:
Trong phản ứng với kim loại số oxi hóa của nguyên tử các nguyên tố halogen giảm. Mỗi nguyên tử halogen từ số oxi hóa 0 sẽ nhận thêm 1 electron thành số oxi hóa -1.
Các quá trình khử xảy ra:
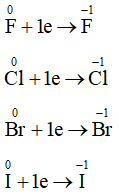
Lời giải:
Theo chiều từ F2 đến I2 khả năng phản ứng với H2 giảm dần.
Do năng lượng liên kết của phân tử H-X giảm dần hay độ bền của phân tử HX giảm dần.
Phương trình minh họa:
Lời giải:
Phản ứng của chlorine với dung dịch kiềm:
Trong phản ứng với dung dịch kiềm ở hai điều kiện nhiệt độ khác nhau, số oxi hóa của chlorine vừa tăng, vừa giảm sau phản ứng.
⇒ Phản ứng này thuộc loại phản ứng oxi hóa – khử.
Câu hỏi 12 trang 111 Hóa học 10: Tiến hành thí nghiệm 1, quan sát và ghi nhận hiện tượng.
Thí nghiệm 1: So sánh tính chất hóa học của halogen
Hóa chất: dung dịch NaBr, NaI, nước chlorine, nước bromine và dung dịch hồ tinh bột.
Dụng cụ: ống nghiệm, ống hút nhỏ giọt, kẹp gỗ, giá để ống nghiệm.
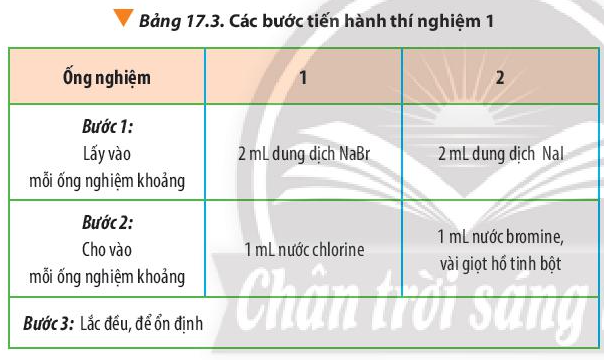
Tiến hành: Thực hiện các bước theo Bảng 17.3
Lời giải:
Hiện tượng:
- Ống nghiệm 1: Dung dịch NaBr không màu, khi thêm 1 ml nước chlorine, dung dịch có màu vàng.
- Ống nghiệm 2: Dung dịch NaI không có màu, khi thêm nước bromine, dung dịch sẫm màu. Sau đó nhỏ vài giọt dung dịch hồ tinh bột, dung dịch có màu đen tím.

Lời giải:
Giải thích kết quả thí nghiệm 1:
- Ống nghiệm 1: Tính oxi hóa của chlorine mạnh hơn bromine, chlorine sẽ oxi hóa ion bromide thành bromine, dung dịch bromine có màu vàng. Phương trình hóa học:
Cl2 + 2NaBr → 2NaCl + Br2
- Ống nghiệm 2: Tính oxi hóa của bromine mạnh hơn iodine, bromine sẽ oxi hóa ion iodide thành iodine, I2 tan tốt trong dung dịch NaI, dung dịch sẫm màu. Tính chất đặc trưng của iodine khi kết hợp với hồ tinh bột cho dung dịch màu đen tím.
Br2 + 2NaI → 2NaBr + I2
Câu hỏi 14 trang 111 Hóa học 10: Tiến hành thí nghiệm 2, quan sát và ghi nhận hiện tượng.
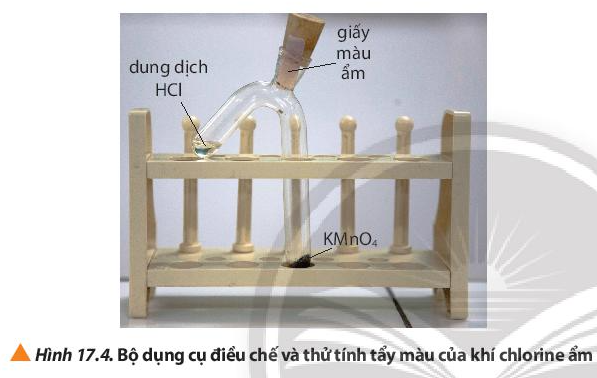
Thí nghiệm 2: Tính tẩy màu của khí chlorine ẩm
Hóa chất: tinh thể potassium permanganate (KMnO4), dung dịch HCl đặc, giấy màu, nước cất.
Dụng cụ: ống nghiệm 2 nhánh, nút cao su, giá đỡ, thìa thủy tinh, ống hút nhỏ giọt.
Lưu ý: Kiểm tra nút cao su phải được đậy kín trước khi thực hiện bước 2.
Bước 2: Nghiêng ống nghiệm sao cho dung dịch HCl tiếp xúc với KMnO4.
Phương trình hóa học của phản ứng điều chế khí Cl2:
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
Lời giải:
Hiện tượng: Khi nghiêng ống nghiệm để HCl tiếp xúc với KMnO4, có hiện tượng sủi bọt khí màu vàng, khí thoát ra làm giấy màu ẩm bị mất màu.
Lời giải:
Phương trình hóa học của phản ứng điều chế khí Cl2:
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
KMnO4 đã phản ứng với HCl tạo khí Cl2 có màu vàng lục.
Khí Cl2 tác dụng chậm với nước tạo thành HCl và HClO, trong đó HClO có tính oxi hóa mạnh nên có khả năng tẩy màu.
Cl2 + H2O ⇌ HCl + HClO
Luyện tập trang 112 Hóa học 10: Viết phương trình hóa học của các phản ứng sau:
Lời giải:
Cu + Cl2 → CuCl2 (1)
2Al + 3Br2 → 2AlBr3 (2)
2Ca(OH)2 + 2Cl2 → CaCl2 + Ca(OCl)2 + 2H2O (3)
6KOH + 3Br2 5KBr + KBrO3 + 3H2O (4)
Cl2 + 2KBr → 2KCl + Br2 (5)
Br2 + 2NaI → 2NaBr + I2 (6)
Lời giải:
Tính tẩy màu của khí chlorine ẩm được ứng dụng:
+ Tẩy trắng sợi, vải, giấy.
+ Sản xuất chất tẩy rửa, diệt khuẩn (như nước javel …)
+ Khử trùng nước sinh hoạt, nước trong các bể bơi.
6. Ứng dụng của các halogen
Câu hỏi 16 trang 113 Hóa học 10: Nhận xét vai trò của halogen trong đời sống, sản xuất và y tế
Lời giải:
Halogen có vai trò rất quan trọng trong đời sống, sản xuất và y tế.
- Fluorine: được sử dụng để sản xuất các chất dẻo ma sát thấp: teflon phủ trên bề mặt chảo, thiết bị nhà bếp, dụng cụ thí nghiệm,… Một số hợp chất của fluorine dùng trong sản xuất nhôm, thuốc trừ sâu, chống gián,…. Một số muối fluorien được thêm vào thuốc đánh răng, tạo men răng,…
- Chlorine: được sử dụng để tẩy trắng, khử trùng nước; một lượng lớn chlorine được dùng để sản xuất dung môi hữu cơ,…

- Bromine: được sử dụng điều chế thuốc an thần, thuốc trừ sâu, thuốc nhuộm, mực in, …

- Iodine: các hợp chất iodine được sử dụng làm chất xúc tác, dược phẩm, thuốc nhuộm,…

Câu hỏi 17 trang 113 Hóa học 10: Tìm hiểu thêm những ứng dụng khác của halogen trong thực tế.
Lời giải:
Một số ứng dụng khác của halogen trong thực tế:
- Ứng dụng làm đèn halogen: Sự kết hợp của khí halogen (iodine và bromine) và sợi wolfram tạo ra phản ứng hóa học chu trình halogen làm bổ sung wolfram cho dây tóc, tăng tuổi thọ và duy trì độ trong suốt của vỏ bóng đèn.
- Fluorine được dùng làm chất sinh hàn trong tủ lạnh. Ngoài ra còn dùng trong công nghiệp hạt nhân để làm giàu 235U.
- Đồng vị phóng xạ 131I dùng để điều trị một số bệnh lí tuyến giáp tự miễn như cường giáp tự miễn, ung thư tuyến giáp …
Lời giải:
Nước Javel (hỗn hợp NaCl và NaClO) có tính oxi hóa mạnh, có tính tẩy màu nên có thể tẩy được vết mực trên áo trắng nhưng không nên sử dụng trên vải quần, áo màu vì nước Javel sẽ làm mất màu của quần áo đó.

Lời giải:
a) Cl2 + H2 2HCl
b) F2 + Cu → CuF2
c) I2 + 2Na 2NaI
d) 3Cl2 + 2Fe 2FeCl3
e) 2Br2 + 2Ca(OH)2 → CaBr2 + Ca(OBr)2 + 2H2O
f) 3Cl2 + 6KOH 5KCl + KClO3 + 3H2O
g) Br2 + 2KI → 2KBr + I2
Trả lời:
Halogen có cấu hình electron lớp ngoài cùng là ns2np5, nên nguyên tử dễ dàng nhận thêm 1 electron hoặc dùng chung electron với nguyên tử khác để đạt cấu hình electron bền vững của khí hiếm tương ứng từ đó tạo nên các hợp chất hóa học.
Trong tự nhiên, vì tính oxi hóa mạnh nên halogen oxi hóa hầu hết các chất nên không tồn tại ở dạng tự do,
Lời giải:
a) 200 lít nước ⇔ 200 000 g nước
250 mg = 0,25 g
Đặt x là số viên nén chloramine B 25% (loại viên 1 gam)
⇒ m chất tan = 0,25x (gam)
Áp dụng công thức tính nồng độ phần trăm:
⇔ ⇔ x = 8
Vậy cần dùng 8 viên nén chloramine B 25% (loại viên 1 gam) để xử lí bình chứa 200 lít nước.
b) 1 lít nước ⇔ 1 kg nước = 1000 g nước.
Đặt y là khối lượng chloramine B 25% dạng bột cần dùng
⇒ m chất tan = 0,25.y (gam)
Áp dụng công thức tính nồng độ phần trăm:
⇔ ⇔ y = 81,6 gam
Vậy cần dử dụng 81,6 gam chloramine B 25% dạng bột pha với 1 lít nước để được dung dịch sát khuẩn 2%.