Giải Hoá 10 (Chân trời sáng tạo) Bài 9: Liên kết ion
Hoidap.vietjack.com trân trọng giới thiệu: lời giải bài tập Hoá lớp 10 Bài 9: Liên kết ion sách Chân trời sáng tạo hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hoá 10 Bài 9. Mời các bạn đón xem:
Giải bài tập Hóa lớp 10 Bài 9: Liên kết ion
Video giải Hóa lớp 10 Bài 9: Liên kết ion
Muối thường là các hợp chất chứa liên kết ion. Liên kết ion là gì?
Lời giải:
Liên kết ion là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
1. Ion và sự hình thành liên kết ion
Lời giải:
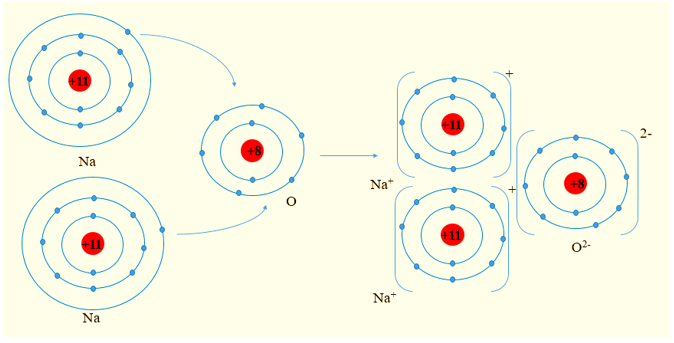
- Ion sodium có số electron trên lớp vỏ ít hơn số proton trong hạt nhân.
- Ion oxide có số electron trong lớp vỏ nhiều hơn số proton trong hạt nhân.
Lời giải:
Điện tích ion = số đơn vị điện tích hạt nhân – số electron của ion.
+ Điện tích ion sodium = 11 – 10 = +1
+ Điện tích ion oxide = 8 – 10 = -2.
Lời giải:
- Ion Na+ và ion O2- thu được đều có 8 electron ở lớp ngoài cùng nên bền vững về mặt hóa học.
- Hai ion Na+ và O2- đều có cấu hình electron giống với khí hiếm He với 2 lớp electron và 8 electron ở lớp ngoài cùng.
Lời giải:
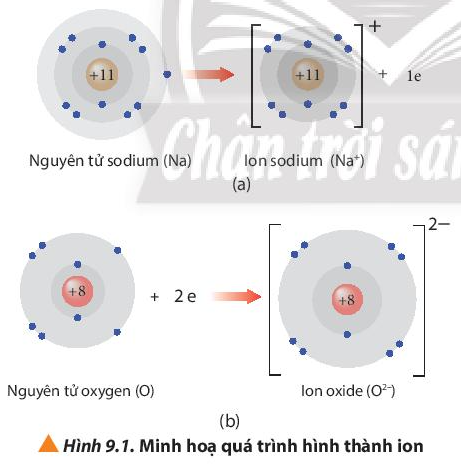
- Nguyên tử các nguyên tố kim loại dễ nhường electron tạo thành cation.
- Nguyên tử các nguyên tố phi kim dễ nhận electron tạo thành anion.
Lời giải:
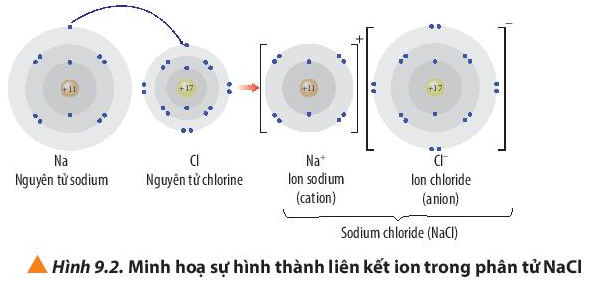
Nguyên tử Na (Z = 11) nhường đi 1 electron ở lớp ngoài cùng trở thành ion mang điện tích dương, kí hiệu là Na+.
Nguyên tử Cl (Z = 17) nhận 1 electron từ nguyên tử Na trở thành ion mang điện tích âm, kí hiệu là Cl-.
Các ion Na+ và Cl- mang điện tích trái dấu hút nhau tạo thành liên kết trong phân tử NaCl.
Phương trình hóa học: 2Na + Cl2 → 2NaCl.
Lời giải:
- Ion Na+ có 2 lớp electron, lớp ngoài cùng có 8 electron ⇒ Cấu hình electron ion Na+ giống cấu hình electron của khí hiếm Ne.
- Ion Cl- có 3 lớp electron, lớp ngoài cùng có 8 electron ⇒ Cấu hình electron ion Cl- giống với cấu hình electron của khí hiếm Ar.
Lời giải:
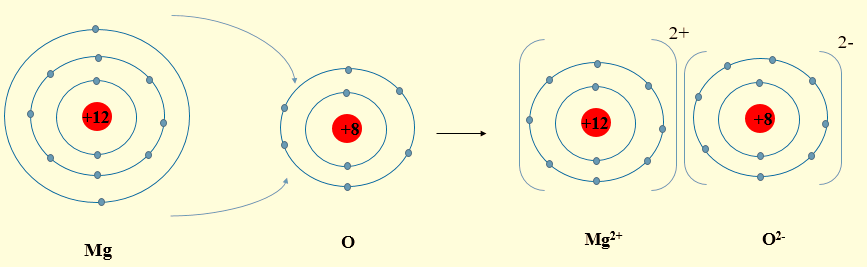
- Nguyên tử Mg (cấu hình electron: 1s22s22p63s2) có 2 electron ở lớp ngoài cùng, có xu hướng nhường 2 electron để đạt cấu hình electron của khí hiếm, tạo thành ion Mg2+.
- Nguyên tử O (cấu hình electron: 1s22s22p4) có 6 electron ở lớp ngoài cùng, có xu hướng nhận 2 electron của Mg để đạt cấu hình electron của khí hiếm, tạo thành ion O2-.
- Hai ion Mg2+ và O2- tạo thành mang điện tích trái dấu, hút nhau tạo thành phân tử MgO
2. Tinh thể ion
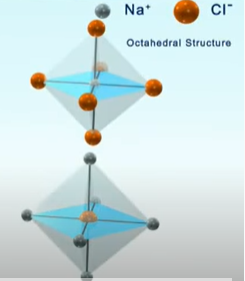
Câu hỏi 7 trang 56 Hóa học 10: Quan sát Hình 9.3, cho biết:
a) Tinh thể NaCl có cấu trúc của hình khối nào.
b) Các ion Na+ và Cl- phân bố trong tinh thể như thế nào
c) Xung quanh mỗi loại ion có bao nhiêu ion ngược dấu gần nhất
Lời giải:
a) Tinh thể NaCl có cấu trúc là hình lập phương.
b) Các ion Na+ và Cl- được xếp xen kẽ nhau đều đặn trên các đỉnh và tâm các mặt của hình lập phương.
c) Xung quanh mỗi loại ion có 6 ion ngược dấu gần nhất.
Câu hỏi 8 trang 56 Hóa học 10: Em hiểu thế nào về tinh thể ion?
Lời giải:
Tinh thể ion là loại tinh thể được tạo nên bởi các cation và anion. Các ion được sắp xếp theo trật tự nhất định trong không gian theo kiểu mạng lưới (ở các nút mạng các cation và anion xếp luân phiên liên kết chặt chẽ với nhau do cân bằng lực hút và lực đẩy).
Lời giải:
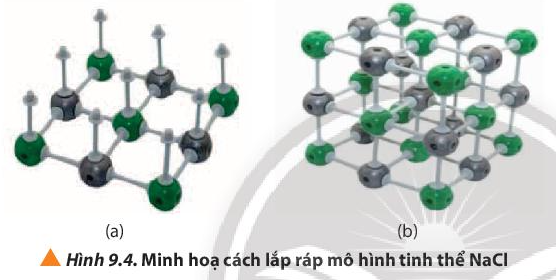
Quan sát hình 9.4 ta có:
- Số lượng quả cầu cần là: 3 × 3 × 3 = 27 quả.
- Số lượng mỗi que nối cần là: 12 × 3 + 9 × 2 = 54 que nối.
Lời giải:
Lượng ion Na+ mà người này nạp vào cơ thể là:
= 1,966 gam = 1966 mg
Ta có: 500 < 1966 < 2300 nên nếu một người sử dụng 5,0 g muối ăn mỗi ngày thì lượng ion Na+ mà người ấy nạp vào cơ thể không vượt mức giới hạn cho phép.
Bài tập (trang 58)
Bài 1 trang 58 Hóa học 10: Ion Mg2+ có cấu hình electron giống cấu hình electron của khí hiếm nào?
Lời giải:
Đáp án đúng là: B
Cấu hình electron nguyên tử Mg (Z = 12): 1s22s22p63s2
Nguyên tử Mg nhường 2 electron tạo thành ion Mg2+ có cấu hình electron là:
1s22s22p6 giống với cấu hình electron của khí hiếm neon.
Lời giải:
Đáp án đúng là: D
- Cấu hình electron của ion Ca2+ là: 1s22s22p6 3s23p6 giống với cấu hình electron của khí hiếm agon.
- Cấu hình electron của ion F- là: 1s22s22p6 giống với cấu hình electron của khí hiếm neon.
- Cấu hình electron của ion Al3+ là: 1s22s22p6 giống với cấu hình electron của khí hiếm neon.
- Cấu hình electron của ion N3- là:1s22s22p6 giống với cấu hình electron của khí hiếm neon.
b) Có hợp chất ion nào chỉ tạo bởi các ion trên với nhau không? Vì sao?
Lời giải:
a)
– Potassium (K, Z = 19) có cấu hình electron là: 1s22s22p63s23p64s1
Nguyên tử K nhường 1 electron tạo thành ion K+ có cấu hình electron là: 1s22s22p63s23p6 giống với cấu hình electron của khí hiếm Ar.
- Cấu hình electron của nguyên tử Mg (Z = 12): 1s22s22p63s2
Nguyên tử Mg nhường 2 electron tạo thành ion Mg2+ có cấu hình electron là:1s22s22p6 giống với cấu hình electron của khí hiếm neon.
b) Hợp chất ion được tạo thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
Do đó không có hợp chất ion nào chỉ tạo bởi các ion K+ và Mg2+ với nhau vì hai ion này cùng mang điện tích dương.
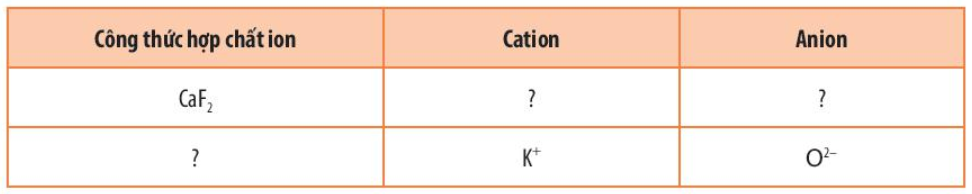
Bài 4 trang 58 Hóa học 10: Hoàn thành những thông tin còn thiếu trong bảng sau:
Lời giải:
|
Công thức hợp chất ion |
Cation |
Anion |
|
CaF2 |
Ca2+ |
F- |
|
K2O |
K+ |
O2- |
Lời giải:
- Nguyên tử Na (Z = 11, cấu hình electron: 1s22s22p63s1) có 1 electron ở lớp ngoài cùng, có xu hướng nhường 1 electron để đạt cấu hình electron của khí hiếm, tạo thành ion Na+.
- Nguyên tử O (Z = 8, cấu hình electron: 1s22s22p4) có 6 electron ở lớp ngoài cùng, có xu hướng nhận 2 electron để đạt cấu hình electron của khí hiếm, tạo thành ion O2-.
Nguyên tử O nhận 2 electron của hai nguyên tử Na tạo thành ion là O2-.
- Hai ion Na+ và ion O2- hút nhau tạo thành phân tử Na2O.