Bạn A và B thực hiện phản ứng giữa kẽm với dung dịch hydrocloric acid
Lời giải Bài 16.12 trang 52 SBT Hóa học 10 sách Cánh Diều hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập Hóa học 10.
Giải SBT Hóa học 10 Cánh Diều Bài 16: Tốc độ phản ứng hóa học
Bài 16.12 trang 52 SBT Hóa học 10: Bạn A và B thực hiện phản ứng giữa kẽm với dung dịch hydrocloric acid và thu được thể tích khí thoát ra theo thời gian. Hai bạn lặp lại thí nghiệm ba lần và kết quả của ba lần thí nghiệm được hai bạn ghi vào bảng sau:
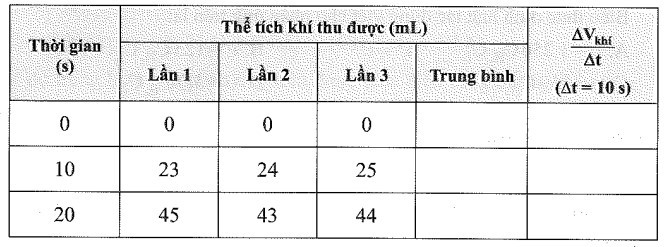
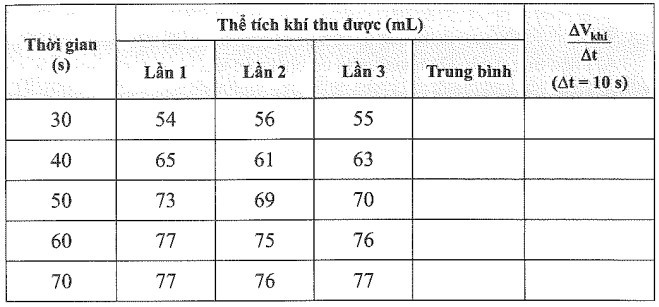
a) Cho biết khí thoát ra là khí gì. Hãy viết và cân bằng phương trình hoá học của phản ứng xảy ra.
b) Hoàn thành hai cột còn trống trong bảng trên. Hãy biểu diễn kết quả của hai bạn lên đồ thị thể tích khí thu được theo thời gian. Vì sao hai bạn lại lặp lại thí nghiệm ba lần?
c) Dựa vào đồ thị, cho biết khi nào phản ứng kết thúc. Vì sao?
d) Phản ứng diễn ra nhanh nhất trong khoảng thời gian nào? Sau đó, phản ứng diễn ra nhanh dần hay chậm dần?
e) Nếu thí nghiệm được lặp lại với nồng độ HCl lớn hơn thì tốc độ phản ứng sẽ nhanh hơn hay chậm hơn?
g) Nếu hai bạn không đo được thể tích khí thoát ra, em hãy đề xuất một cách khác để xác định tốc độ phản ứng.
Lời giải:
a) Khí thoát ra là khí H2.
Phương trình hóa học: Zn(s) + 2HCl(aq) → H2(g) + ZnCl2(aq)
b) Hoàn thành bảng:
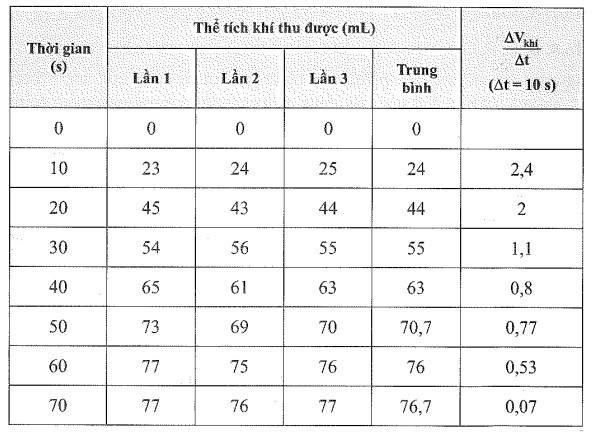
Biểu diễn kết quả của hai bạn lên đồ thị thể tích khí thu được theo thời gian:
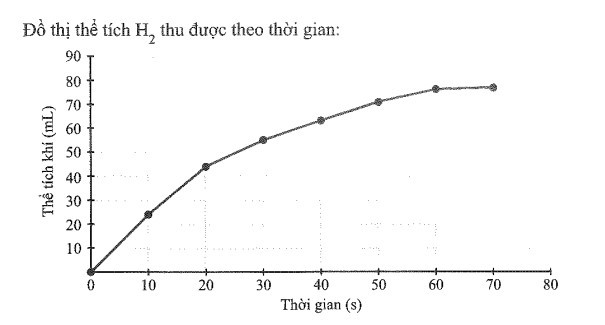
Hai bạn cần lặp lại thí nghiệm ba lần để giảm sai số trong quá trình thực nghiệm và tăng độ tin cậy của kết quả thu được.
c) Dựa vào đồ thị thấy khoảng 70 giây phản ứng sẽ kết thúc vì khi đó khí thoát ra rất chậm và gần như không đổi.
d) Dựa vào đồ thị xác định phản ứng nhanh nhất trong khoảng 10 giây đầu, sau đó chậm dần.
e) Nếu thí nghiệm được lặp lại với nồng độ HCl lớn hơn thì tốc độ phản ứng sẽ nhanh hơn.
g) Nếu hai bạn không đo được thể tích khí thoát ra, có thể thực hiện thí nghiệm bằng cách đặt bình phản ứng lên cân và theo dõi sự thay đổi khối lượng của bình phản ứng khi phản ứng diễn ra để tính khối lượng H2 thu được.
Xem thêm các bài giải sách bài tập Hóa học 10 bộ sách Cánh Diều hay, chi tiết khác:
Bài 16.1 trang 49 SBT Hóa học 10: Những phát biểu nào sau đây là đúng?
Bài 16.2 trang 49 SBT Hóa học 10: Những phát biểu nào sau đây không đúng?
Bài 16.3 trang 49 SBT Hóa học 10: Khi cho một lượng xác định chất phản ứng vào bình để cho phản ứng hoá học xảy ra, tốc độ phản ứng sẽ ...
Bài 16.4 trang 50 SBT Hóa học 10: Tốc độ phản ứng còn được tính theo sự thay đổi lượng chất (số mol, khối lượng) theo thời gian. Cho hai phản ứng xảy ra đồng thời trong hai bình (1) và (2):...
Bài 16.5 trang 50 SBT Hóa học 10: Cho hai phản ứng có phương trình hóa học như sau:...
Bài 16.6 trang 50 SBT Hóa học 10: Phản ứng 3H2 + N2 → 2NH3 có tốc độ mất đi của H2 so với tốc độ hình thành NH3 như thế nào?...
Bài 16.7 trang 50 SBT Hóa học 10: Cho phản ứng:...
Bài 16.8 trang 51 SBT Hóa học 10: Những phát biểu nào sau đây không đúng?...
Bài 16.9 trang 51 SBT Hóa học 10: Cho phản ứng đơn giản: H2 + I2 → 2HI...
Bài 16.10 trang 51 SBT Hóa học 10: Cho phản ứng: 2A + B → 2M + 3N...
Bài 16.14 trang 53 SBT Hóa học 10: Một bạn học sinh thực hiện hai thí nghiệm:...
Xem thêm lời giải sách bài tập Hóa học lớp 10 Cánh diều với cuộc sống hay, chi tiết khác:
Bài 17: Nguyên tố và đơn chất halogen
Bài 18: Hydrogen halide và hydrohalic acid
Bài 14: Phản ứng hóa học và enthalpy
Bài 15: Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học


