Sách bài tập Hóa học 10 Bài 7 Cánh diều: Xu hướng biến đổi một số tính chất của đơn chất, biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm
Với giải sách bài tập Hóa học 10 Bài 7: Xu hướng biến đổi một số tính chất của đơn chất, biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm sách Cánh diều hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập trong SBT Hóa học 10 Bài 7.
Giải sách bài tập Hóa học lớp 10 Bài 7: Xu hướng biến đổi một số tính chất của đơn chất, biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm - Cánh diều
a) Al và In.
b) Si và N.
c) P và Pb.
d) C và F.
Lời giải:
a) Al và In thuộc cùng nhóm IIIA, ZAl < ZIn do đó bán kính In lớn hơn.
b) So sánh gián tiếp qua P:
Si và P thuộc cùng chu kì 3, ZSi < ZP do đó bán kính Si > P (1).
N và P thuộc cùng nhóm VA, ZP > ZN do đó bán kính P > N (2).
Từ (1) và (2) có bán kính Si lớn hơn bán kính N.
c) So sánh gián tiếp qua Bi:
P và Bi cùng thuộc nhóm VA, ZBi > ZP nên bán kính Bi > P (1)
Pb và Bi cùng thuộc chu kì 6, ZPb < ZBi nên bán kính Pb > Bi (2)
Từ (1) và (2) có bán kính Pb lớn hơn bán kính P.
d) C và F cùng thuộc chu kì 2, Zc < ZF nên bán kính C lớn hơn bán kính F.
Bài 7.2 trang 20 SBT Hóa học 10: Dãy nguyên tử nào sau đây có bán kính tăng dần?
Lời giải:
Đáp án đúng là: A
|
|
Nhóm IA |
Nhóm IIA |
Nhóm IVA |
Nhóm VIA |
Nhóm VIIA |
|
Chu kì 2 |
|
|
|
|
F |
|
Chu kì 3 |
|
|
Si |
S |
|
|
Chu kì 4 |
|
Ca |
Ge |
|
|
|
Chu kì 5 |
Rb |
|
|
|
|
Theo quy luật biến đổi bán kính trong 1 chu kì và nhóm có bán kính các nguyên tử tăng dần theo thứ tự: F < S < Si < Ge < Ca < Rb.
Bài 7.3 trang 20 SBT Hóa học 10: Dãy các ion nào sau đây có bán kính tăng dần?
Lời giải:
Đáp án đúng là: D
Các ion này đều có cấu hình electron là 1s22s22p63s23p6, bán kính ion sẽ phụ thuộc vào điện tích hạt nhân.
Điện tích hạt nhân càng lớn càng hút mạnh electron ở lớp ngoài cùng, bán kính sẽ càng nhỏ. Điện tích hạt nhân của Ca2+, K+, Cl-, S2- lần lượt là +20, +19, +17, +16 nên bán kính sẽ tăng dần từ Ca2+, K+, Cl-, S2-.
Bài 7.4 trang 20 SBT Hóa học 10: Cho bảng số liệu sau đây:
Dựa trên xu hướng biến đổi tuần hoàn và dữ liệu trong bảng trên, giá trị nào sau đây là phù hợp nhất với bán kính ion K+?
A. 90 pm.
B. 133 pm.
C. 195 pm.
D. 295 pm.
Lời giải:
Đáp án đúng là: B
Các cation luôn có bán kính nhỏ hơn đáng kể so với nguyên tử trung hòa tương ứng do có số lượng electron ít hơn, lực hút của hạt nhân lên các electron mạnh hơn, do vậy bán kính của K+ phải nhỏ hơn bán kính của K (227 pm).
Bên cạnh đó, theo xu hướng biến đổi tuần hoàn thì bán kính của K+ phải lớn hơn bán kính của Na+ (98 pm), tương tự như bán kính của K lớn hơn của Na.
Trong hai giá trị 133 và 195 pm, giá trị 133 pm phù hợp hơn vì thể hiện sự giảm đáng kể bán kính cation so với nguyên tử trung hòa, tương tự trường hợp Na và Na+ trong bảng số liệu.
Lời giải:
Đáp án đúng là: B
Tính kim loại giảm dần theo chiều từ trái sang phải trong một chu kì và tăng dần từ trên xuống dưới trong một nhóm.
Lời giải:
a) Sr và Sb.
Sr và Sb cùng thuộc chu kì 5, ZSr < ZSb nên Sr thể hiện tính kim loại nhiều hơn so với Sb.
b) As và Bi.
As và Bi cùng thuộc nhóm VA, ZAs < ZBi nên Bi thể hiện tính kim loại nhiều hơn so với As.
c) B và O.
B và O cùng thuộc chu kì 2, ZB < ZO nên B thể hiện tính kim loại nhiều hơn so với O.
d) S và As.
So sánh gián tiếp thông qua Se.
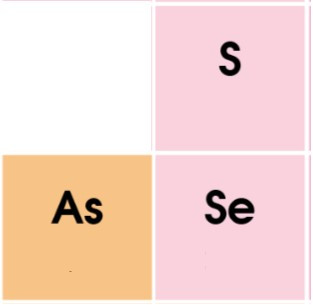
Tính kim loại: As > Se > S
Vậy As thể hiện tính kim loại nhiều hơn S.
Bài 7.7 trang 21 SBT Hóa học 10: Dãy các nguyên tố nào sau đây có tính kim loại giảm dần?
Lời giải:
Đáp án đúng là: C
|
|
Nhóm IIA |
Nhóm IIIA |
Nhóm IVA |
Nhóm VA |
|
Chu kì 2 |
|
|
|
N |
|
Chu kì 3 |
|
Al |
Si |
P |
|
Chu kì 4 |
|
|
|
|
|
Chu kì 5 |
Sr |
|
|
|
Dựa vào quy luật biến đổi tính kim loại trong một chu kì và trong một nhóm A, ta có tính kim loại giảm dần theo thứ tự: Sr > Al > Si > P > N.
Lời giải:
Đáp án đúng là: B
Xét trong một chu kì theo chiều tăng dần của điện tích hạt nhân (chiều từ trái sang phải) độ âm điện của các nguyên tố nhìn chung tăng dần, tính phi kim của các nguyên tố tăng dần, tính kim loại giảm dần, bán kính nguyên tử giảm dần.
Như vậy, xu hướng biến đổi độ âm điện của các nguyên tố trong bảng tuần hoàn tương tự như xu hướng biến đổi của tính phi kim.
Lời giải:
Đáp án đúng là: A
Ta có 1s22s22p5 là cấu hình electron của F (Z = 9), đây là nguyên tố có độ âm điện lớn nhất trong bảng tuần hoàn (3,98).
Lời giải:
Trong số các nguyên tố thuộc chu kì 2 trong bảng tuần hoàn (trừ Ne), (1) Li là nguyên tố có độ âm điện nhỏ nhất và bán kính nguyên tử (2) lớn nhất; (3) F là nguyên tố có độ âm điện lớn nhất nhưng bán kính nguyên tử (4) nhỏ nhất. Tính kim loại giảm dần từ (5) Li tới (6) F, còn tính phi kim thì biến đổi theo chiều ngược lại.
D. Mức độ lệch của cặp electron là như nhau trong ba trường hợp.
Lời giải:
Đáp án đúng là: C
Thứ tự đúng là: F > Cl > Br vì độ âm điện F > Cl > Br (các nguyên tố trong cùng một nhóm VIIA).
Lời giải:
|
Basic oxide |
Acidic oxide |
Oxide lưỡng tính |
|
Na2O, MgO |
Al2O3 |
P2O5, SO3, Cl2O7 |
Bài 7.13 trang 22 SBT Hóa học 10: Những oxide nào sau đây tạo ra môi trường acid khi cho vào nước?
Lời giải:
Đáp án đúng là: A và B.
CO2 và SO3 là ocidic oxide nên tạo ra môi trường acid khi cho vào nước.
|
a) Một khí hoạt động rất mạnh, nguyên tử có độ âm điện lớn: |
Lời giải:
a ghép với 4; b ghép với 1; c ghép với 2; d ghép với 3.
Lời giải:
Nhôm – Al thuộc nhóm IIIA, vậy eka – nhôm (Ea) thuộc nhóm IIIA cũng sẽ có 3 electron lớp ngoài cùng, công thức oxide cao nhất sẽ là Ea2O3, công thức hydroxide là Ea(OH)3.
Al(OH)3 là một chất lưỡng tính nên Ea(OH)3 cũng có khả năng là một chất lưỡng tính, nhưng sẽ thể hiện tính base mạnh hơn Al(OH)3.
a) Nếu giữa X và Y hình thành liên kết thì cặp electron liên kết sẽ bị lệch về phía nguyên tử nào?
Lời giải:
a) Nếu giữa X và Y hình thành liên kết thì cặp electron liên kết sẽ bị lệch về phía nguyên tử X (nguyên tử có độ âm điện lớn hơn).
b) Giả sử X và Y ở cùng một chu kì của bảng tuần hoàn, em dự đoán nguyên tố Y có bán kính nguyên tử lớn hơn, do độ âm điện của X lớn hơn Y, mà trong một chu kỳ, chiều tăng bán kính nguyên tử là chiều giảm của độ âm điện.
c) Nếu X và Y ở cùng một chu kì của bảng tuần hoàn, oxide cao nhất của X sẽ có tính acid mạnh hơn oxide cao nhất của Y do tính phi kim của X mạnh hơn Y (độ âm điện của X lớn hơn Y).
Lời giải:
M là nguyên tố kim loại nhóm IA do phản ứng với nước tạo MOH nên sẽ có 1 electron ở lớp ngoài cùng.
Nếu M ở chu kì 4, M sẽ có 4 lớp electron.
Cấu hình electron của M là: 1s22s22p63s23p64s1.


