Khi pha loãng 100 mL H^2SO^4 đặc bằng nước thấy cốc đựng dung dịch nóng lên
Lời giải Bài 14.11 trang 43 SBT Hóa học 10 sách Cánh Diều hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập Hóa học 10.
Giải SBT Hóa học 10 Cánh Diều Bài 14: Phản ứng hóa học và enthalpy
Bài 14.11 trang 43 SBT Hóa học 10: Khi pha loãng 100 mL H2SO4 đặc bằng nước thấy cốc đựng dung dịch nóng lên. Vậy quá trình pha loãng H2SO4 đặc là quá trình thu nhiệt hay tỏa nhiệt?
Theo em, khi pha loãng H2SO4 đặc nên cho từ từ H2SO4 đặc vào nước hay ngược lại? Vì sao?
Lời giải:
Khi pha loãng 100 mL H2SO4 đặc bằng nước thấy cốc đựng dung dịch nóng lên. Vậy quá trình pha loãng H2SO4 đặc là quá trình tỏa nhiệt.
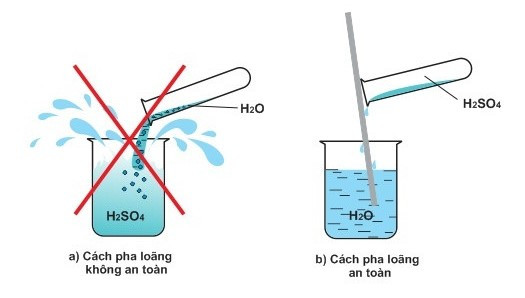
Để pha loãng H2SO4 đặc an toàn cần cho từ từ H2SO4 đặc vào nước và khuấy nhẹ bằng đũa thủy tinh. Tuyệt đối không làm ngược lại vì phản ứng tỏa nhiệt mạnh, làm nước sôi đột ngột kéo theo những giọt acid bắn ra ngoài gây nguy hiểm.
Xem thêm các bài giải sách bài tập Hóa học 10 bộ sách Cánh Diều hay, chi tiết khác:
Bài 14.1 trang 41 SBT Hóa học 10: Những phát biểu nào sau đây là đúng?...
Bài 14.2 trang 41 SBT Hóa học 10: Những phát biểu nào sau đây là không đúng?...
Bài 14.3 trang 41 SBT Hóa học 10: Phát biểu nào sau đây đúng? ...
Bài 14.4 trang 41 SBT Hóa học 10: Mỗi quá trình sau đây là thu nhiệt hay tỏa nhiệt?...
Bài 14.6 trang 42 SBT Hóa học 10: Chọn câu trả lời đúng...
Bài 14.7 trang 42 SBT Hóa học 10: Những phát biểu nào sau đây đúng?...
Bài 14.8 trang 42 SBT Hóa học 10: Cho hai phản ứng cùng xảy ra ở điều kiện chuẩn:...
Bài 14.9 trang 43 SBT Hóa học 10: Phản ứng phân hủy 1 mol H2O (g) ở điều kiện tiêu chuẩn:...
Bài 14.12 trang 43 SBT Hóa học 10: Nhiệt tỏa ra khi đốt cháy 1 gam một mẫu than là 23,0 kJ...
Xem thêm lời giải sách bài tập Hóa học lớp 10 Cánh diều với cuộc sống hay, chi tiết khác:
Bài 15: Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học
Bài 16: Tốc độ phản ứng hóa học
Bài 17: Nguyên tố và đơn chất halogen


