Quảng cáo
1 câu trả lời 246
Chào bạn, tôi sẽ giúp bạn đánh giá sự sắp xếp electron trong các cấu hình trên:
Nguyên tắc loại trừ Pauli: Mỗi orbital nguyên tử chỉ chứa tối đa 2 electron có spin đối nhau.
Quy tắc Hund: Trong một phân lớp electron (ví dụ: p, d, f), các electron sẽ chiếm các orbital riêng biệt trước khi chúng bắt đầu ghép đôi trong cùng một orbital. Các electron độc thân trong cùng một phân lớp phải có spin song song.
Đánh giá:
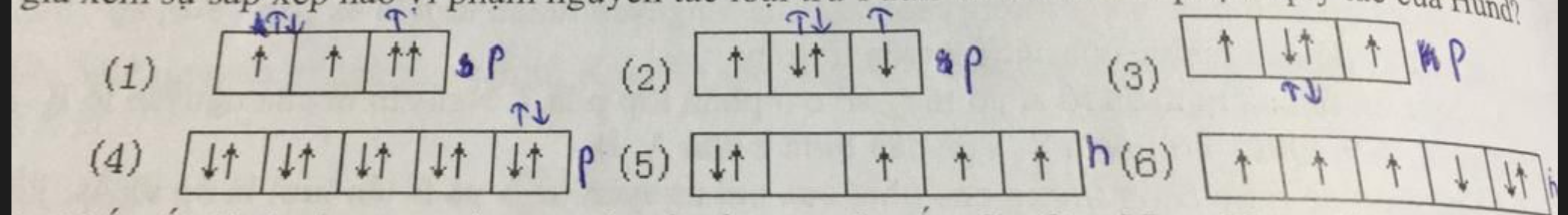
(1) Vi phạm quy tắc Hund: Các electron trong phân lớp 2p phải được phân bố vào mỗi orbital trước khi ghép đôi. Ở đây, có một orbital trống trong khi orbital khác đã chứa 2 electron.
(2) Vi phạm quy tắc Hund: Tương tự như (1), các electron nên được phân bố đều vào mỗi orbital 2p trước khi ghép đôi.
(3) Đúng: Tuân theo cả quy tắc Pauli và Hund. Mỗi orbital 2p chứa tối đa 2 electron với spin đối nhau, và các electron độc thân có spin song song.
(4) Vi phạm quy tắc Pauli: Orbital cuối cùng của phân lớp 2p chứa 3 electron, vượt quá số lượng tối đa 2 electron.
(5) Đúng: Tuân theo cả quy tắc Pauli và Hund. Mỗi orbital 3d chứa 1 electron độc thân với spin song song.
(6) Vi phạm quy tắc Hund: Các electron trong phân lớp 3d nên được phân bố vào mỗi orbital trước khi ghép đôi. Ở đây, có một orbital trống trong khi orbital khác đã chứa 2 electron.
Tóm lại:
Vi phạm Pauli: (4)
Vi phạm Hund: (1), (2), (6)
Đúng: (3), (5)
Quảng cáo
Bạn cần hỏi gì?
Câu hỏi hot cùng chủ đề
-
Hỏi từ APP VIETJACK105525
-
Hỏi từ APP VIETJACK
 Đã trả lời bởi chuyên gia
64941
Đã trả lời bởi chuyên gia
64941 -
 Đã trả lời bởi chuyên gia
59184
Đã trả lời bởi chuyên gia
59184 -
 Đã trả lời bởi chuyên gia
42319
Đã trả lời bởi chuyên gia
42319 -
Hỏi từ APP VIETJACK
 Đã trả lời bởi chuyên gia
39500
Đã trả lời bởi chuyên gia
39500