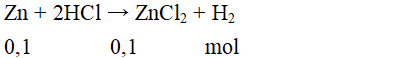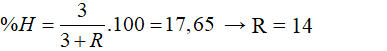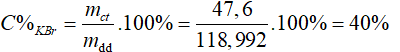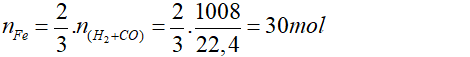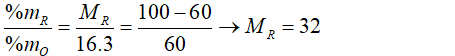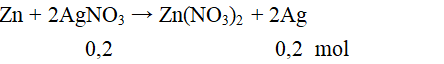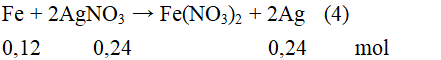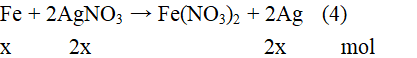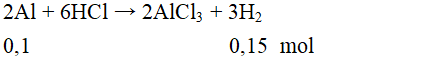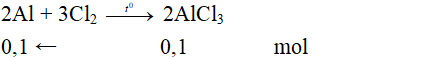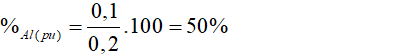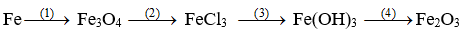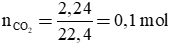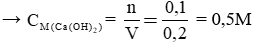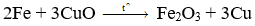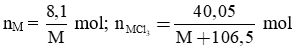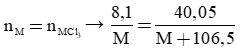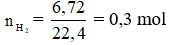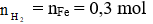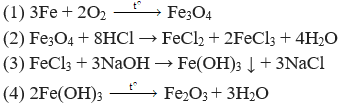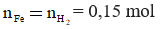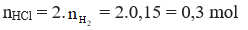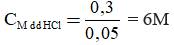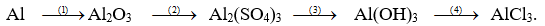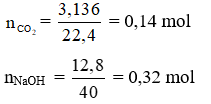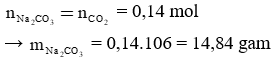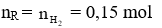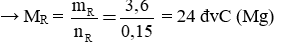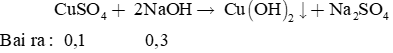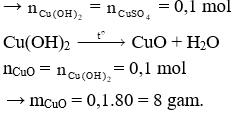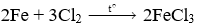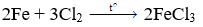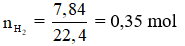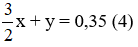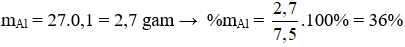Bộ 30 đề thi Học kì 1 Hóa học lớp 9 có đáp án
Bộ 30 đề thi Học kì 1 Hóa học lớp 9 có đáp án giúp học sinh ôn luyện để đạt điểm cao trong bài thi Hóa học 9 Học kì 1. Mời các bạn cùng đón xem:
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Học kì 1 Hóa học lớp 9 có đáp án - (Đề số 1)
Phần trắc nghiệm
Câu 1: Dãy chất gồm các oxit bazơ là:
A. CuO, NO, MgO, CaO.
B. CuO, CaO, MgO, Na2O.
C. CaO, CO2, K2O, Na2O.
D. K2O, FeO, P2O5, Mn2O7.
Câu 2: Chất nào sau đây góp phần nhiều nhất vào sự hình thành mưa axit ?
A . CO2
B. SO2
C. N2
D. O3
Câu 3: Cho 0,1 mol kim loại kẽm vào dung dịch HCl dư. Khối lượng muối thu được là:
A. 20,4
B. 1,36 g
C. 13,6 g
D. 27,2 g
Câu 4: Phản ứng nào dưới đây là phản ứng trao đổi ?
A. 2Na + 2H2O → 2NaOH + H2
B. BaO + H2O → Ba(OH)2
C. Zn + H2SO4 → ZnSO4 + H2
D. BaCl2 + H2SO4 → BaSO4 + 2HCl
Câu 5: Khi thả một cây đinh sắt sạch vào dung dịch CuSO4 loãng, có hiện tượng sau:
A. Sủi bọt khí, màu xanh của dung dịch nhạt dần.
B. Có một lớp đồng màu đỏ phủ lên đinh sắt, màu xanh của dung dịch đậm dần.
C. Có một lớp đồng màu đỏ phủ lên đinh sắt, dung dịch không đổi màu.
D. Có một lớp đồng màu đỏ phủ lên đinh sắt, màu xanh của dung dịch nhạt dần
Câu 6: Có một mẫu Fe bị lẫn tạp chất là nhôm, để làm sạch mẫu sắt này bằng cách ngâm nó với:
A. Dung dịch NaOH dư
B. Dung dịch H2SO4 loãng
C. Dung dịch HCl dư
D. Dung dịch HNO3 loãng
Câu 7: Dãy phi kim tác dụng với oxi tạo thành oxit axit là:
A. S, C, P.
B. S, C, Cl2.
C. C, P, Br2.
D. C, Cl2, Br2.
Câu 8: X là nguyên tố phi kim có hoá trị III trong hợp chất với khí hiđro. Biết thành phần phần trăm khối lượng của hiđro trong hợp chất là 17,65%. X là nguyên tố:
A. C
B. S
C. N
D. P
Phần tự luận
Câu 1: (1 điểm). Hãy cho biết hiện tượng xảy ra khi nhúng một viên kẽm vào:
a. Dung dịch CuSO4
b. Dung dịch HCl
Câu 2: (1 điểm). Bằng phương pháp hóa học hãy nhận biết dung dịch các chất chứa trong các lọ bị mất nhãn sau: HCl, KOH, NaNO3, Na2SO4
Câu 3: (2 điểm). Hãy lập phương trình hóa học của các phản ứng sau:
a. Al + Cl2 →
b. Cu + AgNO3 →
c. Na2O + H2O →
d. FeCl3 + NaOH →
Câu 4: (1 điểm). Hoà tan hết 2,3g Na kim loại vào 97,8g nước . Hãy tính nồng độ % của dung dịch thu được sau phản ứng?
Câu 5: (1 điểm). Cho 10,5g hỗn hợp 2 kim loại Cu và Zn vào dd H2SO4 loãng dư, người ta thu được 2,24 lít khí (đktc). Hãy tính thành phần % theo khối lượng của Cu và Zn .
Câu 6: (1 điểm). Hoà tan hoàn toàn 3,25g một kim loại X (hoá trị II) bằng dung dịch HCl thu được 1,12 lít khí H2 (ở đktc). Hãy xác định tên kim loại X ?
Câu 7: (1 điểm). Ngâm lá sắt có khối lượng 56 gam vào dung dịch AgNO3, sau một thời gian lấy lá sắt ra rửa nhẹ cân được 57,6 gam. Hãy tính khối lượng Ag sinh ra sau phản ứng?
( Cho: N = 14, Na = 23, Cu = 64, Zn = 65, Ag = 108, O = 16 )
Đáp án đề thi Học kì 1 môn Hóa học 9 - Đề số 1
TRẮC NGHIỆM: (2 điểm)
Chọn đúng mỗi câu được 0,25đ
Câu 1. B
Oxit bazo là oxit của kim loại
Câu 2. B
SO2 góp phần gây nên mưa axit.
Câu 3. C
mmuối = 0,1.136 = 13,6 gam.
Câu 4. D
Phản ứng trao đổi: BaCl2 + H2SO4 → BaSO4 + 2HCl
Câu 5. D
Fe + CuSO4 → FeSO4 + Cu
Có một lớp đồng màu đỏ phủ lên đinh sắt, màu xanh của dung dịch nhạt dần
Câu 6. A
Al tác dụng với NaOH còn Fe thì không.
Câu 7. A
S + O2 → SO2
C + O2 → CO2
4P + 5O2 → 2P2O5
Cl2 và Br2 không tác dụng trực tiếp với O2.
Câu 8. C
Hợp chất khí có dạng: RH3
Theo bài ra:
TỰ LUẬN
Câu 1
a. Kẽm tan một phần, có lớp chất rắn màu đỏ bám vào viên kẽm, dung dịch màu xanh nhạt dần.
PTHH: Zn + CuSO4 → ZnSO4 + Cu↓ (0.5 điểm)
b. Kẽm tan và có sủi bọt khí.
PTHH: Zn + 2HCl → ZnCl2 + H2↑ (0.5 điểm)
Câu 2
- Lấy mỗi lọ 1 ít dung dịch làm mẫu thử. Cho quỳ tím lần lượt vào từng mẫu thử.
+ Mẫu làm quỳ tím hóa đỏ là dung dịch HCl. (0,25 điểm)
+ Mẫu làm quỳ tím hóa xanh là dung dịch KOH. (0,25 điểm)
+ Mẫu không đổi màu quỳ tím là dung dịch NaNO3 và Na2SO4
- Cho dung dịch BaCl2 lần lượt vào 2 mẫu thử còn lại. (0,25 điểm)
+ Mẫu nào có tạo kết tủa trắng là dung dịch Na2SO4.
PTHH: BaCl2 + Na2SO4 → BaSO4↓ + 2NaCl (0,25 điểm)
+ Mẫu còn lại là NaNO3
Câu 3
a. 2Al + 3Cl2 → 2AlCl3 (0,5 điểm)
b. Cu + 2AgNO3 → Cu(NO3)2 + 2Ag↓ (0,5 điểm)
c. Na2O + H2O → 2NaOH (0,5 điểm)
d. FeCl3 + 3NaOH → Fe(OH)3↓ + 3NaCl (0,5 điểm)
Câu 4
nNa = 2,3/23 = 0,1 (mol)
2Na + 2H2O → 2NaOH + H2
Theo pt: nNaOH = nNa = 0,1 mol ⇒ mNaOH = 0,1. 40 = 4g (0,5 điểm)
nH2 = (1/2) .nH2 = 0,1 : 2 = 0,05 mol ⇒ mH2 = 2. 0,05 = 0,1 g
mdd sau pư = 2,3 + 97,8 – 0,1 = 100g
C% = (mNaOH/mdd).100% = (4/100).100% = 4% (0,5 điểm)
Câu 5
nH2 = 2,24 / 22,4 = 0,1 mol
Zn + H2SO4 → ZnSO4 + H2
Cu không tác dụng với H2SO4 loãng (0,5 điểm)
Theo pt: nZn = nH2 = 0,1 mol
⇒ mZn = 0,1.65 = 6,5 g
⇒ mCu = 10,5 – 6,5 = 4 g
% mZn = (6,5/10,5).100% = 61,9%
% mCu = 100% - 61,9% = 38,1% (0,5 điểm)
Câu 6
X + 2HCl → XCl2 + H2
nH2 = 1,12/22,4 = 0,05 mol (0,5 điểm)
Theo pt: nx = nH2 = 0,05 mol
MX = 3,25/0,05 = 65 g/mol
⇒ X là Zn (0,5 điểm)
Câu 7
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag (0,25 điểm)
1 mol Fe phản ứng tạo thành 2 mol Ag thì khối lượng tăng thêm là: 2.108 – 56 = 160g (0,25 điểm)
Theo bài: m tăng = 57,6 – 56 = 1,6 g
⇒ nFe pư = 1,6/160 = 0,1 mol
nAg = 2.nFe = 0,1.2 = 0,2 mol
mAg = 0,2 .108 = 21,6 g (0,5 điểm)
___________________________________________________________________
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Học kì 1 Hóa học lớp 9 có đáp án - (Đề số 2)
Phần tự luận
Câu 1: (2 điểm) Viết phương trình hóa học của CuO lần lượt với dung dịch HCl, dung dịch H2SO4 loãng.
Câu 2: (2 điểm) Khi điện phân dung dịch NaCl thu được 250g dung dịch NaOH 12%. Tính thể tích khí Cl2 (ở đktc) thu được (Na=23, O=16, H=1).
Câu 3: (2 điểm) Xác định chất X trong sơ đồ chuyển hóa:
X to, O2→ SO2 to, O2→ SO3
Viết phương trình hóa học.
Câu 4: (2 điểm) Khi cho 4,48 lít khí clo (đktc) đủ để tác dụng hết với 88,81 ml dung dịch KBr (D=1,34 g/ml). Phản ứng xảy ra theo phương trình:
Cl2 + 2KBr → 2KCl + Br2
Thể tích dung dịch thay đổi không đáng kể.
Tính nồng độ % của dung dịch KBr (K=39, Br=80).
Câu 5: (2 điểm) Chỉ dùng quỳ tím, hãy phân biệt 3 dung dịch: NaCl, H2SO4 và BaCl2.
Đáp án đề thi Học kì 1 môn Hóa học 9 - Đề số 2
Câu 1:
CuO + 2HCl → CuCl2 + H2O
CuO + H2SO4 → CuSO4 + H2O
Câu 2:
2NaCl + 2H2O đp có mn→ 2NaOH + H2 + Cl2
nNaOH = 250x12/(100 x 40) = 0,75 mol => nH2 = nCl2 = 0,375 mol
=> VH2 = VCl2 = 0,375 x 22,4 = 8,4 lít
Câu 3:
X là lưu huỳnh
S + O2 to,xt→ SO2
2SO2 + O2 to,xt→ 2SO3
Câu 4:
Cl2 + 2KBr → 2KCl + Br2
nCl2 = 0,2 mol => KBr = 0,4 mol
=> mKBr = 119 x 0,4 = 47,6 gam.
Khối lượng dung dịch KBr = 88,8 x 1,34 = 118,992 gam.
Câu 5:
Dung dịch làm quỳ tím hóa đỏ là H2SO4.
Dùng dung dịch H2SO4 nhận ra dung dịch BaCl2 do tạo kết tủa trắng.
H2SO4 + BaCl2 → BaSO4↓ + 2HCl.
Dung dịch NaCl không có hiện tượng gì.
___________________________________________________________________
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Học kì 1 Hóa học lớp 9 có đáp án - (Đề số 3)
Phần tự luận
Câu 1: (2 điểm) Lấy một thí dụ cho mỗi loại phản ứng sau:
a) Loại phản ứng trao đổi
b) Loại phản ứng thay thế
c) Loại phản ứng hóa hợp
d) Loại phản ứng trung hòa
Câu 2: (2 điểm) Gọi x, y lần lượt là số mol của NaOH và HCl.
Trộn 2 dung dịch NaOH và HCl trên với nhau, tạo ra dung dịch có pH=7.
Tìm biểu thức liên hệ giữa x và y.
Câu 3: (2 điểm) Có thể dùng hóa chất nào để phân biệt dung dịch HCl với dung dịch H2SO4 loãng?
Câu 4: (2 điểm) Hoàn thành phương trình phản ứng hóa học sau:
FexOy + CO to→ (M) + (N)
Câu 5: (2 điểm) Ống nghiệm (1) chứa 2ml dung dịch HCl 1M. Ống nghiệm (2) chứa 2ml dung dịch H2SO4 1M. Cho Zn dư vào hai dung dịch axit trên thì thể tích khí hidro thu được từ ống nghiệm (1) và (2) tương ứng là V1 và V2 đo ở cùng điều kiện. viết phương trình hóa học. So sánh V1 và V2.
Đáp án đề thi Học kì 1 môn Hóa học 9 - Đề số 3
Câu 1:
a) Ví dụ về loại phản ứng trao đổi: HCl + AgNO3 → AgCl↓ + HNO3
b) Ví dụ về loại phản ứng thay thế: Fe + CuSO4 → Cu + FeSO4
c) Ví dụ về loại phản ứng hóa hợp: Cl2 + H2 to→ 2HCl
d) Ví dụ về loại phản ứng trung hòa: NaOH + HCl → NaCl + H2O
Câu 2:
pH = 7 thì dung dịch trung tính và ngược lại.
=> NaOH và HCl vừa hết.
NaOH + HCl → NaCl + H2O
Nghĩa là: nNaOH = nHCl => x = y.
Câu 3:
Có thể dùng dung dịch Ba(OH)2 để phân biệt H2SO4 và HCl.
Trường hợp nào có kết tủa trắng xuất hiện là H2SO4; không có hiện tượng gì là HCl
Ba(OH)2 + H2SO4 → BaSO4↓trắng + 2H2O
Ba(OH)2 + 2HCl → BaCl2 + 2H2O
Câu 4:
FexOy + yCO to→ xFe + yCO2
Câu 5:
Zn + 2HCl → ZnCl2 + H2 (1)
Zn + H2SO4 → ZnSO4 + H2 (2)
nHCl = 0,002 => nH2 (1) = 0,001 mol => V1 = 0,001 x 22,4 = 0,0224 lít
nH2SO4 = 0,002 => nH2 (2) = 0,002 mol => V2 = 0,002 x 22,4 = 0,0448 lít
=> V2 = 2V1.
___________________________________________________________________
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Học kì 1 Hóa học lớp 9 có đáp án - (Đề số 4)
Phần trắc nghiệm (4 điểm: mỗi câu 0,5 điểm)
Câu 1: Ngâm hỗn hợp gồm các kim loại Al, Cu, Fe trong dung dịch AgNO3 (dư). Người ta thu được
A. Cu
B. Ag
C. Fe
D. cả Cu lẫn Ag
Câu 2: Công thức oxit cao nhất của 3 nguyên tố P, S, Cl là
A. P2O3, SO3, Cl2O7
B. P2O5, SO3, Cl2O5
C. P2O5, SO2, Cl2O5
D. P2O5, SO3, Cl2O7
Câu 3: Khi Fe tác dụng với dung dịch H2SO4 loãng, sản phẩm của phản ứng là
A. FeSO4
B. Fe2(SO4)3
C. FeSO4 và H2
D. Fe2(SO4)2 và SO2
Câu 4: Có các chất: brom, iot, clo, nito, oxi. Phi kim ở trang thái khí, khi ẩm có tính tẩy màu là
A. brom
B. oxi
C. clo
D. iot
Câu 5: Kim loại nào sau đây tan được trong dung dịch NaOH?
A. Ag
B. Fe
C. Cu
D. Al
Câu 6: Một quá trình không sinh ra khí CO2 là
A. đốt cháy khí đốt tự nhiên
B. sản xuất vôi sống
C. sự hô hấp
D. sự vôi tôi
Câu 7: Khi cho KMnO4, MnO2 (số mol bằng nhau) lần lượt tác dụng hết với dung dịch HCl thu được khí clo có thể tích tương ứng là V1 và V2 (đktc). Biểu thức liên hệ giữa V1 và V2 là
A. V1 = 2,5V2
B. V1 = V2
C. V1 = 1,5V2
D. V1 = 0,5V2
Câu 8: Cho 1,008 m3 (đktc) hỗn hợp khí Co và H2 khử hoàn toàn Fe2O3 ở nhiệt độ thích hợp. Khối lượng sắt thu được sẽ là (Fe=56)
A. 0,84kg
B. 2,52kg
C. 5,04kg
D. 1,68kg
Phần tự luận
Câu 9: (2 điểm) Có 4 lọ đựng 4 khí riêng biệt: oxi, hidro, clo và cacbon đioxit. Hãy nhận biết mỗi khí.
Câu 10: (2 điểm) Viết phương trình hóa học biểu diễn những chuyển đổi hóa học sau:
Fe2O3 (1)→ Fe (2)→ FeCl3 (3)→ Fe(OH)3 (4)→ Fe(NO3)3.
Câu 11: (2 điểm) Nguyên tố R có công thức oxit là RO3. Trong RO3 oxi chiếm 60% về khối lượng.
a) Xác định tên nguyên tố R.
b) Cho biết tính chất hóa học cơ bản của R.
Viết phương trình hóa học để minh họa (O=16, S=32, Fe=56, Se=79).
Đáp án đề thi Học kì 1 môn Hóa học 9 - Đề số 4
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Đáp án | B | D | C | C | D | D | A | D |
Câu 1:B
Al, Cu, Fe hoạt động mạnh hơn Ag đẩy được Ag ra khỏi dung dịch AgNO3.
Do AgNO3 dư nên Al, Cu, Fe tan hết. Chỉ thu được Ag.
Câu 2:D
Công thức oxit cao nhất của 3 nguyên tố P, S, Cl là P2O5, SO3, Cl2O7.
Câu 3:C
Fe + H2SO4 → FeSO4 + H2
Câu 4:C
Các chất: brom, iot, clo, nito, oxi.
Chỉ có clo là phi kim ở trạng thái khí, khi ẩm có tính tẩy màu.
Câu 5:D
Chỉ có Al tan được trong dung dịch NaOH (SGK, trang 56)
Câu 6:D
Phương trình hóa học của sự tôi vôi: CaO + H2O → Ca(OH)2.
Không sinh ra khí CO2.
Câu 7:A
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O (1)
MnO2 + 4HCl to→ MnCl2 + Cl2 + 2H2O (2)
Tỉ lệ số mol Cl2 tạo ra ở phương trình (1) so với phương trình (2) là 2,5: 1 khi số mol KMnO4, MnO2 bằng nhau.
Câu 8:D
Đổi 1,008 m3 = 1008 dm3 =1008 lít.
3CO + Fe2O3 to→ 2Fe + 3CO2 (1)
3H2 + Fe2O3 to→ 2Fe + 3H2O (2)
Theo phương trình (1), (2):
Khối lượng sắt thu được = 30 x 56 = 1680 gam hay 1,68kg.
Câu 9:
Đánh số thứ tự từng lọ chứa khí.
Dẫn lần lượt từng khí vào ống nghiệm đựng dung dịch nước vôi trong, khí làm đục dung dịch nước vôi là khí CO2.
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Dẫn các khí còn lại qua mẩu giấy màu ẩm, khí nào làm mất màu giấy là khí Clo.
Cho que đóm còn tàn đỏ vào lọ đựng hai khí còn lại, Khí làm que đóm bùng cháy là khí oxi.
Khí còn lại làm que đóm tắt là hiđro.
Câu 10:
3CO + Fe2O3 to→ 2Fe + 3CO2
2Fe + 3Cl2 to→ 2FeCl3
FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
Fe(OH)3 + 3HNO3 → Fe(NO3)3 + 3H2O
Câu 11:
% về khối lượng O = 60%
Ta có:
→ R là lưu huỳnh.
Lưu huỳnh là một phi kim hoạt động trung bình.
Tác dụng với oxi tạo oxit axit. Ví dụ:
S + O2 → SO2
Tác dụng với kim loại cho muối. Ví dụ:
Fe + S → FeS
Tác dụng với H2. Ví dụ:
H2 + S → H2S.
___________________________________________________________________
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Học kì 1 Hóa học lớp 9 có đáp án - (Đề số 5)
Câu 1: (2.0 điểm)
a. Trình bày tính chất hóa học của axit. Viết phương trình hóa học minh họa.
b. Hãy giải thích vì sao trong bất cứ hoàn cảnh nào cũng không được cho axit đậm đặc vào nước.
Câu 2: (2.0 điểm)
Phân biệt các dung dịch sau bằng phương pháp hóa học:
a. HNO3, HCl, BaCl2, NaOH
b. Al, Fe, Cu
Câu 3: (1.0 điểm)
Hoàn thành chuỗi phản ứng sau:
Na → NaOH → Na2CO3 → Na2SO4 → NaCl
Câu 4: (2.0 điểm)
Sau một lần đi tham quan nhà máy, khi về lớp làm bài tập tường trình thầy giáo có đặt ra một câu hỏi thực tế: "Khí SO2 và CO2 do nhà máy thải ra gây ô nhiễm không khí rất nặng. Vậy em hãy nêu lên cách để loại bỏ bớt lượng khí trên trước khi thải ra môi trường". Bạn Ân cảm thấy rất khó và không biết cách trả lời em hãy hỗ trợ bạn ấy để giải quyết câu hỏi này.
Câu 5: (3.0 điểm)
Biết 2,24 lít khí Cacbonic (đktc) tác dụng hết với 200 ml dung dịch Ba(OH)2, sản phẩm thu được là muối trung hòa và nước.
a. Viết phương trình xảy ra.
b. Tính nồng độ mol của dung dịch Ba(OH)2 cần dùng.
c. Tính khối lượng kết tủa thu được
Đáp án đề thi Học kì 1 môn Hóa học 9 - Đề số 5
Câu 1
a. TCHH của axit:
- Axit làm đổi màu quỳ tím thành màu đỏ. (0.25 điểm)
- Axit tác dụng với oxit bazơ tạo thành muối và nước. (0.25 điểm)
H2SO4 + CaO → CaSO4 + H2O
- Axit tác dụng với bazo tạo thành muối và nước. (0.25 điểm)
H2SO4 + Ca(OH)2 → CaSO4 + 2H2O
- Axit tác dụng với kim loại tạo thành muối và giải phóng khí hidro. (0.25 điểm)
Fe + 2HCl → FeCl2 + H2
- Axit tác dụng với muối tạo thành muối mới và axit mới.
H2SO4 + BaCl2 → BaSO4 + 2HCl (0.25 điểm)
b. Khi axit gặp nước sẽ xảy ra quá trình hidrat hóa, đồng thời sẽ tỏa ra 1 lượng nhiệt lớn. Axit đặc lại nặng hơn nước nên khi cho nước vào axit thì nước sẽ nổi lên trên mặt axit, nhiệt tỏa ra làm cho nước sôi mãnh liệt và bắn tung tóe gây nguy hiểm. (0.75 điểm)
Nếu TCHH không có phương trình thì sẽ không chấm điểm phần đó.
Câu 2 (2 điểm)
a. Trích mẫu thử và đánh số thứ tự:
- Nhúng quỳ tím vào 4 mẫu thử:
+ 2 mẫu làm quỳ chuyển đỏ là HNO3 và HCl
+ Mẫu làm quỳ chuyển xanh là NaOH
+ Mẫu không làm quỳ chuyển màu là là BaCl2
- Nhỏ dd AgNO3 lần lượt vào 2 mẫu HNO3 và HCl
+ Mẫu có kết tủa trắng là HCl
AgNO3 + HCl → AgCl↓ + HNO3
+ Mẫu không có hiện tượng gì là HNO3
b, Trích mẫu thử và đánh số thứ tự
- Lần lượt cho dung dịch axit loãng HCl vào từng mẫu thử
+ Mẫu kim loại nào không tan là Cu.
+ Mẫu kim loại nào tan có hiện tượng sủi bọt khí không màu không mùi là Al, Fe
2Al + 6HCl → 2AlCl3 + 3H2
Fe + 2HCl → FeCl2 + H2
- Cho dung dịch NaOH vào 2 kim loại còn lại: Al, Fe
Kim loại nào có hiện tượng sủi bọt khí không màu không mùi là Al, không có hiện tượng gì là Fe
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
Câu 3
2Na + 2H2O → 2NaOH + H2 (0.25 điểm)
2NaOH + CO2 → Na2CO3 + H2O (0.25 điểm)
Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2 (0.25 điểm)
Na2SO4 + BaCl2 → 2NaCl + BaSO4↓ (0.25 điểm)
Câu 4 (2 điểm)
Trước khi thải phải có hệ thống lọc khí chứa Ca(OH)2 đề hấp thụ khí thải:
Ca(OH)2 + CO2 → CaCO3↓ + H2O
Ca(OH)2 + SO2 → CaSO3↓ + H2O
Câu 5
a. Ba(OH)2 + CO2 → BaCO3 + H2O (1 điểm)
b. nCO2 = 2,24 / 22,4 = 0,1 mol (1 điểm)
Theo pt: nBa(OH)2 = nBaCO3 = nCO2 = 0,1 mol
Vdd = 200ml = 0,2 l
CMBa(OH)2 = n/V = 0,1 / 0,2 = 0,5 M
c. mBaCO3 = 0,1 . 197 = 19,7g (1 điểm)
___________________________________________________________________
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Học kì 1 Hóa học lớp 9 có đáp án - (Đề số 6)
Cho biết nguyên tử khối (theo đvC) của các nguyên tố:
Fe = 56; Cu = 64; S = 32; H = 1; O = 16; Zn = 65; Ag = 108; N = 14; Ba = 137; Cl = 35,5
Phần trắc nghiệm
Câu 1. Phương trình hóa học nào sau đây không đúng?
A. 2Fe + 3Cl2 → 2FeCl3
B. 2CO2 + Ca(OH)2 → Ca(HCO3)2
C. 2NaCl + H2SO4 → Na2SO4 + 2HCl
D. Fe + CuSO4 → FeSO4 + Cu
Câu 2. Ngâm một lá Zn dư vào 200 ml dung dịch AgNO3 1M. Khi phản ứng kết thúc khối lượng Ag thu được là:
A. 6,5 gam
B. 10,8 gam
C. 13 gam
D. 21,6 gam
Câu 3. Có các chất đựng riêng biệt trong mỗi ống nghiệm sau đây: Al, Fe, CuO, CO2, FeSO4, H2SO4. Lần lượt cho dung dịch NaOH vào mỗi ống nghiệm trên. Dung dịch NaOH phản ứng với:
A. Al, CO2, FeSO4, H2SO4
B. Fe, CO2, FeSO4, H2SO4
C. Al, Fe, CuO, FeSO4
D. Al, Fe, CO2, H2SO4
Câu 4. Kim loại X có những tính chất hóa học sau:
- Phản ứng với oxit khi nung nóng.
- Phản ứng với dung dịch AgNO3.
- Phản ứng với dung dịch H2SO4 loãng giải phóng khí H2 và muối của kim loại hóa trị II. Kim loại X là:
A. Cu
B. Fe
C. Al
D. Na.
Phần tự luận
Câu 5 (3đ). Viết phương trình hóa học hoàn thành chuỗi biến hóa sau, ghi rõ điều kiện (nếu có)
Al -1→ Fe -2→ FeCl3 -3→ Fe(OH)3 -4→ Fe2O3
Câu 6 (2đ) . Bằng phương pháp hóa học nhận biết các dung dịch sau: NaOH, H2SO4, Na2SO4, HCl. Viết phương trình hóa học (nếu có).
Câu 7 (3đ) . Cho m gam hỗn hợp X gồm Fe và Cu vào dung dịch H2SO4 loãng, dư thu được 4,48 lít khí (đktc) và thấy còn 8,8 gam chất rắn không tan. Lấy phần chất rắn không tan ra thu được 250 ml dung dịch Y.
a. Xác định phần trăm về khối lượng các chất trong X.
b. Dung dịch Y tác dụng vừa đủ với BaCl2 thu được 69,9 gam kết tủa. Tính nồng độ mol các chất trong Y.
c. Nếu cho 12 gam X vào 300 ml dung dịch AgNO3 0,8M. Sau một thời gian thu được 28 gam chất rắn Z. Tính khối lượng của Ag có trong Z?
Đáp án đề thi Học kì 1 môn Hóa học 9 - Đề số 6
Trắc nghiệm (2,0 điểm). Mỗi câu trả lời đúng được 0,5 điểm
Câu 1. C
Dung dịch NaCl không phản ứng với dung dịch H2SO4.
Câu 2. D
mAg = 0,2.108 = 21,6 gam.
Câu 3. A
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
CO2 + 2NaOH → Na2CO3 + 2H2O
FeSO4 + 2NaOH → Fe(OH)2 + Na2SO4
H2SO4 + 2NaOH → Na2SO4 + 2H2O
Câu 4. B
3Fe + 2O2 → Fe3O4
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Fe + H2SO4 → FeSO4 + H2
Tự luận
Câu 5
Viết đúng mỗi phương trình hóa học được (0.5 điểm); cân bằng đúng mỗi phương trình được (0.25 điểm)
(1) 2Al + 3FeCl2 → 2AlCl3 + 3Fe (0.75 điểm)
(2) 2Fe + 3Cl2 → 2FeCl3 (0.75 điểm)
(3) FeCl3 + 3KOH → Fe(OH)3 + 3KCl (0.75 điểm)
(4) 2Fe(OH)3 → Fe2O3 + 3H2O (0.75 điểm)
Chú ý: Học sinh có thể viết PTHH khác đúng vẫn cho điểm tối đa
Câu 6
Học sinh trình bày được cách nhận biết và viết được PTHH (nếu có) đúng mỗi dung dịch được 0,5 điểm.
Trích mẫu thử và đánh số thứ tự:
- Nhúng quỳ tím vào 4 mẫu thử:
+ 2 mẫu làm quỳ chuyển đỏ là H2SO4 và HCl
+ Mẫu làm quỳ chuyển xanh là NaOH
+ Mẫu không làm quỳ chuyển màu là là Na2SO4
- Nhỏ dd BaCl2 lần lượt vào 2 mẫu H2SO4 và HCl
+ Mẫu có kết tủa trắng là H2SO4
BaCl2 + H2SO4 → BaSO4↓ + 2HCl
+ Mẫu còn lại là HCl
Câu 7
- Theo giả thiết ta có:
nH2 = 4,48/22,4 = 0,2 mol (0.25 điểm)
- Phương trình hóa học: Fe + H2SO4 → FeSO4 + H2 (1) (0.25 điểm)
Theo PTHH (1) ta có: nFe = nH2 = 0,2 mol
⇒ mFe = 0,2.56 ⇒ mFe = 11,2 (gam)
Suy ra, giá trị m là: m = 11,2 + 8,8 ⇒ m = 20 (gam) (0.5 điểm)
a. Vậy thành phần phần trăm về khối lượng các chất trong X là:
%mFe = (11.2/20).100 = 56%
và %mCu = 100 - 56 = 44% (0.5 điểm)
b. Theo bài ra dung dịch Y gồm FeSO4 và H2SO4 dư
Phương trình hóa học:
BaCl2 + FeSO4 → BaSO4 + FeCl2 (2)
BaCl2 + H2SO4 → BaSO4 + 2HCl (3) (0.5 điểm)
Theo giả thiết, ta có:
nBaSO4 = 69,9/233 ⇒ nBaSO4 = 0,3 mol
Khi đó theo PTHH (1), (2), (3) ta có:
nFeSO4(Y) = 0,2 mol và nH2SO4(Y) = 0,1 mol (0.25 điểm)
Vậy nồng độ mol các chất trong Y là:
CM FeSO4 = 0,2/0,25 = 0,8 M
Và CM H2SO4 = 0,1/0,25 = 0,4 M (0.25 điểm)
c. Theo giả thiết và kết quả ở phần (a) ta có:
Trong 20 gam X có 0,2 mol Fe và 0,1375 mol Cu
Vậy trong 12 gam X có 0,12 mol Fe và 0,0825 mol Cu
Và nAgNO3 = 0,3.0,8 = 0,24 mol (0.25 điểm)
- Phương trình hóa học có thể:
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag (4)
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag (5)
Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag (6)
Giả sử chỉ xảy ra phản ứng (4) và phản ứng (4) diễn ra hoàn toàn:
Chất rắn sau phản ứng gồm Ag: 0,24 mol và Cu 0,0825 mol
mchất rắn = 0,24.108 + 0,0825.64 = 31,2 > mZ = 28.
Vậy điều giả sử là sai. Sau một thời gian để thu được 28 gam chất rắn Z phản ứng (4) mới diễn ra 1 phần. Gọi số mol Fe phản ứng trong (4) là x mol. Ta có:
Sau một thời gian, thu được chất rắn Z gồm: Fe: (0,12 – x) mol; Ag: 2x mol; Cu: 0,0825 mol
Có mZ = 28 gam
→ 56(0,12 – x) + 108.2x + 64.0,0825 = 28 → x = 0,1.
Vậy số mol Ag có trong Z là 0,2 mol.
Khối lượng Ag có trong Z là 0,2.108 = 21,6 gam. (0.25 điểm)
Chú ý: Học sinh có thể không cần viết đủ cả 3 PTHH (4), (5), (6) nhưng có cách trình bày đúng để tìm được khối lượng của Ag trong Z là 21,6 gam thì vẫn đạt 0,25 điểm.
___________________________________________________________________
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Học kì 1 Hóa học lớp 9 có đáp án - (Đề số 7)
Phần trắc nghiệm
Câu 1: Dãy chất gồm các oxit bazơ là:
A. CuO, NO, MgO, CaO.
B. CuO, CaO, MgO, Na2O.
C. CaO, CO2, K2O, Na2O.
D. K2O, FeO, P2O5, Mn2O7.
Câu 2: Chất nào sau đây góp phần nhiều nhất vào sự hình thành mưa axit ?
A . CO2
B. SO2
C. N2
D. O3
Câu 3: Cho 0,1 mol kim loại kẽm vào dung dịch HCl dư. Khối lượng muối thu được là:
A. 20,4
B. 1,36 g
C. 13,6 g
D. 27,2 g
Câu 4: Phản ứng nào dưới đây là phản ứng trao đổi ?
A. 2Na + 2H2O → 2NaOH + H2
B. BaO + H2O → Ba(OH)2
C. Zn + H2SO4 → ZnSO4 + H2
D. BaCl2 + H2SO4 → BaSO4 + 2HCl
Câu 5: Khi thả một cây đinh sắt sạch vào dung dịch CuSO4 loãng, có hiện tượng sau:
A. Sủi bọt khí, màu xanh của dung dịch nhạt dần.
B. Có một lớp đồng màu đỏ phủ lên đinh sắt, màu xanh của dung dịch đậm dần.
C. Có một lớp đồng màu đỏ phủ lên đinh sắt, dung dịch không đổi màu.
D. Có một lớp đồng màu đỏ phủ lên đinh sắt, màu xanh của dung dịch nhạt dần
Câu 6: Có một mẫu Fe bị lẫn tạp chất là nhôm, để làm sạch mẫu sắt này bằng cách ngâm nó với:
A. Dung dịch NaOH dư
B. Dung dịch H2SO4 loãng
C. Dung dịch HCl dư
D. Dung dịch HNO3 loãng
Câu 7: Dãy phi kim tác dụng với oxi tạo thành oxit axit là:
A. S, C, P.
B. S, C, Cl2.
C. C, P, Br2.
D. C, Cl2, Br2.
Câu 8: X là nguyên tố phi kim có hoá trị III trong hợp chất với khí hiđro. Biết thành phần phần trăm khối lượng của hiđro trong hợp chất là 17,65%. X là nguyên tố:
A. C
B. S
C. N
D. P
Phần tự luận
Câu 1: (1 điểm). Hãy cho biết hiện tượng xảy ra khi nhúng một viên kẽm vào:
a. Dung dịch CuSO4
b. Dung dịch HCl
Câu 2: (1 điểm). Bằng phương pháp hóa học hãy nhận biết dung dịch các chất chứa trong các lọ bị mất nhãn sau: HCl, KOH, NaNO3, Na2SO4
Câu 3: (2 điểm). Hãy lập phương trình hóa học của các phản ứng sau:
a. Al + Cl2 →
b. Cu + AgNO3 →
c. Na2O + H2O →
d. FeCl3 + NaOH →
Câu 4: (1 điểm). Hoà tan hết 2,3g Na kim loại vào 97,8g nước . Hãy tính nồng độ % của dung dịch thu được sau phản ứng?
Câu 5: (1 điểm). Cho 10,5g hỗn hợp 2 kim loại Cu và Zn vào dd H2SO4 loãng dư, người ta thu được 2,24 lít khí (đktc). Hãy tính thành phần % theo khối lượng của Cu và Zn .
Câu 6: (1 điểm). Hoà tan hoàn toàn 3,25g một kim loại X (hoá trị II) bằng dung dịch HCl thu được 1,12 lít khí H2 (ở đktc). Hãy xác định tên kim loại X ?
Câu 7: (1 điểm). Ngâm lá sắt có khối lượng 56 gam vào dung dịch AgNO3, sau một thời gian lấy lá sắt ra rửa nhẹ cân được 57,6 gam. Hãy tính khối lượng Ag sinh ra sau phản ứng?
( Cho: N = 14, Na = 23, Cu = 64, Zn = 65, Ag = 108, O = 16 )
Đáp án đề thi Học kì 1 môn Hóa học 9 - Đề số 7
TRẮC NGHIỆM: (2 điểm)
Chọn đúng mỗi câu được 0,25đ
Câu 1. B
Oxit bazo là oxit của kim loại
Câu 2. B
SO2 góp phần gây nên mưa axit.
Câu 3. C
mmuối = 0,1.136 = 13,6 gam.
Câu 4. D
Phản ứng trao đổi: BaCl2 + H2SO4 → BaSO4 + 2HCl
Câu 5. D
Fe + CuSO4 → FeSO4 + Cu
Có một lớp đồng màu đỏ phủ lên đinh sắt, màu xanh của dung dịch nhạt dần
Câu 6. A
Al tác dụng với NaOH còn Fe thì không.
Câu 7. A
S + O2 → SO2
C + O2 → CO2
4P + 5O2 → 2P2O5
Cl2 và Br2 không tác dụng trực tiếp với O2.
Câu 8. C
Hợp chất khí có dạng: RH3
Theo bài ra:
TỰ LUẬN
Câu 1
a. Kẽm tan một phần, có lớp chất rắn màu đỏ bám vào viên kẽm, dung dịch màu xanh nhạt dần.
PTHH: Zn + CuSO4 → ZnSO4 + Cu↓ (0.5 điểm)
b. Kẽm tan và có sủi bọt khí.
PTHH: Zn + 2HCl → ZnCl2 + H2↑ (0.5 điểm)
Câu 2
- Lấy mỗi lọ 1 ít dung dịch làm mẫu thử. Cho quỳ tím lần lượt vào từng mẫu thử.
+ Mẫu làm quỳ tím hóa đỏ là dung dịch HCl. (0,25 điểm)
+ Mẫu làm quỳ tím hóa xanh là dung dịch KOH. (0,25 điểm)
+ Mẫu không đổi màu quỳ tím là dung dịch NaNO3 và Na2SO4
- Cho dung dịch BaCl2 lần lượt vào 2 mẫu thử còn lại. (0,25 điểm)
+ Mẫu nào có tạo kết tủa trắng là dung dịch Na2SO4.
PTHH: BaCl2 + Na2SO4 → BaSO4↓ + 2NaCl (0,25 điểm)
+ Mẫu còn lại là NaNO3
Câu 3
a. 2Al + 3Cl2 → 2AlCl3 (0,5 điểm)
b. Cu + 2AgNO3 → Cu(NO3)2 + 2Ag↓ (0,5 điểm)
c. Na2O + H2O → 2NaOH (0,5 điểm)
d. FeCl3 + 3NaOH → Fe(OH)3↓ + 3NaCl (0,5 điểm)
Câu 4
nNa = 2,3/23 = 0,1 (mol)
2Na + 2H2O → 2NaOH + H2
Theo pt: nNaOH = nNa = 0,1 mol ⇒ mNaOH = 0,1. 40 = 4g (0,5 điểm)
nH2 = (1/2) .nH2 = 0,1 : 2 = 0,05 mol ⇒ mH2 = 2. 0,05 = 0,1 g
mdd sau pư = 2,3 + 97,8 – 0,1 = 100g
C% = (mNaOH/mdd).100% = (4/100).100% = 4% (0,5 điểm)
Câu 5
nH2 = 2,24 / 22,4 = 0,1 mol
Zn + H2SO4 → ZnSO4 + H2
Cu không tác dụng với H2SO4 loãng (0,5 điểm)
Theo pt: nZn = nH2 = 0,1 mol
⇒ mZn = 0,1.65 = 6,5 g
⇒ mCu = 10,5 – 6,5 = 4 g
% mZn = (6,5/10,5).100% = 61,9%
% mCu = 100% - 61,9% = 38,1% (0,5 điểm)
Câu 6
X + 2HCl → XCl2 + H2
nH2 = 1,12/22,4 = 0,05 mol (0,5 điểm)
Theo pt: nx = nH2 = 0,05 mol
MX = 3,25/0,05 = 65 g/mol
⇒ X là Zn (0,5 điểm)
Câu 7
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag (0,25 điểm)
1 mol Fe phản ứng tạo thành 2 mol Ag thì khối lượng tăng thêm là: 2.108 – 56 = 160g (0,25 điểm)
Theo bài: m tăng = 57,6 – 56 = 1,6 g
⇒ nFe pư = 1,6/160 = 0,1 mol
nAg = 2.nFe = 0,1.2 = 0,2 mol
mAg = 0,2 .108 = 21,6 g (0,5 điểm)
- Bộ 5 đề kiểm tra tự biên soạn có đáp án và thang điểm chi tiết:
___________________________________________________________________
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Học kì 1 Hóa học lớp 9 có đáp án - (Đề số 8)
Phần tự luận
Câu 1: (2 điểm) Từ MnO2, dung dịch HCl, KClO3 và cacbon, viết phương trình hóa học để điều chế các khí: clo, oxi, cacbon đioxit.
Câu 2: (2 điểm) Tính thể tích khí oxi thu được (đktc) khi nhiệt phân 15,8g KMnO4 với hiệu suất 85% (K=39, Mn=55, O=16).
Câu 3: (2 điểm) Cho m gam SO3 vào 20g dung dịch H2SO4 10% tạo ra dung dịch H2SO4 20%.
a) Viết phương trình hóa học của SO3 với H2O.
b) Tìm giá trị của m (H=1, O=16, S=32).
Câu 4: (2 điểm) Cho hỗn hợp gồm Fe, Mg có khối lượng 8g tác dụng hết với dung dịch HCl thu được 4,48 lít khí H2 (đktc).
a) Viết phương trình hóa học của Fe và Mg với dung dịch HCl.
b) Tính tỉ lệ theo số mol của Fe và của Mg trong hỗn hợp ban đầu (Fe=56, Mg=24)
Câu 5: (2 điểm) Cho luồng khí clo (dư) tác dụng với 9,2g kim loại hóa trị I, tạo ra 23,4 g muối. Xác định tên kim loại (Na=23, Ag=108, Li=7, K=39, Cl=35,5).
Đáp án đề thi Học kì 1 môn Hóa học 9 - Đề số 8
Câu 1:
Điều chế clo: MnO2 + 4HCl to→ MnCl2 + Cl2 + 2H2O
Điều chế oxi: 2KClO3 to→ 2KCl + 3O2
Điều chế CO2: C + O2 to→ CO2
Câu 2:
2KMnO4 to→ K2MnO4 + MnO2 + O2
nKMnO4 = 15,8/158 = 0,1 mol
Theo PTHH có: nO2 = 1/2 nKMnO4 = 0,05 mol
Mà hiệu suất phản ứng là 85% nên số mol Oxi thu được là:
nO2 = 0,05 x 0,85 = 0,0425 mol.
Thể tích khí oxi thu được (đktc): 0,0425 x 22,4 = 0,952 lít.
Câu 3:
Câu 4:
Fe + 2HCl → FeCl2 + H2
Mg + 2HCl → MgCl2 + H2
Gọi x, y lần lượt là số mol của Fe, Mg
Ta có: 56x + 24y = 8
nH2 = x+y = 4,48/22,4 = 0,2 mol.
Giải ta được x = y = 0,1.
Câu 5:
2M + Cl2 to→ 2MCl
Ta có: 9,2/M = 23,4/(M+35,5) => M = 23 (Na).
___________________________________________________________________
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Học kì 1 Hóa học lớp 9 có đáp án - (Đề số 9)
Phần trắc nghiệm
Câu 1: Axit làm quỳ tím hóa
A. Xanh
B. đỏ
C. Hồng
D. Vàng
Câu 2: Bazơ nào sau đây không tan trong nước.
A. NaOH
B. KOH
C. Ca(OH)2
D. Cu(OH)2
Câu 3: Muối nào sau đây không tan.
A. K2SO3
B. Na2SO3
C CuCl2
D BaSO4
Câu 4: Axit nào sau đây dễ bay hơi.
A. H2SO3
B. H2SO4
C. HCl
D. HNO3
Câu 5: Cho 5,6g sắt vào dung dịch đồng sunfat dư. Khối lượng đồng thu được là:
A. 6,4 g
B 12,8 g
C. 64 g
D. 128 g
Câu 6: Cho 2.7g Nhôm vào dung dịch axit clohiđric dư. Thể tích khí hiđrô thoát ra (đktc) là:
A. 3.36 l
B. 2.24 l
C. 6.72 l
D. 4.48 l
Phần tự luận
Câu 1. Hoàn thành chuổi phản ứng hoá học sau:(2.5 đ)
Fe -(1)→ FeCl3 -(2)→ Fe(OH)3 -(3)→ Fe2O3 -(4)→ Fe2(SO4)3
Câu 2. (2đ) Nhận biết các chất sau bằng phương pháp hóa học :
Na2SO4, HCl, H2SO4, NaCl. Viết PTPƯ nếu có:
Câu 3. (3đ) Cho một lượng bột sắt dư vào 200ml dung dịch axit H2SO4. Phản ứng xong thu được 4,48 lít khí hiđrô (đktc)
a. Viết phương trình phản ứng hoá học
b. Tính khối lượng sắt đã tham gia phản ứng
c. Tính nồng độ mol của dung dịch axit H2SO4 đã dùng
Fe = 56, O = 16, H = 1, S = 32
Đáp án đề thi Học kì 1 môn Hóa học 9 - Đề số 9
Trắc nghệm mỗi ý đúng (0.5 điểm)
Câu 1. B
Axit làm quỳ tím chuyển sang màu đỏ.
Câu 2. D
Cu(OH)2 không tan trong nước.
Câu 3. D
BaSO4 kết tủa bền, không tan trong nước.
Câu 4. A
H2SO3 là axit yếu, không bền ở điều kiện thường
H2SO3 → H2O + CO2
Câu 5. A
mCu = 0,1.64 = 6,4 gam.
Câu 6. A
→ V = 0,15.22,4 = 3,36 lít.
Tự Luận
Câu 1. Mỗi PTHH đúng 0,5 đ
(1) 2Fe + 3Cl2 → 2FeCl3
(2) FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
(3) 2Fe(OH)3 → Fe2O3 + 3H2O
(4) Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
Câu 2.
- Cho quỳ tím vào các mẫu thử:
+ Nếu quỳ tím hóa đỏ là: HCl, H2SO4, .. ( nhóm 1) (0.5 điểm)
+ Quỳ tím không chuyển màu là: Na2SO4 , NaCl. ( nhóm 2) (0.5 điểm)
- Cho BaCl2 vào nhóm 1, chất nào xuất hiện kết tủa trắng là: H2 SO4, còn lại là HCl (0.5 điểm)
BaCl2 + H2SO4 BaSO4↓ + HCl (0.5 điểm)
- Cho BaCl2 vào nhóm 2, chất nào xuất hiện kết tủa trắng là: Na2SO4, còn lại là NaCl (0.5 điểm)
BaCl2 + Na2SO4 → BaSO4↓ + NaCl (0.5 điểm)
Câu 3.
a. Fe + H2SO4 → FeSO4 + H2 (0.5 điểm)
b. Số mol của H2 là n = 4,48/22,4 = 0,2 mol (0.5 điểm)
Theo PTHH suy ra nFe = nH2 = 0,2 mol (0.5 điểm)
Khối lương Fe tham gia phả ứng là :
mFe = 0,2.56 = 11,2 gam (0.5 điểm)
c. Số mol của H2SO4 tham gia phản ứng là :
Theo PTHH suy ra nH2SO4 = nH2 = 0,2 mol (0.5 điểm)
VH2SO4 = 200ml = 0,2 l
Nồng độ mol của H2SO4 là:
CM = 0,2/0,2 = 1 M (0.5 điểm)
___________________________________________________________________
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Học kì 1 Hóa học lớp 9 có đáp án - (Đề số 10)
Phần tự luận
Câu 1: (2 điểm) Viết phương trình hóa học chứng tỏ khi sục khí Cl2 vào nước, nước clo có tính tẩy màu.
Câu 2: (2 điểm) Cho 1 lít hỗn hợp các khí H2, Cl2 đi qua dung dịch Ca(OH)2 dư, còn lại một chất khí có thể tích là 0,5 lít (đo ở cùng điều kiện).
Tính thành phần % theo thể tích của clo trong hỗn hợp ban đầu.
Câu 3: (2 điểm) Rắc bột nhôm đun nóng vào lọ chứa khí Cl2. Thu được 0,1 mol muối và Al còn dư. Hỗn hợp sau phản ứng cho tác dụng với dung dịch HCl (dư) thấy có tạo ra 3,36 lít khí H2 (đktc).
Xác định tỉ lệ % lượng Al tác dụng với clo so với lượng Al ban đầu.
Câu 4: (2 điểm) Sục khí CO2 vào lượng dư nước vôi trong, sau đó nhỏ tiếp dung dịch HCl vào. Mô tả hiện tượng quan sát được.
Câu 5: (2 điểm) Cho hỗn hợp gồm Fe, Fe2O3 tác dụng với dung dịch Hcl thu được 4,48 lít khí (đktc) và một dung dịch có chứa 57,9g hỗn hợp 2 muối.
Tính khối lượng mỗi muối (Fe=56, Cl=35,5, Al=27).
Đáp án đề thi Học kì 1 môn Hóa học 9 - Đề số 10
Câu 1:
Cl2 + H2O ⇋ HCl + HClO
Nước Clo là dung dịch hỗn hợp các chất: Cl2; HCl; HClO nên có màu vàng lục, mùi hắc của khí Clo. Lúc đầu dung dịch axit làm quỳ tím hóa đỏ, nhưng nhanh chóng mất màu do tác dụng oxi hóa mạnh của HClO.
Câu 2:
H2, Cl2 đi qua dung dịch Ca(OH)2 lấy dư, Cl2 bị giữ lại chỉ có H2 thoát ra.
VH2 = 0,5 lít => Thành phần % theo thể tích của clo: 50%.
Câu 3:
Hỗn hợp sau phản ứng gồm Al dư và AlCl3. Cho vào HCl có phản ứng:
2Al + 6HCl → 2AlCl3 + 3H2
Số mol H2 = 3,36/22,4 = 0,15 mol
→ Số mol Al tác dụng với HCl: 0,1 mol.
→ Số mol Al ban đầu là: 0,1 + 0,1 = 0,2 mol
Tỉ lệ % lượng Al tác dụng với Clo so với lượng Al ban đầu là:
Câu 4:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Ca(OH)2 + 2HCl → CaCl2 + 2H2O
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Hiện tượng:
- Xuất hiện kết tủa.
- Sủi bọt và kết tủa tan ra.
Câu 5:
Fe + 2HCl → FeCl2 + H2
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
nH2 = 4,48/22,4 = 0,2 mol => nFeCl2= 0,2 mol
=> mFeCl2 = 0,2 x 127 = 25,4 gam
mFeCl3 = 57,9 – 25,4 = 32,5 gam.
___________________________________________________________________
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Học kì 1 Hóa học lớp 9 có đáp án - (Đề số 11)
(Cho C = 12, O = 16, H = 1, Na = 23, K = 39, Mg = 24, Ca = 40, P = 31, Cl = 35,5,
F = 19, Si = 27, N = 14, S = 32)
I - TRẮC NGHIỆM (7 Điểm)
Câu 1: Sắt(III) oxit (Fe2O3) tác dụng được với:
A. Nước, sản phẩm là axit
B. Bazơ, sản phẩm là muối và nước
C. Nước, sản phẩm là bazơ
D. Axit, sản phẩm là muối và nước
Câu 2: Cho các oxit axit sau: CO2; SO3; N2O5; P2O5. Dãy axit tương ứng với các oxit axit trên là:
A. H2SO3, H2SO3, HNO3, H3PO4
B. H2CO3, H2SO4, HNO2, H3PO4
C. H2CO3, H2SO3, HNO3, H3PO4
D. H2CO3, H2SO4, HNO3, H3PO4
Câu 3: Khi Fe tác dụng với dung dịch H2SO4 loãng, sản phẩm của phản ứng là
A. FeSO4
B. Fe2(SO4)3
C. FeSO4 và H2
D. Fe2(SO4)2 và SO2
Câu 4: Trong hơi thở, chất khí làm đục nước vôi trong là:
A. SO3
B. CO2
C. SO2
D. NO2
Câu 5: Cho dung dịch KOH vào ống nghiệm đựng dung dịch FeCl3. Hiện tượng quan sát được là:
A. Có khí thóat ra
B. Có kết tủa trắng
C. Có kết tủa đỏ nâu
D. Có kết tủa trắng xanh
Câu 6: Để điều chế dung dịch Ba(OH)2, người ta cho:
A. BaO tác dụng với dung dịch HCl
B. BaCl2 tác dụng với dung dịch Na2CO3
C. BaO tác dụng với dung dịch H2O
D. Ba(NO3)2 tác dụng với dung dịch Na2SO4
Câu 7: Cho 2,24 lít khí CO2 (đktc) hấp thụ hoàn toàn bởi 200 ml dung dịch Ca(OH)2, chỉ thu được muối CaCO3. Nồng độ mol của dung dịch Ca(OH)2 cần dùng là:
A. 0,5M
B. 0,25M
C. 0,1M
D. 0,05M
Câu 8: Diêm tiêu có nhiều ứng dụng quan trọng như: Chế tạo thuốc nổ đen, làm phân bón, cung cấp nguyên tố nitơ và kali cho cây trồng, ... Công thức hóa học của diêm tiêu là
A. KCl
B. K2CO3
C. KClO3
D. KNO3
Câu 9: Có thể dùng dung dịch nào sau đây để phân biệt được 3 chất bột: CaO, CaCO3 và BaSO4
A. HCl
B. NaOH
C. KCl
D. BaCl2
Câu 10: Cặp chất tác dụng với nhau sẽ tạo ra khí lưu huỳnh đioxit là:
A. CaCO3 và HCl
B. K2CO3 và HNO3
C. Na2SO3 và H2SO4
D. Na2SO4 và HCl
Câu 11: Trong các loại phân bón sau, phân bón hoá học kép là:
A. (NH4)2SO4
B. Ca (H2PO4)2
C. KCl
D. KNO3
Câu 12: Cho phương trình phản ứng:
Na2CO3 + 2HCl → 2NaCl + X + H2O
X là:
A. CO
B. CO2
C. H2
D. Cl2
Câu 13: Trong các kim loại sau đây, kim loại có độ cứng lớn nhất là:
A. Crom (Cr)
B. Nhôm (Al)
C. Sắt (Fe)
D. Natri (Na)
Câu 14: Kim loại được rèn, kéo sợi, dát mỏng tạo nên các đồ vật khác nhau nhờ tính chất nào sau đây?
A. Tính dẫn nhiệt
B. Tính dẻo
C. Có ánh kim
D. Tính dẫn điện
Câu 15: Dãy kim loại nào sau đây được sắp xếp các kim loại theo thứ tự mức hoạt động hóa học giảm dần
A. K, Al, Mg, Cu, Fe
B. Na, Fe, Al, Zn, Ag
C. K, Mg, Fe, Cu, Au
D. Na, Cu, Al, Fe, Zn.
Câu 16: Thả một mảnh nhôm vào ống nghiệm chứa dung dịch CuSO4. Xảy ra hiện tượng:
A. Không có dấu hiệu phản ứng
B. Có chất khí bay ra, dung dịch không đổi màu
C. Có chất rắn màu trắng bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần
D. Có chất rắn màu đỏ bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần
Câu 17: Kim loại X có những tính chất hóa học sau:
- Phản ứng với oxit khi nung nóng.
- Phản ứng với dung dịch AgNO3.
- Phản ứng với dung dịch H2SO4 loãng giải phóng khí H2 và muối của kim loại hóa trị II. Kim loại X là:
A. Cu
B. Fe
C. Al
D. Na
Câu 18: Gang là hợp kim của sắt với cacbon và một lượng nhỏ các nguyên tố khác như: Si, Mn, S, …trong đó hàm lượng cacbon chiếm:
A. Từ 2% đến 5%
B. Từ 2% đến 6%
C. Trên 6%
D. Dưới 2%
Câu 19: Cho 8,1g một kim loại (hoá trị III) tác dụng với khí clo có dư thu được 40,05g muối. Xác định kim loại đem phản ứng:
A. Au
B. Cr
C. Al
D. Fe
Câu 20: Cho m gam bột sắt vào dung dịch axit sunfuric loãng dư, phản ứng hoàn toàn tạo ra 6,72 lít khí hiđro (đktc). Giá trị của m là:
A. 16,8
B. 15,6
C. 8,4
D. 11,2
II – TỰ LUẬN (3 điểm):
Câu 1: (1 điểm) Hoàn thành các phương trình hóa học biểu diễn dãy chuyển đổi hóa học sau :
Câu 2: (2 điểm) Cho một khối lượng sắt dư vào 50 ml dung dịch HCl. Kết thúc phản ứng, thu được 3,36 lít khí (đktc).
a) Viết phương trình hóa học.
b) Tính khối lượng sắt đã tham gia phản ứng.
c) Tính nồng độ mol của dung dịch HCl đã dùng.
Đáp án đề thi Học kì 1 môn Hóa học 9 - Đề số 11
I – TRẮC NGHIỆM
|
1D |
2D |
3C |
4B |
5C |
6C |
7A |
8D |
9A |
10C |
|
11D |
12B |
13A |
14B |
15C |
16D |
17B |
18A |
19C |
20A |
Câu 1: Đáp án D
Sắt(III) oxit (Fe2O3) tác dụng được với axit tạo muối và nước.
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Câu 2: Đáp án D
CO2 có axit tương ứng là H2CO3
SO3 có axit tương ứng là H2SO4
N2O5 có axit tương ứng là HNO3
P2O5 có axit tương ứng là H3PO4
Câu 3: Đáp án C
Kim loại có nhiều hóa trị phản ứng với HCl, H2SO4 loãng tạo muối hóa trị thấp.
Fe + H2SO4 → FeSO4 + H2
Câu 4: Đáp án B
Khí CO2 làm đục nước vôi trong. Do CO2 phản ứng với Ca(OH)2 tạo kết tủa CaCO3 trắng.
Phương trình phản ứng:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Câu 5: Đáp án C
Phương trình phản ứng:
3KOH + FeCl3 → 3KCl + Fe(OH)3↓ (đỏ nâu)
Câu 6: Đáp án C
Để điều chế dung dịch Ba(OH)2, người ta cho BaO tác dụng với dung dịch H2O
BaO + H2O → Ba(OH)2
Câu 7: Đáp án A
Phương trình phản ứng:
CO2 + Ca(OH)2 → CaCO3 + H2O
Theo phương trình:
Câu 8: Đáp án D
Muối kali nitrat (KNO3) còn có tên là diêm tiêu.
Câu 9: Đáp án A
Dùng HCl để nhận biết 3 chất bột trên.
- Chất bột chỉ tan trong HCl là CaO
CaO + 2HCl → CaCl2 + H2O
- Chất bột tan trong HCl đồng thời có khí thoát ra là CaCO3
CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
- Chất bột không tan trong HCl là BaSO4.
Câu 10: Đáp án C
A. Loại vì tạo phản ứng tạo khí CO2. Phương trình phản ứng:
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
B. Loại vì tạo phản ứng tạo khí CO2. Phương trình phản ứng:
K2CO3 + 2HNO3 → 2KNO3 + H2O + CO2
C. Chọn. Phản ứng tạo khí lưu huỳnh đioxit (SO2)
Na2SO3 + H2SO4 → Na2SO4 + H2O + SO2
D. Loại vì không xảy ra phản ứng.
Câu 11: Đáp án D
Phân bón hóa học kép là loại phân có chứa hai hoặc cả ba nguyên tố dinh dưỡng N, P, K.
KNO3 là phân bón hóa học kép chứa nguyên tố dinh dưỡng kali và đạm (N).
Câu 12: Đáp án B
Muối Na2CO3 phản ứng với axit HCl tạo muối mới (NaCl) và axit mới (H2CO3).
Tuy nhiên axit H2CO3 không bền và phân hủy ngay thành CO2 và H2O.
Vậy X là CO2. Phương trình phản ứng đầy đủ:
Na2CO3 + 2HCl → 2NaCl + CO2↑ + H2O
Câu 13: Đáp án A
Kim loại có độ cứng lớn nhất là crom (Cr).
Câu 14: Đáp án B
Kim loại được rèn, kéo sợi, dát mỏng tạo nên các đồ vật khác nhau nhờ tính dẻo.
Câu 15: Đáp án C
Chú ý dãy hoạt động hóa học của một số kim loại:
K, Na, Mg, Al, Zn, Fe, Pb, (H), Cu, Ag, Au
Câu 16: Đáp án D
Hiện tượng: Có chất rắn màu đỏ bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần
Giải thích: Do Al đẩy Cu ra khỏi muối tạo kim loại Cu có màu đỏ.
2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
Câu 17: Đáp án B
Kim loại thỏa mãn điều kiện trên là Fe
- Fe phản ứng với oxit khi nung nóng.
- Fe phản ứng với dung dịch AgNO3.
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag.
- Fe phản ứng với dung dịch H2SO4 loãng giải phóng khí H2 và muối của kim loại hóa trị II.
Câu 18: Đáp án A
Gang: Hàm lượng cacbon từ 2% đến 5%
Thép: Hàm lượng cacbon dưới 2%
Câu 19: Đáp án C
Đặt kim loại có công thức hóa học là M
Phương trình phản ứng:
2M + 3Cl2 → 2MCl3
Theo bài ra:
Theo phương trình:
→ M = 27 (Al)
Câu 20: Đáp án A
Fe + H2SO4 → FeSO4 + H2
Theo phương trình:
→ mFe = 0,3.56 = 16,8 gam
II – TỰ LUẬN (3 điểm):
Câu 1: ( 2 điểm)
Câu 2: (2 điểm)
Số mol khí H2 = 
a) Phương trình phản ứng:
Fe + 2HCl → FeCl2 + H2
b) Khối lượng sắt đã phản ứng:
Theo phương trình:
→ mFe = 0,15.56 = 8,4 gam
c) Số mol HCl phản ứng:
Theo phương trình:
Đổi 50 ml = 0,05 lít
Nồng độ mol của dung dịch HCl:
___________________________________________________________________
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Học kì 1 Hóa học lớp 9 có đáp án - (Đề số 12)
Họ, tên thí sinh: .....................................................................Lớp: .............................
(Cho C = 12, O = 16, H = 1, Na = 23, K = 39, Mg = 24, Ca = 40, P = 31, Cl = 35,5,
F = 19, Si = 27, N = 14, S = 32)
I - TRẮC NGHIỆM (7 Điểm)
Câu 1: Oxit bazơ không có tính chất hóa học nào sau đây?
A. Một số oxit bazơ tác dụng được với nước ở điều kiện thường.
B. Oxit bazơ tác dụng được với dung dịch axit.
C. Oxit bazơ tác dụng được với tất cả kim loại.
D. Một số oxit bazơ tác dụng được với oxit axit.
Câu 2: Chất nào sau đây góp phần nhiều nhất vào sự hình thành mưa axit?
A. CO2
B. SO2
C. N2
D. O3
Câu 3: Các oxit tác dụng được với nước là
A. PbO2, K2O, SO3.
B. BaO, K2O, SO2.
C. Al2O3, NO, SO2.
D. CaO, FeO, NO2.
Câu 4: Dẫn từ từ 3,136 lít khí CO2 (đktc) vào một dung dịch có hòa tan 12,8 gam NaOH sản phẩm thu được là muối Na2CO3. Khối lượng muối Na2CO3 thu được là:
A. 14,84 gam
B. 18, 96 gam
C. 16,96 gam
D. 16,44 gam
Câu 5: Cặp chất tác dụng với dung dịch axit clohiđric là
A. NaOH, BaCl2
B. NaOH, BaCO3.
C. NaOH, Ba(NO3)2.
D. NaOH, BaSO4.
Câu 6: Hoà tan hết 3,6 g một kim loại hoá trị II bằng dung dịch H2SO4 loãng được 3,36 lít H2 (đktc). Kim loại là:
A. Zn.
B. Mg.
C. Fe.
D. Ca.
Câu 7: Để nhận biết các dung dịch sau: H2SO4, NaOH, HCl, người ta dùng
A. quỳ tím và dung dịch BaCl2.
B. quỳ tím và dung dịch KOH.
C. phenolphtalein.
D. phenolphtalein và dung dịch NaCl.
Câu 8: Sau khi làm thí nghiệm, có những khí thải độc hại: HCl, H2S, CO2, SO2. Dùng chất nào sau đây để loại bỏ chúng là tốt nhất?
A. Muối NaCl
B. Nước vôi trong
C. Dung dịch HCl
D. Dung dịch NaNO3
Câu 9: Nếu chỉ dùng dung dịch NaOH thì có thể phân biệt được 2 dung dịch muối trong mỗi cặp chất sau:
A. Na2SO4 và Fe2(SO4)3
B. Na2SO4 và K2SO4
C. Na2SO4 và BaCl2
D. Na2CO3 và K3PO4
Câu 10: Trộn dung dịch có chứa 0,1 mol CuSO4 và một dung dịch chứa 0,3 mol NaOH, lọc kết tủa, rửa sạch rồi đem nung đến khối lượng không đổi thu được m g chất rắn. Giá trị m là:
A. 8 g
B. 4 g
C. 6 g
D. 12 g
Câu 11: Cho những phân bón có công thức: KNO3, NH4NO3, Ca(H2PO4)2, CO(NH2)2, (NH4)HPO4, KCl, NH4Cl. Số phân bón đơn là:
A. 5
B. 4
C. 3
D. 2
Câu 12: Phát biểu nào sau đây sai?
A. Phân urê cung cấp nitơ cho cây trồng.
B. Urê có công thức là (NH2)2CO.
C. Supephotphat có Ca(H2PO4)2.
D. Phân lân cung cấp kali cho cây trồng.
Câu 13: Trong tất cả các kim loại sau đây, kim loại nào dẫn điện tốt nhất?
A. Vàng (Au)
B. Bạc (Ag)
C. Đồng (Cu)
D. Nhôm (Al)
Câu 14: Hiện tượng xảy ra khi đốt sắt trong bình khí clo là:
A. Khói màu trắng sinh ra.
B. Xuất hiện những tia sáng chói.
C. Tạo chất bột trắng bám xung quanh thành bình.
D. Có khói màu nâu đỏ tạo thành.
Câu 15: Dãy kim loại được sắp xếp theo chiều hoạt động hóa học tăng dần:
A. K, Al, Mg, Cu, Fe.
B. Cu, Fe, Mg, Al, K.
C. Cu, Fe, Al, Mg, K.
D. K, Cu, Al, Mg, Fe.
Câu 16: Nhôm là kim loại
A. dẫn điện và nhiệt tốt nhất trong số tất cả kim loại.
B. dẫn điện và nhiệt đều kém
C. dẫn điện tốt nhưng dẫn nhiệt kém.
D. dẫn điện và nhiệt tốt nhưng kém hơn đồng.
Câu 17: Kim loại Fe tác dụng được với bao nhiêu chất trong dãy sau: HCl, H2SO4 đặc nguội, dung dịch NaOH, dung dịch Al(NO3)3; khí Cl2
A. 2
B. 3
C. 4
D. 5
Câu 18: Nguyên tắc luyện thép từ gang là
A. tăng thêm hàm lượng cacbon trong gang để thu được thép.
B. dùng chất khử CO khử oxit sắt thành sắt ở nhiệt độ cao.
C. dùng CaO hoặc CaCO3 để khử tạp chất Si, P, S, Mn, … trong gang để thu được thép.
D. dùng O2 oxi hóa các tạp chất Si, P, S, Mn, … trong gang để thu được thép.
Câu 19: Kim loại nào sau đây có khả năng tự tạo ra màng oxit cứng bảo vệ khi để ngoài không khí?
A. Al
B. Fe
C. Ca
D. Na
Câu 20: “Ăn mòn kim loại” là sự phá huỷ kim loại do:
A. Tác dụng hoá học của các chất trong môi trường xung quanh.
B. Kim loại phản ứng hoá học với chất khí hoặc hơi nước ở nhiệt độ cao.
C. Kim loại tác dụng với dung dịch chất điện ly tạo nên dòng diện.
D. Tác động cơ học.
II – TỰ LUẬN: (3 điểm)
Câu 1: (1 điểm)
Viết phương trình hóa học hoàn thành sơ đồ chuyển hóa sau (ghi rõ điều kiện nếu có)
Câu 2: Cho 7,5 gam hỗn hợp X gồm Al, Mg tác dụng với dung dịch HCl 14,6% (vừa đủ) thu được 7,84 lít khí (đktc) và dung dịch Y.
a) Viết phương trình hóa học xảy ra.
b) Tính thành phần % khối lượng của mỗi kim loại có trong hỗn hợp X.
Đáp án đề thi Học kì 1 môn Hóa học 9 - Đề sối 12
I – TRẮC NGHIỆM (7 điểm)
|
1C |
2B |
3B |
4A |
5B |
6B |
7A |
8B |
9A |
10A |
|
11A |
12D |
13B |
14D |
15C |
16D |
17A |
18D |
19A |
20A |
Câu 1: Đáp án C
Oxit bazơ không có tính chất tác dụng được với kim loại.
Câu 2: Đáp án B
SO2 là chất góp phần nhiều nhất vào sự hình thành mưa axit
Câu 3: Đáp án B
Các oxit: PbO2; Al2O3; FeO không tác dụng với nước.
Câu 4: Đáp án A
Xét tỉ lệ: 
Câu 5: Đáp án B
NaOH + HCl → NaCl + H2O
BaCO3 + 2HCl → BaCl2 + CO2↑ + H2O
Chú ý:
- Phản ứng trung hòa axit - bazơ luôn xảy ra.
- Phản ứng giữa axit và muối xảy ra với điều kiện: sản phẩm tạo thành có chất kết tủa hoặc chất bay hơi.
Câu 6: Đáp án B
nkhí = 3,36 : 22,4 = 0,15 mol
Gọi kim loại là R (hóa trị II)
R + H2SO4 (loãng) → RSO4 + H2
Theo phương trình:
Vậy kim loại cần tìm là magie (Mg).
Câu 7: Đáp án A
Ta có thể sử dụng thuốc thử là quỳ tím và dung dịch BaCl2.
- Trích mẫu thử của từng dung dịch ra ống nghiệm và đánh số thứ tự
- Thử bằng quỳ tím.
+ Quỳ tím hóa đỏ: H2SO4 và HCl
+ Quỳ tím hóa xanh: NaOH.
- Nhỏ dung dịch BaCl2 vào hai mẫu thử H2SO4 và HCl.
+ Mẫu thử tạo kết tủa trắng là H2SO4
H2SO4 + BaCl2 → BaSO4↓ + 2HCl
+ Không có hiện tượng gì là HCl.
Câu 8: Đáp án B
Nước vôi trong sẽ phản ứng với các khí trên để loại bỏ chúng.
Ca(OH)2 + 2HCl → CaCl2 + 2H2O
Ca(OH)2 + H2S → CaS + 2H2O
CO2 + Ca(OH)2 → CaCO3↓ + H2O
SO2 + Ca(OH)2 → CaSO3↓ + H2O
Câu 9:Đáp án A
Sử dụng NaOH có thể phân biệt được cặp Na2SO4 và Fe2(SO4)3
+ Nếu không có hiện tượng gì → Na2SO4
+ Nếu xuất hiện kết tủa đỏ nâu → Fe2(SO4)3
6NaOH + Fe2(SO4)3 → 2Fe(OH)3(↓ đỏ nâu) + 3Na2SO4.
Câu 10: Đáp án A
Xét tỉ lệ: 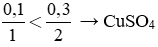
Số mol Cu(OH)2 tính theo số mol CuSO4
Câu 11: Đáp án A
Phân bón đơn là NH4NO3, Ca(H2PO4)2, CO(NH2)2, KCl, NH4Cl.
Lưu ý:
- Phân bón hóa học đơn chỉ chứa một trong ba nguyên tố dinh dưỡng chính là đạm (N), lân (P), kali (K).
- Phân bón kép có chứa hai hoặc cả ba nguyên tố dinh dưỡng N, P, K.
Câu 12: Đáp án D
Phát biểu sai là: D. Phân lân cung cấp kali cho cây trồng.
Vì phân lân cung cấp nguyên tố P cho cây trồng.
Câu 13: Đáp án B
Kim loại dẫn điện tốt nhất là Ag, sau đó đến Cu, Al, Fe,…
Câu 14: Đáp án D
Hiện tượng: Có khói màu nâu đỏ tạo thành.
Do sắt đã phản ứng với khí clo tạo thành FeCl3
Phương trình phản ứng:
Câu 15: Đáp án C
Thứ tự chiều hoạt động hóa học tăng dần của kim loại là: Cu, Fe, Al, Mg, K.
Câu 16: Đáp án D
Nhôm là kim loại dẫn điện và nhiệt tốt nhưng kém hơn đồng.
Kim loại dẫn điện tốt nhất là Ag, sau đó đến Cu, Al, Fe,…
Kim loại nào dẫn điện tốt thường cũng dẫn nhiệt tốt.
Câu 17: Đáp án A
Kim loại Fe tác dụng được với: HCl, khí Cl2
Fe + 2HCl → FeCl2 + H2
Câu 18: Đáp án D
Nguyên tắc luyện thép từ gang là: làm giảm hàm lượng các tạp chất (C, S, Si, Mn,..) có trong gang bằng cách oxi hoá các tạp chất đó thành oxit rồi biến thành xỉ và tách ra khỏi thép
Câu 19: Đáp án A
Kim loại có khả năng tự tạo ra màng oxit cứng bảo vệ khi để ngoài không khí là Al.
Al trong không khí thường có lớp màng oxit Al2O3 bảo vệ.
Câu 20: Đáp án A
Sự phá hủy kim loại và hợp kim do tác dụng hóa học của môi trường được gọi là sự ăn mòn kim loại.
II – TỰ LUẬN: (3 điểm)
Câu 1:
Câu 2:
a) Phương trình hóa học:
2Al + 6HCl → 2AlCl3 + 3H2 (1)
Mg + 2HCl → MgCl2 + H2 (2)
b)
Gọi x, y lần lượt là số mol của Al, Mg
Theo đề bài ta có: 27x + 24y = 7,5 (3)
Dựa vào phương trình (1), (2) ta có:
Giải hệ phương trình (3) và (4) ta được: x = 0,1; y = 0,2
%mMg = 100% - 36% = 64%
___________________________________________________________________
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Học kì 1 Hóa học lớp 9 có đáp án - (Đề số 13)
(Cho C = 12, O = 16, H = 1, Na = 23, K = 39, Mg = 24, Ca = 40, P = 31,
Cl = 35,5, F = 19, Si = 27, N = 14, S = 32)
Câu 1: Khi thả một cây đinh sắt sạch vào dung dịch CuSO4 loãng, có hiện tượng sau:
A. Sủi bọt khí, màu xanh của dung dịch nhạt dần.
B. Có một lớp đồng màu đỏ phủ lên đinh sắt, màu xanh của dung dịch đậm dần.
C. Có một lớp đồng màu đỏ phủ lên đinh sắt, dung dịch không đổi màu.
D. Có một lớp đồng màu đỏ phủ lên đinh sắt, màu xanh của dung dịch nhạt dần.
Câu 2: Bazơ nào sau đây không tan trong nước.
A. NaOH
B. KOH
C. Ca(OH)2
D. Cu(OH)2
Câu 3: Phương trình hóa học nào sau đây không đúng?
A. 2Fe + 3Cl2 → 2FeCl3
B. 2CO2 + Ca(OH)2 → Ca(HCO3)2
C. 2NaCl + H2SO4 → Na2SO4 + 2HCl
D. Fe + CuSO4 → FeSO4 + Cu
Câu 4: Dãy phi kim tác dụng với oxi tạo thành oxit axit là:
A. S, C, P.
B. S, C, Cl2.
C. C, P, Br2.
D. C, Cl2, Br2.
Câu 5: Muối nào sau đây không tan.
A. K2SO3
B. Na2SO3
C. CuCl2
D. BaSO4
Câu 6: Có các chất đựng riêng biệt trong mỗi ống nghiệm sau đây: Al, Fe, CuO, CO2, FeSO4, H2SO4. Lần lượt cho dung dịch NaOH vào mỗi ống nghiệm trên. Dung dịch NaOH phản ứng với:
A. Al, CO2, FeSO4, H2SO4
B. Fe, CO2, FeSO4, H2SO4
C. Al, Fe, CuO, FeSO4
D. Al, Fe, CO2, H2SO4
Câu 7: Dãy chất gồm các oxit bazơ là:
A. CuO, NO, MgO, CaO.
B. CuO, CaO, MgO, Na2O.
C. CaO, CO2, K2O, Na2O.
D. K2O, FeO, P2O5, Mn2O7.
Câu 8: Có một mẫu Fe bị lẫn tạp chất là nhôm, để làm sạch mẫu sắt này bằng cách ngâm nó với:
A. Dung dịch NaOH dư
B. Dung dịch H2SO4 loãng
C. Dung dịch HCl dư
D. Dung dịch HNO3 loãng
Câu 9: Cho 5,6 g sắt vào dung dịch đồng sunfat dư. Khối lượng đồng thu được là:
A. 6,4 g
B. 12,8 g
C. 64 g
D. 128 g
Câu 10: Cho 0,1 mol kim loại kẽm vào dung dịch HCl dư. Khối lượng muối thu được là:
A. 20,4
B. 1,36 g
C. 13,6 g
D. 27,2 g
Câu 11: X là nguyên tố phi kim có hoá trị III trong hợp chất với khí hiđro. Biết thành phần phần trăm khối lượng của hiđro trong hợp chất là 17,65%. X là nguyên tố:
A. C
B. S
C. N
D. P
Câu 12: Ngâm một lá Zn dư vào 200 ml dung dịch AgNO3 1M. Khi phản ứng kết thúc khối lượng Ag thu được là:
A. 6,5 gam
B. 10,8 gam
C. 13 gam
D. 21,6 gam
Câu 13: Axit nào sau đây dễ bay hơi.
A. H2SO3
B. H2SO4
C. HCl
D. HNO3
Câu 14: Chất nào sau đây góp phần nhiều nhất vào sự hình thành mưa axit?
A. CO2
B. SO2
C. N2
D. O3
Câu 15: Phản ứng nào dưới đây là phản ứng trao đổi?
A. 2Na + 2H2O → 2NaOH + H2
B. BaO + H2O → Ba(OH)2
C. Zn + H2SO4 → ZnSO4 + H2
D. BaCl2 + H2SO4 → BaSO4 + 2HCl
Câu 16. Kim loại X có những tính chất hóa học sau:
- Phản ứng với oxit khi nung nóng.
- Phản ứng với dung dịch AgNO3.
- Phản ứng với dung dịch H2SO4 loãng giải phóng khí H2 và muối của kim loại hóa trị II. Kim loại X là:
A. Cu
B. Fe
C. Al
D. Na.
Câu 17: Axit làm quỳ tím hóa
A. Xanh
B. đỏ
C. Hồng
D. Vàng
Câu 18: Những tính chất vật lí chung của kim loại là:
A. Tính dẻo, có ánh kim và rất cứng.
B. Tính dẻo, tính dẫn điện, nhiệt độ nóng chảy cao.
C. Tính dẫn điện, dẫn nhiệt, có ánh kim, có khối lượng riêng lớn.
D. Tính dẻo, tính dẫn điện, dẫn nhiệt, và có ánh kim.
Câu 19: Nguyên liệu sản xuất nhôm là quặng:
A. Hematit
B. Manhetit
C. Bôxit
D. Pirit.
Câu 20: Kim loại nào sau đây nhẹ nhất (có khối lượng riêng nhỏ nhất)?
A. Liti (Li)
B. Na (Natri )
C. Kali (K)
D. Rubiđi (Rb)
II - TỰ LUẬN (3 điểm)
Câu 1: (1 điểm) Bằng phương pháp hóa học hãy nhận biết dung dịch các chất chứa trong các lọ bị mất nhãn sau: HCl, KOH, NaNO3, Na2SO4.
Câu 2: (2 điểm) Cho hỗn hợp gồm Fe, Mg có khối lượng 8g tác dụng hết với dung dịch HCl thu được 4,48 lít khí H2 (đktc).
a) Viết phương trình hóa học của Fe và Mg với dung dịch HCl.
b) Tính tỉ lệ theo số mol của Fe và của Mg trong hỗn hợp ban đầu.
___________________________________________________________________
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Học kì 1 Hóa học lớp 9 có đáp án - (Đề số 14)
(Cho C = 12, O = 16, H = 1, Na = 23, K = 39, Mg = 24, Ca = 40, P = 31,
Cl = 35,5, F = 19, Si = 27, N = 14, S = 32)
Câu 1: Cặp chất tác dụng với nhau sẽ tạo ra khí lưu huỳnh đioxit là:
A. CaCO3 và HCl
B. Na2SO3 và H2SO4
C. CuCl2 và KOH
D. K2CO3 và HNO3
Câu 2: Chất có thể tác dụng với nước cho 1 dung dịch làm quỳ tím chuyển màu thành đỏ
A. MgO
B. CO
C. CaO
D. SO3
Câu 3: Cho 5,4 gam hỗn hợp 2 kim loại Fe và Zn tác dụng hoàn toàn với 90 ml dung dịch HCl 2M. Khối lượng muối thu được là
A. 11,79 gam
B. 11,5 gam
C. 15,71 gam
D. 17,19 gam
Câu 4: Nhỏ vài giọt dung dịch FeCl3 vào ống nghiệm đựng 1ml dung dịch NaOH, thấy xuất hiện
A. chất không tan màu nâu đỏ
B. chất không tan màu trắng
C. chất tan không màu
D. chất không tan màu xanh lơ
Câu 5: Dung dịch của chất X có pH > 7 và khi tác dụng với dung dịch kali sunfat tạo ra chất không tan. Chất X là.
A. BaCl2
B. NaOH
C. Ba(OH)2
D. H2SO4.
Câu 6: Hoà tan 23,5 g kali oxit vào nước được 0,5 lít dung dịch A. Nồng độ mol của dung dịch A là:
A. 0,25M.
B. 0,5M
C. 1M.
D. 2M.
Câu 7: Nung muối canxi cacbonat ở nhiệt độ trên 900oC thu được khí gì?
A. SO2
B. CO2
C. O2
D. SO3
Câu 8: Muối nào sau đây không tan.
A. K2SO3
B. Na2SO3
C. CuCl2
D. BaSO4
Câu 9: Chất tác dụng với dung dịch muối Al2(SO4)3 ở nhiệt độ thường là
A. H2O
B. CaCl2
C. Fe(OH)2
D. Mg
Câu 10: Phản ứng nào dưới đây là phản ứng trao đổi?
A. 2Na + 2H2O → 2NaOH + H2
B. BaO + H2O → Ba(OH)2
C. Zn + H2SO4 → ZnSO4 + H2
D. BaCl2 + H2SO4 → BaSO4 + 2HCl
Câu 11: Cặp chất nào sau đây không thể tồn tại trong 1 dung dịch (phản ứng với nhau)?
A. NaOH, MgSO4
B. KCl, Na2SO4
C. CaCl2, NaNO3
D. ZnSO4, H2SO4
Câu 12: Cho 1,84 hỗn hợp 2 muối ACO3 và BCO3 tác dụng hết với dung dịch HCl thu được 0,672 lít CO2 (đktc) và dung dịch X. Khối lượng muối trong dung dịch X là:
A. 1,17g
B. 3,17g
C. 2,17g
D. 4,17g
Câu 13: Hòa tan 0,25 mol NaCl vào nước, thu được 2 lit dung dịch NaCl. Vậy nồng độ mol của dung dịch trên là
A. 0,125M
B. 0,25M
C. 1,25M
D. 0,5M
Câu 14: Cho các phát biểu sau:
(1) Phân amoni nitrat NH4NO3 chứa 21% nitơ
(2) Phân photphat tự nhiên có thành phần chính là Ca3(PO4)2, tan chậm trong đất chua
(3) Các phân bón KCl, K2SO4, Ca(H2PO4)2 và (NH2)2CO đều là phân bón đơn
(4) Cu(OH)2, Fe(OH)3, Al(OH)3, Ba(OH)2 đều bị nhiệt phân hủy cho oxit và nước
(5) SO2, SO3, N2O5, P2O5, CO, CO2 là những oxit axit
(6) Các bazơ Mg(OH)2, Fe(OH)2, Ca(OH)2 đều có thể làm quỳ tím hóa xanh
Số phát biểu sai là:
A. 2
B. 3
C. 4
D. 5
Câu 15: Trong các loại phân bón hóa học sau, loại nào là phân đạm?
A. KCl
B. Ca3(PO4)2
C. K2SO4
D. (NH2)2CO
Câu 16: Cho AgNO3 tác dụng với HCl sản phẩm của phản ứng có
A. H2O
B. AgCl
C. NaOH
D. H2.
Câu 17: Một trong những thuốc thử nào sau đây có thể dùng để phân biệt dung dịch muối Na2CO3 và Na2SO4?
A. MgCl2
B. Pb(NO3)2
C. AgNO3
D. HCl
Câu 18: Những tính chất vật lí chung của kim loại là:
A. Tính dẻo, có ánh kim và rất cứng.
B. Tính dẻo, tính dẫn điện, nhiệt độ nóng chảy cao.
C. Tính dẫn điện, dẫn nhiệt, có ánh kim, có khối lượng riêng lớn.
D. Tính dẻo, tính dẫn điện, dẫn nhiệt, và có ánh kim.
Câu 19: Trong các kim loại sau đây, kim loại dẫn điện tốt nhất là:
A. Nhôm (Al)
B. Bạc (Ag)
C. Đồng (Cu)
D. Sắt (Fe)
Câu 20: Axit nào tác dụng được với Mg tạo ra khí H2:
A. H2SO4 đặc, HCl
B. HCl, H2SO4 loãng
C. HNO3loãng, H2SO4 loãng
D. HNO3 đặc, H2SO4đặc
Câu 21: Không sử dụng dây điện trần trong sinh hoạt vì
A. dễ nóng chảy.
B. dễ bị điện giật.
C. mất thẩm mỹ.
D. dẩn điện không tốt.
Câu 22: Dãy các kim loại nào sau đây được sắp xếp theo chiều hoạt động hóa học giảm dần?
A. Cu, Ag, Fe, Al, Mg, K
B. K, Mg, Al, Fe, Cu, Ag.
C. Ag, Cu, Fe, Al, Mg, K.
D. K, Mg, Al, Cu, Ag, Fe.
Câu 23: Để bảo quản kim loại Na trong phòng thí nghiệm, người ra thường ngâm Na trong chất nào dưới đây?
A. H2O.
B. Dung dịch H2SO4 đặc.
C. Dung dịch HCl.
D. Dầu hỏa.
Câu 24: Đun nóng 6,4 g lưu huỳnh và 1,3 g kẽm. Sau phản ứng thu được các chất với khối lượng là:
A. 2,17g Zn và 0,89g S
B. 5,76 g S và 1,94 g ZnS
C. 2,12 g ZnS
D. 7,7 g ZnS
Câu 25: Cho 10,5g hỗn hợp 2 kim loại Cu và Zn vào dd H2SO4 loãng dư, người ta thu được 2,24 lít khí (đktc). Thành phần % theo khối lượng của Cu và Zn lần lượt là:
A. 61,9% và 38,1%
B. 38,1% và 61,9%
C. 65% và 35%
D. 35% và 65%
Câu 26: Thành phần chính của quặng pirit là
A. Fe2O3
B. FeS2
C. Fe3O4
D. Al2O3
Câu 27: Sắt bị nam châm hút là do
A. Sắt là kim loại nặng.
B. Sắt có từ tính.
C. Sắt có màu trắng.
D. Sắt có tính dẫn điện
Câu 28: Nhôm hoạt động hoá học mạnh hơn sắt, vì:
A. Al, Fe đều không phản ứng với HNO3 đặc nguội.
B. Al có phản ứng với dung dịch kiềm.
C. Nhôm đẩy được sắt ra khỏi dung dịch muối sắt.
D. Chỉ có sắt bị nam châm hút.
Câu 29: Để phân biệt 3 gói bột: Fe, Cu và Al có thể dùng các dung dịch
A. NaOH và FeCl2
B. HCl và CuCl2
C. Ca(OH)2 và NaCl
D. HCl và NaOH
Câu 30: Sau một ngày lao động người ta phải làm vệ sinh các thiết bị, máy móc, dụng cụ lao động bằng kim loại. Việc làm này có mục đích chính là gì?
A. Để kim loại sáng bóng đẹp mắt.
B. Để không gây ô nhiễm môi trường
C. Để không làm bẩn quần áo khi lao động
D. Để kim loại đỡ ăn mòn
___________________________________________________________________
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Học kì 1 Hóa học lớp 9 có đáp án - (Đề số 15)
Họ và tên thí sinh:..................................................................... Lớp: ........................
(Cho C = 12, O = 16, H = 1, Na = 23, K = 39, Mg = 24, Ca = 40, P = 31,
Cl = 35,5, F = 19, Si = 27, N = 14, S = 32)
Câu 1: Dãy gồm các chất đều là bazơ tan là:
A. NaOH, KOH, Ba(OH)2
B. Ca(OH)2, Mg(OH)2, Cu(OH)2
C. NaOH, KOH, Al(OH)3
D. Ba(OH)2, Fe(OH)3, NaOH
Câu 2: Chất nào sau đây tác dụng được với dung dịch axit H2SO4 loãng
A. Cu
B. HCl
C. CO2
D. Zn
Câu 3: Chất có thể tác dụng với nước cho 1 dung dịch làm quỳ tím chuyển màu thành đỏ
A. MgO
B. SO3
C. CaO
D. CO
Câu 4: Hãy chọn cách sắp xếp theo tính hoạt động hóa học tăng dần (từ trái sang phải) của các nhóm kim loại sau:
A. Al, Zn, Fe, Na, Cu, Ag, Pb
B. Ag, Cu, Pb, Fe, Zn, Al, Na
C. Ag, Cu, Pb, Zn, Fe, Al, Na
D. Ag, Pb, Cu, Fe, Zn, Al, Na
Câu 5: Có 3 lọ mất nhãn đựng các hóa chất sau: HCl, H2SO4, NaOH. Hãy chọn thuốc thử nào sau đây để nhận biết dung dịch trong mỗi lọ?
A. Dùng quì tím
B. Dùng dung dịch BaCl2
C. Dùng quì tím và dung dịch BaCl2
D. Dùng quì tím và dung dịch phenol phtalein .
Câu 6: Trong công nghiệp, sản xuất axitsunfuric qua mấy công đoạn?
A. 1
B. 2
C. 3
D. 4
Câu 7: Oxit vừa tan trong nước vừa hút ẩm là:
A. SO2
B. CaO
C. Fe2O3
D. Al2O3
Câu 8: Nguyên liệu chính để sản xuất nhôm là:
A. criolit
B. quặng bôxit
C. điện
D. Than chì
Câu 9: Cặp chất nào sau đây tồn tại trong một dung dịch?
A. NaCl và AgNO3.
B. NaOH và K2CO3.
C. Na2SO4 và BaCl2.
D. Na2CO3 và H3PO4.
Câu 10: Hiện tượng xảy ra khi cho Al vào ống nghiệm chứa sẵn 2 ml dung dịch NaOH
A. có khí không màu thoát ra, nhôm tan dần.
B. nhôm tan dần, có kết tủa trắng.
C. xuất hiện dung dịch màu xanh.
D. không có hiện tượng xảy ra.
Câu 11: Đồng(II) sunfat là tên gọi của chất có công thức hóa học:
A. CuCl2
B. Cu2O
C. CuS
D. CuSO4
Câu 12: Đâu không phải là công thức hóa học của axit
A. HCl
B. NH3
C. H3PO4
D. HNO3
Câu 13: Phản ứng nào dưới đây là phản ứng trao đổi?
A. 2Na + 2H2O → 2NaOH + H2
B. BaO + H2O → Ba(OH)2
C. Zn + H2SO4 → ZnSO4 + H2
D. BaCl2 + H2SO4 → BaSO4 + 2HCl
Câu 14: Cho 0,1 mol kim loại kẽm vào dung dịch HCl dư. Khối lượng muối thu được là:
A. 20,4
B. 1,36 g
C. 13,6 g
D. 2,04 g
Câu 15: Phương trình hóa học nào sau đây không đúng?
A. 2Fe + 3Cl2 → 2FeCl3
B. 2CO2 + Ca(OH)2 → Ca(HCO3)2
C. 2NaCl + H2SO4 → Na2SO4 + 2HCl
D. Fe + CuSO4 → FeSO4 + Cu
Câu 16: Nhôm phản ứng được với:
A. Khí clo, dung dịch kiềm, axit, khí oxi.
B. Khí clo, axit, oxit bazơ, khí hiđro.
C. Oxit bazơ, axit, hiđro, dung dịch kiềm.
D. Khí clo, axit, oxi, hiđro, dung dịch magiesunfat.
Câu 17: Để điều chế dung dịch Ba(OH)2, người ta cho:
A. BaO tác dụng với dung dịch HCl
B. BaCl2 tác dụng với dung dịch Na2CO3
C. BaO tác dụng với dung dịch H2O
D. Ba(NO3)2 tác dụng với dung dịch Na2SO4
Câu 18: Cho 2,24 lít khí CO2 (đktc) hấp thụ hoàn toàn bởi 200 ml dung dịch Ca(OH)2, chỉ thu được muối CaCO3. Nồng độ mol của dung dịch Ca(OH)2 cần dùng là:
A. 0,5M
B. 0,25M
C. 0,1M
D. 0,05M
Câu 19: Trộn dung dịch có chứa 0,1 mol CuSO4 và một dung dịch chứa 0,3 mol NaOH, lọc kết tủa, rửa sạch rồi đem nung đến khối lượng không đổi thu được m g chất rắn. Giá trị m là:
A. 8 g
B. 4 g
C. 6 g
D. 12 g
Câu 20: “Ăn mòn kim loại” là sự phá huỷ kim loại do:
A. Tác dụng hoá học của các chất trong môi trường xung quanh.
B. Kim loại phản ứng hoá học với chất khí hoặc hơi nước ở nhiệt độ cao.
C. Kim loại tác dụng với dung dịch chất điện ly tạo nên dòng diện.
D. Tác động cơ học.
Câu 21: Để phân biệt 3 kim loại Fe, Mg và Al cần dùng
A. Dung dịch HCl và dung dịch NaOH
B. H2O và dung dịch HCl
C. Dung dịch NaOH và H2O
D. Dung dịch CuCl2 và H2O
Câu 22: Phát biểu nào sau đây không đúng?
A. Khi cho sắt tác dụng với dung dịch HCl tạo thành muối và FeCl2
B. Khi cho clo tác dụng với sắt tạo thành muối FeCl3
C. Khi cho clo tác dụng với sắt tạo thành muối FeCl2
D. Khi cho clo tác dụng với FeCl2 tạo thành muối FeCl3
Câu 23: Trung hòa 200ml dung dịch H2SO4 0,1M bằng dung dịch NaOH 10%. Khối lượng dung dịch NaOH cần dùng là:
A. 6g
B. 8g
C. 10g
D. 16g
Câu 24: Dãy phân bón hoá học chỉ chứa toàn phân bón hoá học đơn là:
A. KNO3, NH4NO3, (NH2)2CO
B. KCl, NH4H2PO4, Ca(H2PO4)2
C. (NH4)2SO4, KCl, Ca(H2PO4)2
D. (NH4)2SO4, KNO3, NH4Cl
Câu 25: Nhóm các dung dịch có pH > 7 là:
A. HCl, NaOH
B. H2SO4, HNO3
C. NaOH, Ca(OH)2
D. BaCl2, NaNO3
Câu 26: Cho 1,66g hỗn hợp gồm Al và Fe tác dụng với dung dịch H2SO4 loãng dư. Sau phản ứng thu được 1,12 lít khí H2 (đktc). Thành phần % theo khối lượng mỗi kim loại trong hỗn hợp lần lượt là:
A. 32,5% và 67,5%
B. 67,5% và 32,5%
C. 55% và 45%
D. 45% và 55%
Câu 27: Thả một mảnh nhôm vào ống nghiệm chứa dung dịch CuSO4. Xảy ra hiện tượng:
A. Không có dấu hiệu phản ứng.
B. Có chất rắn màu trắng bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần.
C. Có chất rắn màu đỏ bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần.
D. Có chất khí bay ra, dung dịch không đổi màu.
Câu 28: Để nhận biết dung dịch axit sunfuric và dung dịch axit clohiđric ta dùng thuốc thử:
A. NaNO3.
B. KCl.
C. MgCl2.
D. BaCl2.
Câu 29: Để nhận biết 2 loại phân bón hoá học là: NH4NO3 và NH4Cl. Ta dùng dung dịch:
A. KOH
B. Ca(OH)2
C. AgNO3
D. BaCl2
Câu 30: Dãy kim loại tác dụng được với dung dịch Cu(NO3)2 tạo thành Cu kim loại:
A. Al, Zn, Fe
B. Zn, Pb, Au
C. Mg, Fe, Ag
D. Na, Mg, Al