
Quang Minh
Sắt đoàn
0
0
Cho phương trình nhiệt hóa học:
3H2(g) + N2(g) 2NH3(g)
= –91,80 kJ
Lượng nhiệt tỏa ra tối đa khi dùng 9 gam H2(g) để tạo thành NH3(g) là
Số oxi hóa cao nhất của nguyên tử nitrogen là
Trong tự nhiên, nguyên tố nitrogen chủ yếu tồn tại ở dạng đồng vị nào sau đây?
Cho dung dịch NaOH dư vào 150 mL dung dịch (NH4)2SO4 1M, đun nóng nhẹ đến khi phản ứng hoàn toàn thấy thoát ra V lít khí ammonia. Tính giá trị của V?
Theo thuyết Brønsted – Lowry về acid – base, chất nào sau đây là base?
Cho m gam hỗn hợp gồm Na, Na2O, Ba, BaO (trong đó oxygen chiếm 9,639% khối lượng) tác dụng với một lượng dư H2O, thu được 0,7437 lít H2 và 200 mL dung dịch X. Cho X tác dụng với 200 mL dung dịch chứa hỗn hợp gồm H2SO4 0,2M và HCl 0,1M, thu được 400 mL dung dịch có pH = 13. Giá trị của m gần nhất với giá trị nào sau đây?
Nitric acid đặc tạo được với hydrochloric acid đặc hỗn hợp có tính oxi hóa mạnh (thường được gọi là nước cường toan) có khả năng hòa tan gold theo phản ứng:
Au + HNO3 + HCl AuCl3 + NO + H2O
Hãy tính tổng hệ số của các chất trong PTHH (các hệ số được lấy đến các số nguyên, tối giản).
Viết phương trình điện li của các chất sau AlCl3; Ba(OH)2; Na2CO3; HNO3.
Để nhận biết ion NH4+ trong dung dịch, thuốc thử cần dùng là
Quan sát hình bên dưới và từ dữ kiện năng lượng liên kết trong phân tử N2, dự đoán về độ bền phân tử và khả năng phản ứng của nitrogen ở nhiệt độ thường.
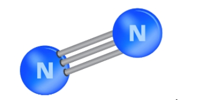
.
Eb (NºN) = 945 kJ/mol
A. Kém bền và hoạt động hóa học mạnh ở nhiệt độ thường.
B. Bền và trơ về mặt hóa học mạnh ở nhiệt độ thường.
C. Bền và hoạt động hóa học mạnh ở nhiệt độ thường.
Cho các chất: NH3, HCl, H3PO4, Ba(OH)2. Theo thuyết Bronsted – Lowry có bao nhiêu chất trong dãy trên là acid?
Dung dịch acid HCl có nồng độ 0,001M có pH bằng bao nhiêu?
Dãy gồm các chất điện li mạnh là
A. KOH, NaCl, H2S.
B. Na2S, H2S , HCl.
C. CH3COOH, NaNO3, Ca(OH)2.
Các dung dịch acid, base, muối dẫn điện được là do trong dung dịch của chúng có các
Cho cân bằng hóa học sau: N2(g) + 3H2(g) 2NH3(g) có ∆H < 0. Cân bằng trên chuyển dịch theo chiều thuận khi
A. tăng nhiệt độ của hệ phản ứng.
B. giảm áp suất của hệ phản ứng.
Xét phản ứng thuận nghịch tổng quát: aA + bB cC + dD. Ở trạng thái cân bằng, hằng số cân bằng (KC) của phản ứng được xác định theo biểu thức:
Việc sản xuất ammonia trong công nghiệp dựa trên phản ứng thuận nghịch sau đây:
N2(g) + 3H2(g) 2NH3(g)
= -92 kJ
Khi hỗn hợp phản ứng đang ở trạng thái cân bằng, những thay đổi dưới đây sẽ làm cân bằng chuyển dịch như thế nào? Giải thích.
(a) Tăng nhiệt độ. (d) Giảm nhiệt độ.
(b) Tăng áp suất. (e) Lấy NH3 ra khỏi hệ.
(c) Thêm chất xúc tác.
Tại sao khi bảo quản các dung dịch muối M3+ (Fe3+, Al3+ …) trong phòng thí nghiệm, người ta thường nhỏ vài giọt acid vào trong lọ đựng dung dịch muối?


