Bài 3. Một hợp chất có thành phần phần trăm theo khối lượng các nguyên tố như sau:
28% Fe; 24% S, còn lại là oxi. Biết 0,45 mol hợp chất có khối lượng là 180 gam. Xác
định công thức hóa học và gọi tên hợp chất.
Quảng cáo
4 câu trả lời 553
Gọi C T hợp chất là FexSyOz
%mO=100%-28%-24%=48%
Ta có:
=>CT là: [Fe2(SO4)3]n
0,45 mol có khối lượng 180g nên 1 mol có khối lượng là: 180 : 0,45=400 g/mol
=>400n=400=>n=1
Vậy CT của hợp chất là: Fe2(SO4)3 (sắt (III) sunfat)
M =180:0,45 = 400
%O = 100% -28% - 24% = 48%
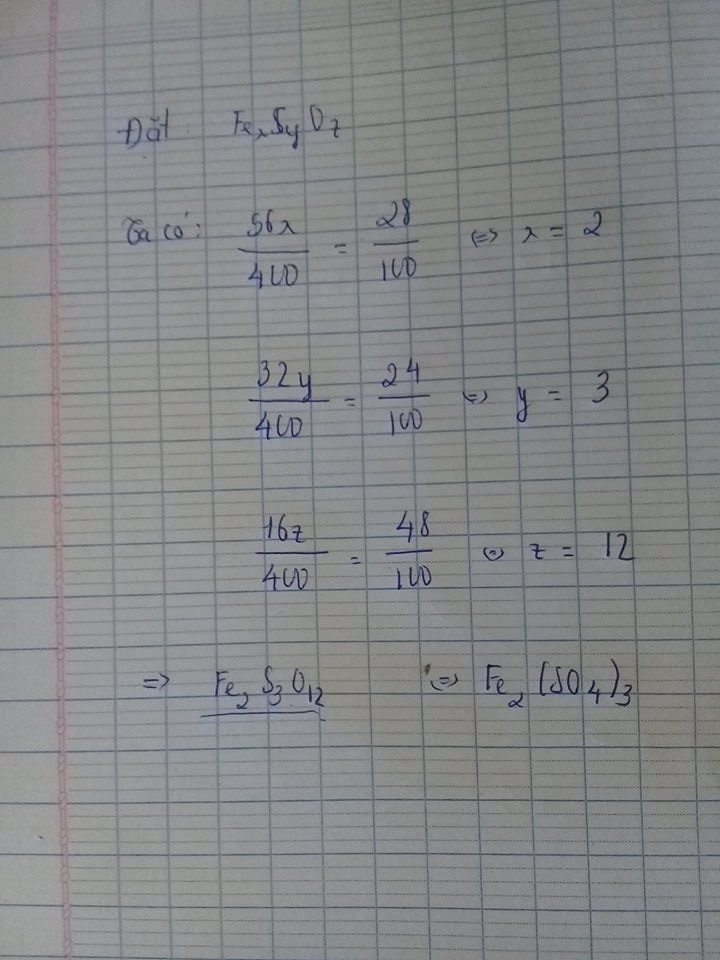
Vậy CTHH của hợp chất là Fe2(SO4)3
Gọi C T hợp chất là FexSyOz
%mO=100%-28%-24%=48%
Ta có:
x:y:z=2856:2432:4816=0,5:0,75:3=2:3:12
=>CT là: [Fe2(SO4)3]n
0,45 mol có khối lượng 180g nên 1 mol có khối lượng là: 180 : 0,45=400 g/mol
=>400n=400=>n=1
Vậy CT của hợp chất là: Fe2(SO4)3 (sắt (III) sunfat)
CT của hợp chất là: Fe2(SO4)3 (sắt (III) sunfat)
Quảng cáo
Bạn muốn hỏi bài tập?
Câu hỏi hot cùng chủ đề
-
25742


