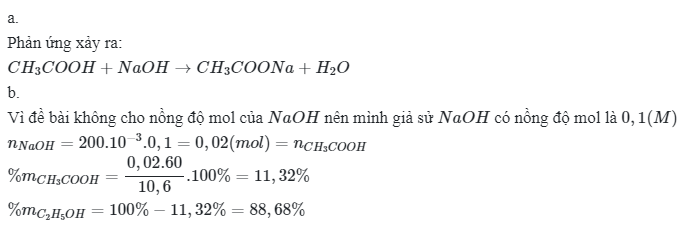Quảng cáo
3 câu trả lời 512
a) Viết phương trình hóa học:
CH3COOH (axit axetic) + C2H5OH (rượu etylic) + NaOH → CH3COONa (muối natri của axit axetic) + C2H5ONa (muối natri của rượu etylic) + H2O
b) Để tính thành phần phần trăm khối lượng mỗi chất trong hỗn hợp, ta cần thực hiện các bước sau:
1. Xác định số mol của mỗi chất trong hỗn hợp:
- Khối lượng mol của NaOH: 200ml dung dịch NaOH có nồng độ 0,1M, nNaOH = C.V = 0,1 x 0,2 = 0,02 mol
- Do phản ứng vừa đủ nên số mol axit axetic và rượu etylic bằng nhau và bằng số mol NaOH, nCH3COOH = nC2H5OH = 0,02 mol
2. Tính khối lượng mỗi chất trong hỗn hợp:
- Khối lượng axit axetic: mCH3COOH = nCH3COOH x MMCH3COOH = 0,02 x 60 = 1,2g
- Khối lượng rượu etylic: mC2H5OH = nC2H5OH x MMC2H5OH = 0,02 x 46 = 0,92g
3. Tính thành phần phần trăm khối lượng mỗi chất trong hỗn hợp:
- Phần trăm khối lượng axit axetic: %CH3COOH = (mCH3COOH / 10,6) x 100%
- Phần trăm khối lượng rượu etylic: %C2H5OH = (mC2H5OH / 10,6) x 100%
...
a.
Phản ứng xảy ra:
$CH_3COOH+NaOH \to CH_3COONa +H_2O$
b.
Vì đề bài không cho nồng độ mol của $NaOH$ nên mình giả sử $NaOH$ có nồng độ mol là $0,1(M)$
$n_{NaOH}=200.10^{-3}.0,1=0,02(mol)=n_{CH_3COOH}$
$\%m_{CH_3COOH}=\dfrac{0,02.60}{10,6}.100\%=11,32\%$
$\%m_{C_2H_5OH}=100\%-11,32\%=88,68\%$
Quảng cáo
Bạn cần hỏi gì?
Câu hỏi hot cùng chủ đề
-
 Đã trả lời bởi chuyên gia
45575
Đã trả lời bởi chuyên gia
45575 -
 Đã trả lời bởi chuyên gia
43639
Đã trả lời bởi chuyên gia
43639 -
Hỏi từ APP VIETJACK
 Đã trả lời bởi chuyên gia
39409
Đã trả lời bởi chuyên gia
39409 -
 Đã trả lời bởi chuyên gia
37090
Đã trả lời bởi chuyên gia
37090 -
 Đã trả lời bởi chuyên gia
36560
Đã trả lời bởi chuyên gia
36560 -
 Đã trả lời bởi chuyên gia
32612
Đã trả lời bởi chuyên gia
32612 -
Hỏi từ APP VIETJACK
 Đã trả lời bởi chuyên gia
32481
Đã trả lời bởi chuyên gia
32481