Nung m gam hỗn hợp Al, đến phản ứng hoàn toàn thu được hỗn hợp rắn Y. Chia Y làm 2 phần bằng nhau. Phần 1 tác dụng với dung dịch loãng dư, sinh ra 3,08 lít khí ở đktc. Phần 2 tác dụng với dung dịch NaOH dư, sinh ra 0,84 lít khí ở đktc. Giá trị của m là:
A. 21,40 B. 29,40 C. 29,43 D. 22,75
Quảng cáo
1 câu trả lời 556
2Al + → + 2Fe
= 3,08/22,4 = 0,1375 mol
= 0,84/22,4 = 0,0375 mol
Thấy phần 2 tác dụng với NaOH sinh ra khí, suy ra sản phẩm có Al dư.
Vậy rắn Y gồm , Fe và Al dư.
Phần 2:
2Al + 2NaOH + 2
Theo PTPU ta có:
= 2/3 . 0,0375 = 0,025 mol
⇒ = 0,025 mol
Phần 1:
Fe + (*)
2Al + (**)
Theo (**) ta có:
0 = 3/2 . 0,025 = 0,0375 mol
⇒ 1 = 0,1375 - 0,0375 = 0,1 mol
⇒2=0,1 mol
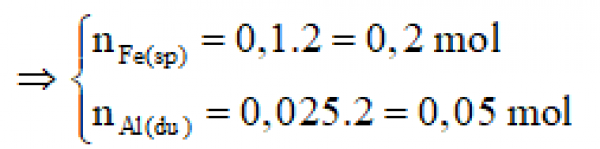
⇒ 3 = 0,2 mol
⇒ 4 = 1/2 . 5 = 1/2 . 0,2 = 0,1 mol
⇒ 6 = 0,1.160+0,05.27+0,2.27=22,75g
⇒ Chọn D.
Quảng cáo
Bạn cần hỏi gì?
Câu hỏi hot cùng chủ đề
-
 Đã trả lời bởi chuyên gia
45540
Đã trả lời bởi chuyên gia
45540 -
 Đã trả lời bởi chuyên gia
43612
Đã trả lời bởi chuyên gia
43612 -
Hỏi từ APP VIETJACK
 Đã trả lời bởi chuyên gia
39357
Đã trả lời bởi chuyên gia
39357 -
 Đã trả lời bởi chuyên gia
37056
Đã trả lời bởi chuyên gia
37056 -
 Đã trả lời bởi chuyên gia
36413
Đã trả lời bởi chuyên gia
36413 -
 Đã trả lời bởi chuyên gia
32526
Đã trả lời bởi chuyên gia
32526 -
Hỏi từ APP VIETJACK
 Đã trả lời bởi chuyên gia
32372
Đã trả lời bởi chuyên gia
32372


