Ngâm một lá sắt có khối lượng 2,5g trong 25ml dung dịch 15% có khối lượng riêng là 1,12g/ml. Sau thời gian phản ứng, người ta lấy lá sắt ra rửa nhẹ, làm khô thì cân nặng 2,56g. Tính nồng độ phần trăm của trong dung dịch sau phản ứng.
A. 4,08% và 10,74% B. 10,745% và 4,08%
C. 4% và 10,754% D. 10,754% và 4%
Quảng cáo
1 câu trả lời 1092
Fe + + Cu
= 1,12.25 = 28g
⇒ = 15/100.28 = 4,2g
⇒ = 4,2/160 = 0,02625 mol
Gọi số mol Fe phản ứng là x mol.
⇒ = x mol
Ta có:
⇒ 2,56 = 2,5 - 56x + 54x
⇒ 8x = 0,06
⇒ x = 0,0075 mol
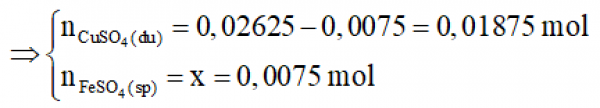
Vậy
= 28 + 0,0075.56 -0,0075.64 = 27,94g
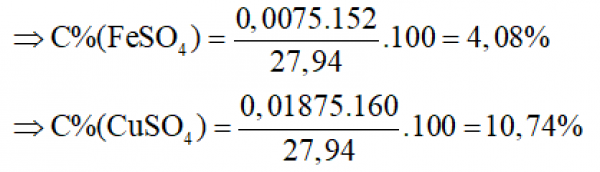
⇒ Chọn A.
Quảng cáo
Bạn cần hỏi gì?
Câu hỏi hot cùng chủ đề
-
 Đã trả lời bởi chuyên gia
45540
Đã trả lời bởi chuyên gia
45540 -
 Đã trả lời bởi chuyên gia
43612
Đã trả lời bởi chuyên gia
43612 -
Hỏi từ APP VIETJACK
 Đã trả lời bởi chuyên gia
39357
Đã trả lời bởi chuyên gia
39357 -
 Đã trả lời bởi chuyên gia
37056
Đã trả lời bởi chuyên gia
37056 -
 Đã trả lời bởi chuyên gia
36413
Đã trả lời bởi chuyên gia
36413 -
 Đã trả lời bởi chuyên gia
32526
Đã trả lời bởi chuyên gia
32526 -
Hỏi từ APP VIETJACK
 Đã trả lời bởi chuyên gia
32372
Đã trả lời bởi chuyên gia
32372
Gửi báo cáo thành công!


