Quảng cáo
3 câu trả lời 330
1) Trước khi kết hợp
Canxi: Ca có 2 electron hoá trị
Oxi: O có 6 electron hoá trị
Biểu diễn (dấu • là electron hoá trị):
Ca :• • :Ö: • •
(O có 6e: 2 cặp + 2 e đơn lẻ)
2) Chuyển electron (liên kết ion)
Ca nhường 2e cho O để đạt cấu hình bền (khí hiếm). O nhận 2e để đủ bát tử (8e).
Ca :• • →→ :Ö: • •
2e chuyển sang O
3) Sau khi kết hợp (ion tạo thành)
Ca trở thành Ca²⁺ (mất 2e, không còn chấm ở vỏ ngoài).
O trở thành O²⁻ (đủ 8e = 4 cặp electron).
Viết Lewis cho cặp ion:
[ Ca ]²⁺ [ :Ö: • • ]²⁻
(O có 4 cặp e: :Ö: với 8e)
Hoặc gọn hơn:
[Ca]²⁺ [O]²⁻
Giải thích ngắn: CaO là liên kết ion: Ca nhường 2e → Ca²⁺; O nhận 2e → O²⁻. Lực hút tĩnh điện giữa Ca²⁺ và O²⁻ tạo nên tinh thể CaO. (Trong thực tế, CaO là mạng tinh thể ion; sơ đồ Lewis trên minh hoạ cặp ion cơ bản.)
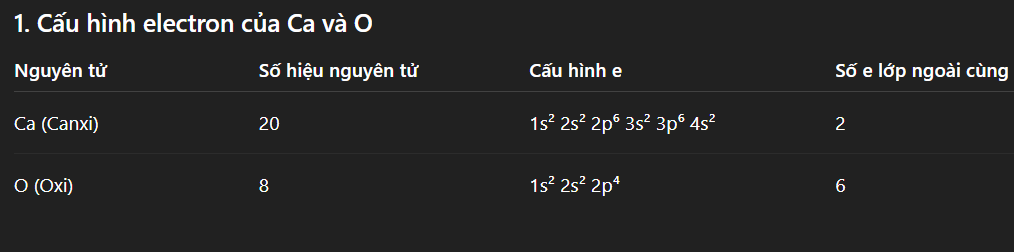
2. Cách tạo liên kết
- Canxi có 2 electron lớp ngoài cùng (4s²) → dễ nhường 2e để trở thành ion Ca²⁺.
- Oxi có 6 electron lớp ngoài cùng, cần nhận thêm 2e để đạt cấu hình bền của khí hiếm (8e lớp ngoài cùng) → trở thành ion O²⁻.
→ Khi Ca và O kết hợp, Canxi nhường 2e cho Oxi:
Ca → Ca2+ + 2e−
O + 2e− → O2−
→ Tạo thành liên kết ion: Ca2+[O]2−
3. Mô hình cấu tạo (mô tả)
Ca²⁺: không còn electron lớp ngoài cùng.
O²⁻: có 8 electron ở lớp ngoài cùng (đủ bát tử).
Giữa chúng là lực hút tĩnh điện giữa ion dương và ion âm → tạo tinh thể CaO.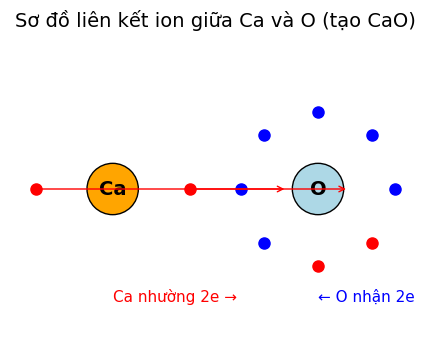
Rất hay 🌟 Ta cùng phân tích và vẽ sơ đồ liên kết ion giữa Ca và O nhé 👇
1. Thông tin cơ bản
Nguyên tử Ca (Canxi): có 2 electron ở lớp ngoài cùng → cấu hình ( [Ar]4s^2 )
→ Dễ mất 2 electron để đạt cấu hình bền vững như khí hiếm Argon.
→ Sau khi mất 2e, Ca trở thành ion dương Ca²⁺.
Nguyên tử O (Oxi): có 6 electron ở lớp ngoài cùng → cấu hình ( [He]2s^2 2p^4 )
→ Cần nhận thêm 2 electron để đủ 8e lớp ngoài cùng (bền vững như Neon).
→ Sau khi nhận 2e, O trở thành ion âm O²⁻.
2. Quá trình hình thành liên kết ion
Ca → Ca²⁺ + 2e⁻
O + 2e⁻ → O²⁻
→ Hai electron mà Ca mất đi sẽ được O nhận.
→ Tạo thành hợp chất ion: CaO
3. Sơ đồ liên kết (dạng Lewis)
Ta có thể biểu diễn như sau:
Ca : (2e ngoài cùng)
O : (6e ngoài cùng)
Trước khi tạo liên kết:
Ca: ••
O : •• ••
••
Sau khi chuyển electron:
Ca mất 2e → [Ca]²⁺
O nhận 2e → [O]²⁻ có 8e lớp ngoài cùng
Sơ đồ:
Ca → [O]²⁻
[O]²⁻ : [:O:]²⁻ (O có 8 electron xung quanh)
Hoặc có thể vẽ ngắn gọn như:
Ca → O
Ca²⁺ [ :O: ]²⁻
4. Kết luận
Loại liên kết: Liên kết ion
Công thức hóa học: ( \text{CaO} )
Cơ chế: Ca cho 2e, O nhận 2e → tạo thành cặp ion ( \text{Ca}^{2+} ) và ( \text{O}^{2-} ).
👉 Tóm tắt sơ đồ đơn giản:
Ca → Ca²⁺ + 2e⁻
O + 2e⁻ → O²⁻
=> Ca²⁺ O²⁻ → CaO
Bạn có muốn mình vẽ sơ đồ Lewis đầy đủ bằng hình minh họa (vòng tròn electron) cho dễ nhìn không? (mình có thể tạo ảnh mô phỏng).
Quảng cáo
Bạn cần hỏi gì?
Câu hỏi hot cùng chủ đề
-
Hỏi từ APP VIETJACK
 Đã trả lời bởi chuyên gia
76562
Đã trả lời bởi chuyên gia
76562 -
 Đã trả lời bởi chuyên gia
64725
Đã trả lời bởi chuyên gia
64725 -
Hỏi từ APP VIETJACK
 Đã trả lời bởi chuyên gia
57963
Đã trả lời bởi chuyên gia
57963 -
56146
-
Hỏi từ APP VIETJACK
 Đã trả lời bởi chuyên gia
42939
Đã trả lời bởi chuyên gia
42939 -
42407
-
 Đã trả lời bởi chuyên gia
41893
Đã trả lời bởi chuyên gia
41893 -
 Đã trả lời bởi chuyên gia
35660
Đã trả lời bởi chuyên gia
35660


