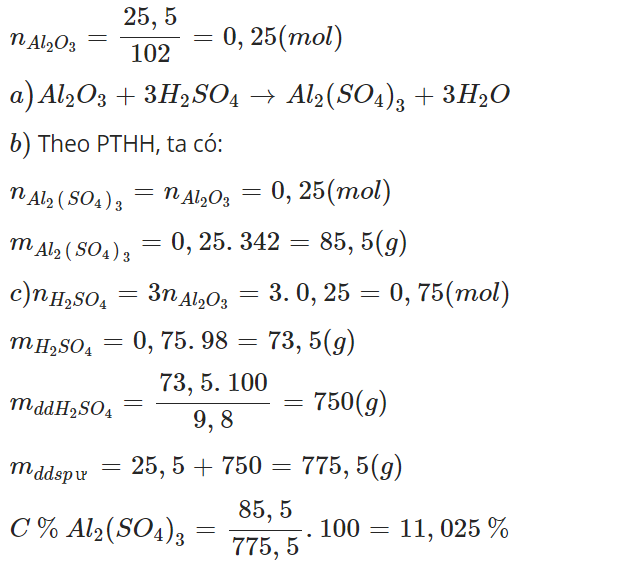hòa tan vừa đủ 25,5g Al2O3 bằng một lượng acid sulfuric 9,8%
c) tính nồng đọ phần trăm của chát trong dung dịch sau phản ứng ( Al2(SO4)3 )
Quảng cáo
2 câu trả lời 240
Để giải bài toán này, ta cần xác định lượng chất Al2(SO4)3 tạo thành sau phản ứng và sau đó tính nồng độ phần trăm của chất này trong dung dịch.
Bước 1: Xác định số mol Al2O3:
- Khối lượng mol của Al2O3 = 27*2 + 16*3 = 102g/mol
- Số mol Al2O3 = 25,5g / 102g/mol = 0,25 mol
Bước 2: Xác định số mol H2SO4:
- Khối lượng mol của H2SO4 = 1*2 + 32 + 16*4 = 98g/mol
- Số mol H2SO4 = 9,8% * 0,25 mol = 0,0245 mol
Bước 3: Xác định số mol Al2(SO4)3 tạo thành:
- Theo phản ứng: Al2O3 + 3H2SO4 -> Al2(SO4)3 + 3H2O
- Số mol Al2(SO4)3 = 0,25 mol (do 1 mol Al2O3 tạo ra 1 mol Al2(SO4)3)
Bước 4: Tính khối lượng mol của Al2(SO4)3:
- Khối lượng mol của Al2(SO4)3 = 27*2 + 32*3 + 16*12 = 342g/mol
- Khối lượng Al2(SO4)3 = 0,25 mol * 342g/mol = 85,5g
Bước 5: Tính nồng độ phần trăm của Al2(SO4)3 trong dung dịch:
- Nồng độ phần trăm = (khối lượng Al2(SO4)3 / tổng khối lượng dung dịch) * 100%
- Nồng độ phần trăm = (85,5g / (25,5g + 98g)) * 100% = (85,5g / 123,5g) * 100% ≈ 69,2%
==> Vậy nồng độ phần trăm của chất Al2(SO4)3 trong dung dịch sau phản ứng là khoảng 69,2%.
Quảng cáo
Bạn cần hỏi gì?
Câu hỏi hot cùng chủ đề
-
 Đã trả lời bởi chuyên gia
13734
Đã trả lời bởi chuyên gia
13734 -
 Đã trả lời bởi chuyên gia
8223
Đã trả lời bởi chuyên gia
8223 -
 Đã trả lời bởi chuyên gia
5591
Đã trả lời bởi chuyên gia
5591 -
 Đã trả lời bởi chuyên gia
5267
Đã trả lời bởi chuyên gia
5267 -
 Đã trả lời bởi chuyên gia
4929
Đã trả lời bởi chuyên gia
4929 -
 Đã trả lời bởi chuyên gia
4407
Đã trả lời bởi chuyên gia
4407
Gửi báo cáo thành công!