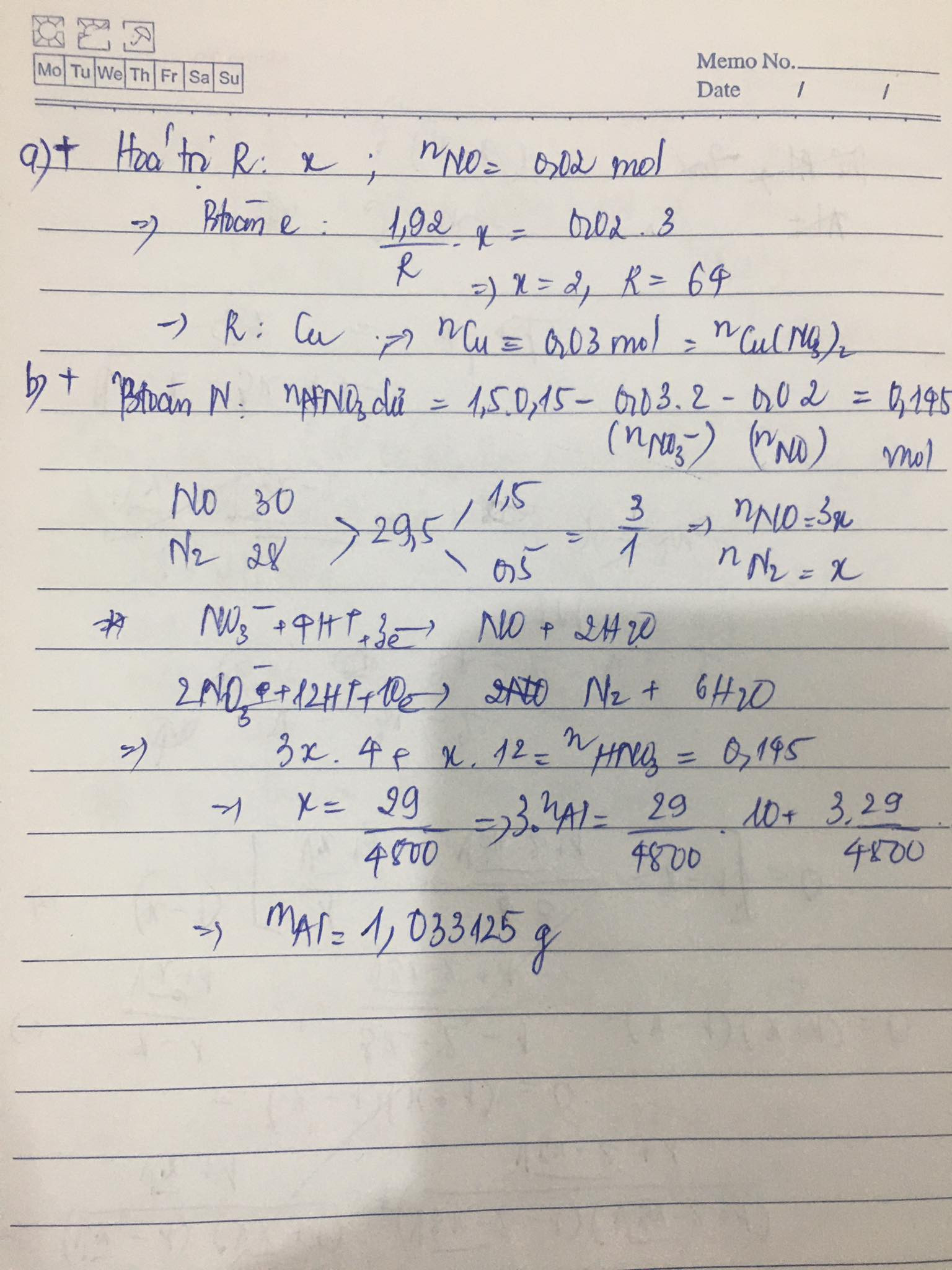Hòa tan 1,92g kim loại R trong 1,5 lít dd HNO 3 0,15M thu được 0,448 lít khí NO(đktc) và ddA.
a) Tìm kim loại R?
b) Thêm ag Al vào dd A để phản ứng hết lượng axit dư (bỏ qua phản ứng của Al với ion kim loại R(+)) thấy thoát
ra hh khí NO và N 2 có tỉ khối so với H 2 bằng 14,75. Tính khối lượng Al đã dùng?
Quảng cáo
2 câu trả lời 2882
a) n HNO3=0,225 (mol) ; n NO= 0,02 (mol)
BTe:
+3e->
0,06 0,02
e nhận = e nhường= 0,06 mol
0,06
Ta có: =>
| n | 1 | 2 |
| 32 (Loại | 64 (Nhận) |
Vậy R là Cu
b) Đặt n NO= x (mol), n N2=y (mol)
=> 0,5x-1,5y=0 (1)
3Cu+ 8HNO3-> 3Cu(NO3)2+ 2NO+4H2O
Ban đầu: 0,03 0,225
Phản ứng: 0,03 0,08
Sau phản ứng: 0,145
BTe:
0
1
Ta có: x+2y=n HNO3 dư= 0,145 mol (2)
Từ (1) và (2) =>2
∑e nhận = ∑e nhường= 0,551 mol
3
m Al= 4,959 (g)
Quảng cáo
Bạn muốn hỏi bài tập?
Câu hỏi hot cùng chủ đề
-
Hỏi từ APP VIETJACK64705
-
Hỏi từ APP VIETJACK44807