Đặt cốc A đựng dung dịch HCl và cốc B đựng dung dịch H2SO4 loãng vào 2 đĩa cân sao cho cân ở vị trí cân bằng. Sau đó làm thí nghiệm như sau:
- Cho 11,2g Fe vào cốc đựng dung dịch HCl.
- Cho m gam Al vào cốc đựng dung dịch H2SO4.
Khi cả Fe và Al đều tan hoàn toàn thấy cân ở vị trí thăng bằng. Tính m?
Quảng cáo
4 câu trả lời 14917
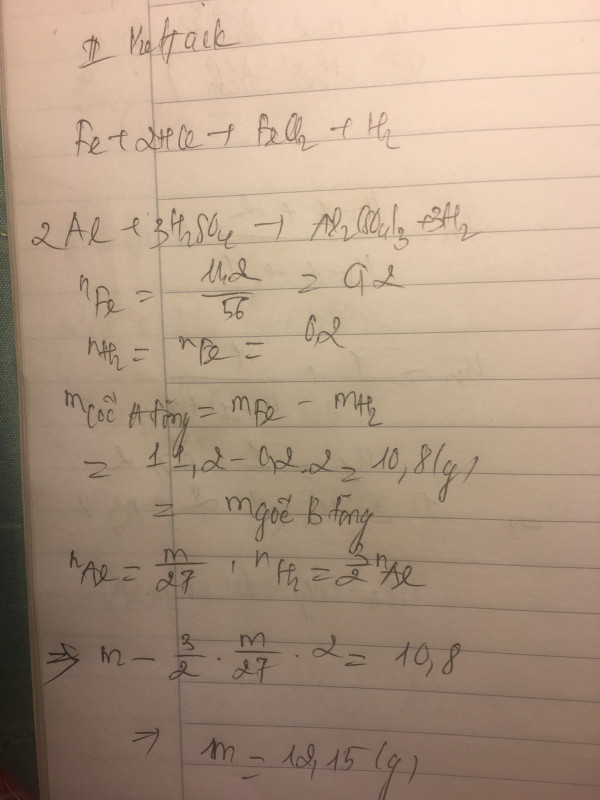
nFe= 11,2 : 56 = 0,2 mol
nAl = m/27 mol
- Khi thêm Fe vào cốc đựng dd HCl (cốc A) có phản ứng:
Fe + 2HCl → FeCl2 +H2
0,2 0,2
Theo định luật bảo toàn khối lượng, khối lượng cốc đựng HCl tăng thêm:
11,2 - (0,2.2) = 10,8g
- Khi thêm Al vào cốc đựng dd H2SO4 có phản ứng:
2Al + 3 H2SO4 → Al2 (SO4)3 + 3H2
m/27 3m/54
- Khi cho m gam Al vào cốc B, cốc B tăng thêm m - 3.m27.2.2
- Để cân thăng bằng, khối lượng ở cốc đựng H2SO4 cũng phải tăng thêm 10,8g. Có: m - 3.m27.2.2 = 10,8
- Giải được m = 12,15 (g)
PTHH Fe+ 2HCl--->FeCl2+H2 (1)
2Al +H2SO4---> Al2(SO4)3 +H2 (2)
Cốc A nH2=nFe=11,2/56=0,2 (mol)
mH2= 0,2.2=0,4 (g)
sau khi pứ kết thúc khối lượng cốc A tăng 11,2-0,4=10,8 (g)
cốc B nH2=1,5 . nAl= 1,5 . m/27 =m/18 (mol)
mH2= 2m/1-m/9 (g)
Sau pứ kết thúc khối lượng cốc B tăng
m-m/9=8m/9 (g)
để kim chỉ vị trí cân bằng thì mA=mB
8m/9=10,8 <=> m=(10,8 .9 )/8=12,15 (g)
Chúc bạn học tốt
PTHH Fe+ 2HCl--->FeCl2+H2 (1)
2Al +H2SO4---> Al2(SO4)3 +H2 (2)
Cốc A nH2=nFe=11,2/56=0,2 (mol)
mH2= 0,2.2=0,4 (g)
sau khi pứ kết thúc khối lượng cốc A tăng 11,2-0,4=10,8 (g)
cốc B nH2=1,5 . nAl= 1,5 . m/27 =m/18 (mol)
mH2= 2m/1-m/9 (g)
Sau pứ kết thúc khối lượng cốc B tăng
m-m/9=8m/9 (g)
để kim chỉ vị trí cân bằng thì mA=mB
8m/9=10,8 <=> m=(10,8 .9 )/8=12,15 (g)
Quảng cáo
Bạn cần hỏi gì?
Câu hỏi hot cùng chủ đề
-
Hỏi từ APP VIETJACK
 Đã trả lời bởi chuyên gia
46597
Đã trả lời bởi chuyên gia
46597 -
Hỏi từ APP VIETJACK
 Đã trả lời bởi chuyên gia
34479
Đã trả lời bởi chuyên gia
34479 -
 Đã trả lời bởi chuyên gia
34235
Đã trả lời bởi chuyên gia
34235 -
 Đã trả lời bởi chuyên gia
29413
Đã trả lời bởi chuyên gia
29413 -
Hỏi từ APP VIETJACK
 Đã trả lời bởi chuyên gia
26539
Đã trả lời bởi chuyên gia
26539 -
 Đã trả lời bởi chuyên gia
26190
Đã trả lời bởi chuyên gia
26190 -
 Đã trả lời bởi chuyên gia
23267
Đã trả lời bởi chuyên gia
23267 -
 Đã trả lời bởi chuyên gia
23214
Đã trả lời bởi chuyên gia
23214


