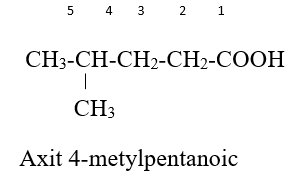Quảng cáo
6 câu trả lời 133
- Axit cacboxylic no, đơn chức, mạch hở (công thức chung: R−COOH) có các tính chất hoá học đặc trưng sau:
1. Tính axit (yếu)
- Do nhóm −COOH phân li ra H+: R − COOH ⇌ R − COO− + H+
=> Làm quỳ tím hóa đỏ.
2. Tác dụng với kim loại đứng trước H
- Tạo muối và giải phóng khí H2: 2R − COOH + 2Na → 2R − COONa + H2↑
3. Tác dụng với bazơ (phản ứng trung hòa)
R − COOH + NaOH → R − COONa + H2O
4. Tác dụng với oxit bazơ
2R − COOH + CuO → (R − COO)2Cu + H2O
5. Tác dụng với muối (giải phóng khí CO₂)
2R − COOH + Na2CO3 → 2R − COONa + CO2↑ + H2O
R − COOH + NaHCO3 → R − COONa + CO2↑ + H2O
6. Phản ứng este hóa (với ancol)
- Khi có H2SO4 đặc, đun nóng:
R − COOH + R′ − OH ⇌ R − COOR′ + H2O
1. Tính axit (quan trọng nhất)
Do có nhóm –COOH nên có tính axit yếu:
Làm quỳ tím → đỏ
Tác dụng với kim loại (trước H):
→ tạo muối + H₂
Ví dụ:
2RCOOH+Zn→(RCOO)2Zn+H2↑2RCOOH + Zn \rightarrow (RCOO)_2Zn + H_2↑2RCOOH+Zn→(RCOO)2Zn+H2↑
Tác dụng với bazơ:
→ muối + nước
RCOOH+NaOH→RCOONa+H2ORCOOH + NaOH \rightarrow RCOONa + H_2ORCOOH+NaOH→RCOONa+H2O
Tác dụng với oxit bazơ:
2RCOOH+CaO→(RCOO)2Ca+H2O2RCOOH + CaO \rightarrow (RCOO)_2Ca + H_2O2RCOOH+CaO→(RCOO)2Ca+H2O
Tác dụng với muối cacbonat:
→ muối + CO₂ + H₂O
2RCOOH+Na2CO3→2RCOONa+CO2↑+H2O2RCOOH + Na_2CO_3 \rightarrow 2RCOONa + CO_2↑ + H_2O2RCOOH+Na2CO3→2RCOONa+CO2↑+H2O
🔥 2. Phản ứng este hoá
Tác dụng với ancol tạo este + nước (có H₂SO₄ đặc, đun nóng):
RCOOH+R′OH⇌RCOOR′+H2ORCOOH + R'OH \rightleftharpoons RCOOR' + H_2ORCOOH+R′OH⇌RCOOR′+H2O👉 Đây là phản ứng rất quan trọng!
🔁 3. Phản ứng tách nước (tạo anhiđrit)
Khi đun nóng mạnh:
2RCOOH→(RCO)2O+H2O2RCOOH \rightarrow (RCO)_2O + H_2O2RCOOH→(RCO)2O+H2O
🔥 4. Phản ứng cháy
RCOOH+O2→CO2+H2ORCOOH + O_2 \rightarrow CO_2 + H_2ORCOOH+O2→CO2+H2O
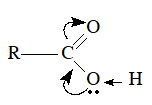
- carboxylic acid là hợp chất hữu cơ mà phân tử có nhóm cacboxyl (-COOH) liên kết trực tiếp với nguyên tử cacbon hoặc nguyên tử hiđro.
- Nhóm 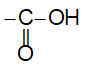
- Nhóm –OH và nhóm >C=O lại có ảnh hưởng qua lại lẫn nhau:
- Liên kết giữa H và O trong nhóm –OH phân cực mạnh, nguyên tử H linh động hơn trong ancol, anđehit và ketone có cùng số nguyên tử C.
2. Phân loại
- Nếu nhóm cacboxyl liên kết trực tiếp với nguyên tử hiđro hoặc gốc ankyl thì tạo thành dãy axit no, mạch hở, đơn chức, công thức chung là CnH2n+1COO, gọi là dãy đồng đẳng của formic acid (HCOOH). Ví dụ: CH3COOH (acetic acid), CH3CH2COOH (axit propionic), ...
- Nếu gốc hydrocarbon trong phân tử axit có chứa liên kết đôi, liên kết ba thì gọi là axit không no. Ví dụ CH2=CH-COOH.
- Nếu gốc hydrocarbon là vòng thơm thì gọi là axit thơm, ví dụ C6H5-COOH (benzoic acid), ...
- Nếu trong phân tử có nhiều nhóm cacboxyl (-COOH) thì gọi là axit đa chức. Ví dụ: HOOC-COOH (oxalic acid), HOOCCH2COOH (axit malonic), ...
3. Danh pháp
- Tên thay thế:
Tên gọi = axit + tên hydrocarbon no tương ứng với mạch chính + “oic”.
VD:
- Tên thông thường: Xuất phát từ nguồn gốc tìm ra chúng.
VD: HOOC-COOH: oxalic acid
HOOC-CH2-COOH: axit malonic.
HOOC-[CH2]4-COOH: axit ađipic.
Quảng cáo
Bạn cần hỏi gì?
Câu hỏi hot cùng chủ đề
-
 Đã trả lời bởi chuyên gia
103747
Đã trả lời bởi chuyên gia
103747 -
 Đã trả lời bởi chuyên gia
89852
Đã trả lời bởi chuyên gia
89852 -
 Đã trả lời bởi chuyên gia
68845
Đã trả lời bởi chuyên gia
68845 -
Hỏi từ APP VIETJACK64916
-
 Đã trả lời bởi chuyên gia
64017
Đã trả lời bởi chuyên gia
64017 -
 Đã trả lời bởi chuyên gia
55537
Đã trả lời bởi chuyên gia
55537 -
Hỏi từ APP VIETJACK45016
-
Hỏi từ APP VIETJACK
 Đã trả lời bởi chuyên gia
43421
Đã trả lời bởi chuyên gia
43421