hãy vẽ sơ đồ liên kết hóa học của các chất sau : CO2 , NH3, CH4, H2F
Quảng cáo
4 câu trả lời 776
Dưới đây là sơ đồ liên kết hóa học của các chất CO2, NH3, CH4 và H2F:
1. CO2 (Carbon Dioxide)
Cấu trúc: Nguyên tử trung tâm là Carbon (C) liên kết với hai nguyên tử Oxy (O) bằng liên kết đôi.
Sơ đồ: O=C=O
2. NH3 (Amoniak)
Cấu trúc: Nguyên tử trung tâm là Nitơ (N) liên kết với ba nguyên tử Hidro (H) bằng ba liên kết đơn. Ngoài ra, Nitơ còn có một cặp electron chưa liên kết.
Sơ đồ:
Mã
H
|
H-N-H
|
H
3. CH4 (Mêtan)
Cấu trúc: Nguyên tử trung tâm là Carbon (C) liên kết với bốn nguyên tử Hidro (H) bằng bốn liên kết đơn.
Sơ đồ:
Mã
H
|
H-C-H
|
H
4. H2F (Axit Hidroflooric)
Cấu trúc: Nguyên tử trung tâm là Flo (F) liên kết với một nguyên tử Hidro (H) bằng một liên kết đơn.
Sơ đồ: H-F
CO2 (Carbon Dioxide)
Cấu trúc: Nguyên tử Carbon (C) ở trung tâm, liên kết với hai nguyên tử Oxygen (O) bằng hai liên kết đôi.
Sơ đồ: O=C=O
NH3 (Amoniac)
Cấu trúc: Nguyên tử Nitrogen (N) ở trung tâm, liên kết với ba nguyên tử Hydrogen (H) bằng ba liên kết đơn. Nguyên tử N còn một cặp electron tự do.
Sơ đồ: H
|
H-N-H
CH4 (Methane)
Cấu trúc: Nguyên tử Carbon (C) ở trung tâm, liên kết với bốn nguyên tử Hydrogen (H) bằng bốn liên kết đơn.
Sơ đồ: H
|
H-C-H
|
H
H2F
Chất H2F không phải là một hợp chất hóa học phổ biến và ổn định. Thông thường, Fluorine (F) có hóa trị -1. Để tạo thành một hợp chất trung hòa về điện với Hydro, công thức phổ biến nhất là HF (Hydrofluoric acid), trong đó một nguyên tử Hydro liên kết với một nguyên tử Fluorine bằng một liên kết đơn.
Nếu bạn muốn biểu diễn một cấu trúc giả định với hai nguyên tử Hydro và một nguyên tử Fluorine, sẽ có những cách sắp xếp khác nhau tùy thuộc vào giả định về liên kết và điện tích. Tuy nhiên, trong H2F, nguyên tử F có độ âm điện rất lớn, nên việc nó liên kết với hai nguyên tử H theo cách thông thường là không điển hình.
Trong trường hợp phổ biến nhất là HF (Hydrofluoric acid):Cấu trúc: Nguyên tử Hydrogen (H) liên kết với nguyên tử Fluorine (F) bằng một liên kết đơn. Nguyên tử Fluorine có ba cặp electron tự do.
Sơ đồ: H-F
Hydro (H): Có 1 electron lớp ngoài cùng. Nó có xu hướng góp chung 1 electron để đạt 2 electron (giống Helium).
Biểu diễn: H•
Carbon (C): Có 4 electron lớp ngoài cùng. Nó có xu hướng góp chung 4 electron để đạt 8 electron.
Biểu diễn: •C• • •
Nitrogen (N): Có 5 electron lớp ngoài cùng. Nó có xu hướng nhận thêm 3 electron hoặc góp chung để đạt 8 electron.
Biểu diễn: •N•• • •
Oxygen (O): Có 6 electron lớp ngoài cùng. Nó có xu hướng nhận thêm 2 electron hoặc góp chung để đạt 8 electron.
Biểu diễn: •O•• • •
Fluorine (F): Có 7 electron lớp ngoài cùng. Nó có xu hướng nhận thêm 1 electron để đạt 8 electron.
Biểu diễn: •F•• • ••
Natri (Na): Có 1 electron lớp ngoài cùng. Nó có xu hướng nhường 1 electron để đạt cấu hình bền của khí hiếm đứng trước nó.
Biểu diễn: Na•
Magie (Mg): Có 2 electron lớp ngoài cùng. Nó có xu hướng nhường 2 electron.
Biểu diễn: Mg••
Trong Hóa học, sơ đồ liên kết hóa học biểu diễn cách các nguyên tử liên kết với nhau để tạo thành phân tử. Dưới đây là sơ đồ liên kết hóa học của các phân tử CO₂, NH₃, CH₄ và HF (sử dụng thay thế cho H₂F vì H₂F là một chất không bền).
Sơ đồ liên kết hóa học
Dưới đây là hình ảnh minh họa về sơ đồ liên kết hóa học của các chất CO₂, NH₃, CH₄ và HF, thể hiện các electron hóa trị và liên kết cộng hóa trị.
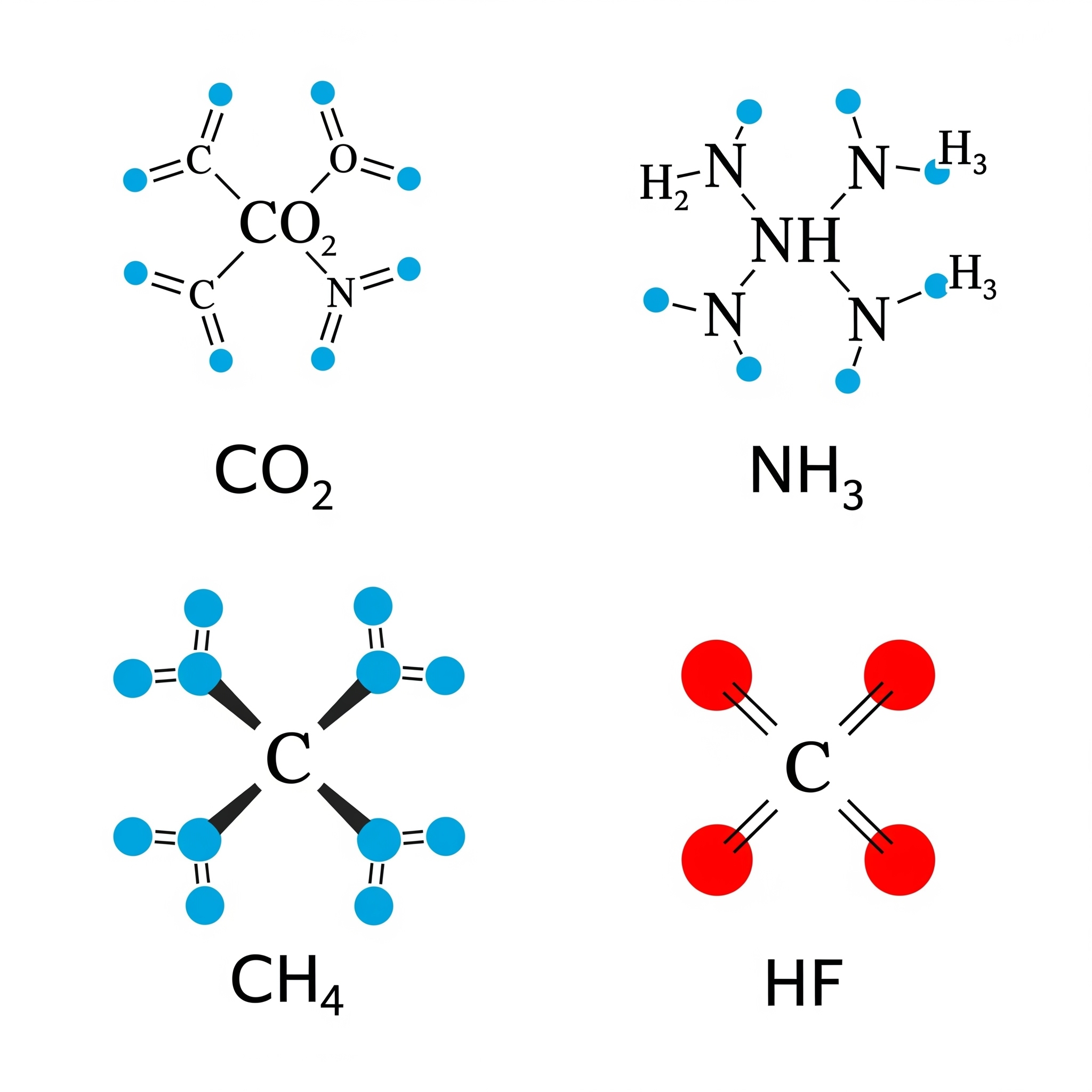
Giải thích các sơ đồ
CO₂ (Carbon dioxide): Nguyên tử carbon ở trung tâm tạo hai liên kết đôi với hai nguyên tử oxy. Mỗi liên kết đôi bao gồm hai cặp electron dùng chung.
NH₃ (Ammonia): Nguyên tử nitơ ở trung tâm tạo ba liên kết đơn với ba nguyên tử hydro. Nguyên tử nitơ còn lại một cặp electron không liên kết (cặp electron tự do).
CH₄ (Methane): Nguyên tử carbon ở trung tâm tạo bốn liên kết đơn với bốn nguyên tử hydro. Tất cả các electron hóa trị của carbon đều tham gia vào liên kết.
HF (Hydrogen fluoride): Nguyên tử hydro tạo một liên kết đơn với nguyên tử flo. Nguyên tử flo còn lại ba cặp electron không liên kết.
Quảng cáo
Bạn cần hỏi gì?
Câu hỏi hot cùng chủ đề
-
 Đã trả lời bởi chuyên gia
9909
Đã trả lời bởi chuyên gia
9909 -
 Đã trả lời bởi chuyên gia
6088
Đã trả lời bởi chuyên gia
6088 -
3971


