Giải Khoa học tự nhiên 7 (Chân trời sáng tạo) Bài 2: Nguyên tử
Hoidapvietjack.com trân trọng giới thiệu: lời giải bài tập Khoa học tự nhiên lớp 7 Bài 2: Nguyên tử sách Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng trả lời câu hỏi và làm bài tập KHTN 7 Bài 2.
Giải bài tập Khoa học tự nhiên 7 Bài 2: Nguyên tử
Video giải bài tập Khoa học tự nhiên 7 Bài 2: Nguyên tử
Mở đầu trang 14 Bài 2 KHTN lớp 7: Từ những vật thể đơn giản như cây bút, quyển vở, chai nước cho đến những công trình nổi tiếng như tháp Eiffel,… đều được tạo nên từ chất. Mỗi chất lại được tạo nên từ những hạt vô cùng nhỏ. Những hạt đó là gì?

Trả lời:
Mỗi chất lại được tạo nên từ những hạt vô cùng nhỏ. Những hạt đó gọi là nguyên tử.
1. Mô hình nguyên tử Rutherford – Bohr
Câu hỏi thảo luận 1 trang 14 KHTN lớp 7: Những đối tượng nào trong Hình 2.1 ta có thể quan sát bằng mắt thường? Bằng kính lúp? Bằng kính hiển vi?
Trả lời:
Quan sát bằng mắt thường: Ruột bút chì
Quan sát bằng kính lúp: Hạt bụi trong không khí
Quan sát bằng kính hiển vi: Tế bào máu, vi khuẩn.
Câu hỏi thảo luận 2 trang 14 KHTN lớp 7: Quan sát Hình 2.2, em hãy cho biết khí oxygen, sắt, than chì có đặc điểm chung gì về cấu tạo?
Trả lời:
Khí oxygen, sắt, than chì đều được tạo nên từ những hạt vô cùng nhỏ, gọi là nguyên tử.
Câu hỏi thảo luận 3 trang 15 KHTN lớp 7: Theo Rutherford – Bohr, nguyên tử có cấu tạo như thế nào?
Trả lời:
Theo Rutherford – Bohr, nguyên tử có cấu tạo gồm hạt nhân ở bên trong và lớp vỏ tạo bởi một hay nhiều electron (kí hiệu là e) mang điện tích âm. Bên trong hạt nhân chứa các hạt proton (kí hiệu là p) mang điện tích dương.
Các electron được sắp xếp thành từng lớp và chuyển động xung quanh hạt nhân theo quỹ đạo tương tự như hành tinh trong hệ Mặt Trời.
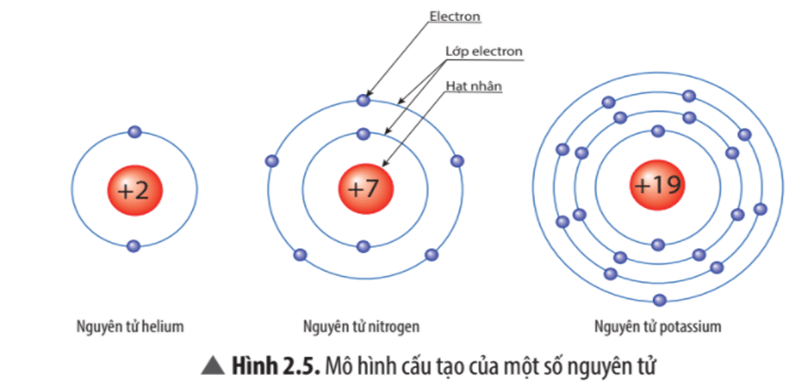
Câu hỏi thảo luận 4 trang 15 KHTN lớp 7: Quan sát Hình 2.5, hãy cho biết nguyên tử nitrogen và potassium có bao nhiêu
a) điện tích hạt nhân nguyên tử?
b) lớp electron?
c) electron trên mỗi lớp?
Trả lời:
|
|
Nguyên tử nitrogen |
Nguyên tử potassium |
|
Điện tích hạt nhân nguyên tử |
+7 |
+19 |
|
Lớp electron |
2 |
4 |
|
Electron trên mỗi lớp |
2/5 |
2/8/8/1 |
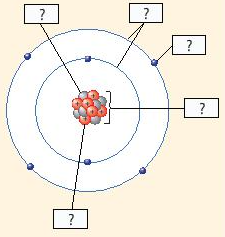 Trả lời:
Trả lời:
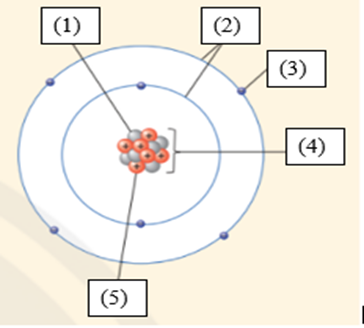
(1) Neutron
(2) Vỏ nguyên tử
(3) Electron
(4) Hạt nhân nguyên tử
(5) Proton
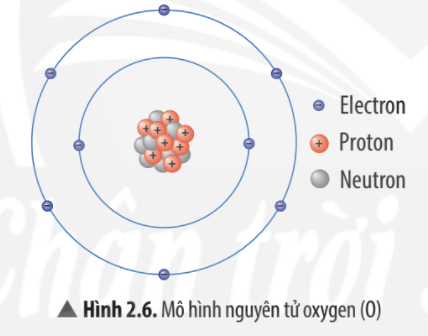
Luyện tập 2 trang 16 KHTN lớp 7: Quan sát Hình 2.6, hãy hoàn thành bảng sau:
|
Số đơn vị điện tích hạt nhân |
Số proton |
Số electron trong nguyên tử |
Số electron ở lớp ngoài cùng |
|
? |
? |
? |
? |
Để lớp electron ngoài cùng của nguyên tử oxygen có đủ số electron tối đa thì cần thêm bao nhiêu electron nữa?
Trả lời:
|
Số đơn vị điện tích hạt nhân |
Số proton |
Số electron trong nguyên tử |
Số electron ở lớp ngoài cùng |
|
8 |
8 |
8 |
6 |
Để lớp electron ngoài cùng của nguyên tử oxygen có đủ số electron tối đa là 8 thì cần thêm 2 electron nữa.
2. Khối lượng nguyên tử
Câu hỏi thảo luận 6 trang 17 KHTN lớp 7: Vì sao người ta thường sử dụng amu làm đơn vị khối lượng nguyên tử?
Trả lời:
Vì khối lượng của nguyên tử rất nhỏ nên để biểu thị khối lượng nguyên tử người ta sử dụng đơn vị khối lượng nguyên tử, viết tắt là amu (atomic mass unit).
1 amu = 1,6605 × 10-24 gam
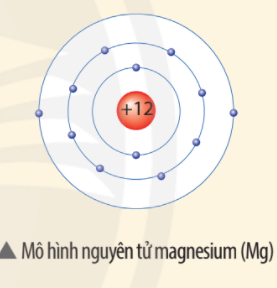
Luyện tập trang 17 KHTN lớp 7: Quan sát mô hình dưới đây, cho biết số proton, số electron và xác định khối lượng nguyên tử magnesium (biết số neutron bằng 12)
Trả lời:
Điện tích hạt nhân nguyên tử Mg là +12.
⇒ Một nguyên tử magnesium (Mg) gồm: 12 proton, 12 electron.
Khối lượng nguyên tử Mg bằng 12 + 12 = 24 amu.
(do khối lượng 1p = 1n = 1 amu).
Bài tập (trang 17)
Bài 1 trang 17 KHTN lớp 7: Em hãy điền vào chỗ trống các từ, cụm từ thích hợp sau để được câu hoàn chỉnh:
|
chuyển động |
các electron |
hạt nhân |
điện tích dương |
trung hòa về điện |
|
vỏ nguyên tử |
điện tích âm |
vô cùng nhỏ |
sắp xếp |
|
Nguyên tử là hạt (1) … và (2) … Theo Rutherford – Bohr, nguyên tử có cấu tạo gồm 2 phần là (3) … (mang (4) …) và (5) … tạo bởi (6) … (mang (7) …).
Trong nguyên tử, các electron (8) … xung quanh hạt nhân và (9) … thành từng lớp.
Trả lời:
(1) vô cùng nhỏ
(2) trung hòa về điện
(3) hạt nhân
(4) điện tích dương
(5) vỏ nguyên tử
(6) các electron
(7) điện tích âm
(8) chuyển động
(9) sắp xếp
Bài 2 trang 17 KHTN lớp 7: Vì sao nói khối lượng hạt nhân được coi là khối lượng nguyên tử?
Trả lời:
Proton và neutron có khối lượng xấp xỉ bằng nhau (gần bằng 1 amu). Electron có khối lượng rất bé (chỉ khoảng bằng 0,00055 amu), nhỏ hơn rất nhiều lần so với khối lượng của proton và neutron. Do đó khối lượng hạt nhân được coi là khối lượng nguyên tử.
Xem thêm lời giải bài tập Khoa học tự nhiên lớp 7 Chân trời sáng tạo hay, chi tiết khác:
Giải Khoa học tự nhiên 7 Bài 3: Nguyên tố hóa học - Kết nối tri thức
Giải Khoa học tự nhiên 7 Bài 4: Sơ lược bảng tuần hoàn các nguyên tố hóa học - Kết nối tri thức
Giải Khoa học tự nhiên 7 Bài 5: Phân tử - Đơn chất – Hợp chất - Kết nối tri thức
Giải Khoa học tự nhiên 7 Bài 6: Giới thiệu về liên kết hóa học