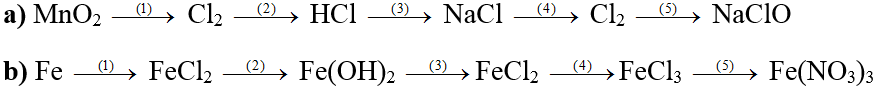Cách hoàn thành phương trình hóa học về Halogen hay, chi tiết
Cách hoàn thành phương trình hóa học về Halogen hay, chi tiết Hóa học lớp 10 với đầy đủ lý thuyết, phương pháp giải và bài tập có lời giải cho tiết sẽ giúp học sinh nắm được Cách hoàn thành phương trình hóa học về Halogen hay, chi tiết
Cách hoàn thành phương trình hóa học về Halogen hay, chi tiết
-
A. Phương pháp & Ví dụ
Lý thuyết và Phương pháp giải
- Nắm vững các tính chất hóa học của các halogen và hợp chất của chúng
- Một số tính chất đặc trưng cần lưu ý:
+ Halogen là những phi kim điển hình. Đi từ flo đến iot, tính oxi hoá giảm dần. Các halogen đứng trước đẩy halogen đứng sau nó ra khỏi dung dịch muối halogen.
+ Flo có độ âm điện lớn nhất nên trong tất cả các hợp chất chỉ có số oxi hoá 1. Các nguyên tố halogen khác, ngoài số oxi hoá –1 còn có các số oxi hoá +1, +3, +5, +7.
+ Tính khử của HX: Tăng dần từ HF < HCl < HBr < HI.
+ Tính axit của dung dịch HX: Tính axit tăng dần từ HF < HCl < HBr < HI.
+ Tính axit của HXO4 : Giảm dần từ HClO4 > HBrO4 > HIO4.

-
Ví dụ minh họa
Ví dụ 1. Cân bằng các phản ứng oxi hóa – khử sau:
a) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
b) KClO3 + HCl → KCl + Cl2 + H2O
c) KOH + Cl2 → KCl + KClO3 + H2O
d) Cl2 + SO2 + H2O → HCl + H2SO4
e) Fe3O4 + HCl → FeCl2 + FeCl3 + H2O
f) CrO3 + HCl → CrCl3 + Cl2 + H2O
g) Cl2 + Ca(OH) 2 → CaCl2 + Ca(OCl)2 + H2O
Hướng dẫn:
a, 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2 O
b, KClO3 + 6HCl → KCl + 3Cl2 + 3H2 O
c, 6KOH + 3Cl2 → 5KCl + KClO3 + 3H2 O
d, Cl2 + SO2 + 2H2O → 2HCl + H2 SO4
e, Fe3 O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O
f, 2CrO3 + 12HCl → 2CrCl3 + 3Cl2 + 6H2 O
g, 2Cl2 + 2Ca(OH) 2 → CaCl2 + Ca(OCl)2 + 2H2O
-
Ví dụ 2. Hoàn thành chuỗi phản ứng sau:
a) MnO2 → Cl2 → HCl → Cl2 → CaCl2 → Ca(OH) 2 → Clorua vôi
b, KMnO4 → Cl2 → KCl → Cl2 → axit hipoclorơ
→ NaClO → NaCl → Cl2 → FeCl3
Hướng dẫn:
a, MnO2 + 4HCl → MnCl2 + Cl2 + 2H2 O
H2 + Cl2 → 2HCl
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2 O
Ca + Cl2 → CaCl2
CaCl2 + NaOH → Ca(OH)2 + NaCl
Cl2 + Ca(OH) 2 → CaOCl2 + H2O
b, 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2 O
Cl2 + 2K → 2 KCl
2KCl → 2K + Cl2
Cl + H2 O → HCl+ HClO
Cl2 + 2NaOH → NaCl + NaClO + H2 O
NaClO + 2HCl → Cl2 + NaCl + H2 O
2NaCl + 2H2 O → H2 + 2NaOH + Cl2
2Fe + 3Cl2 → 2FeCl3
Ví dụ 3: Hoàn thành các phương trình hóa học theo sơ đồ sau, ghi rõ điều kiện phản ứng(nếu có):
Hướng dẫn:
a, 1. MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
2. Cl2 + SO2 + 2H2 O → 2HCl + H2SO4
3. 2Na + 2HCl → 2NaCl + H2
4. 2NaCl + 2H2 O
H2 ↑ + 2NaOH + Cl2
5. Cl2 + 2NaOH → NaCl + NaClO + H2 O
b, 1. Fe + HCl → FeCl2 + H2
2. FeCl2 + NaOH → Fe(OH) 2 + NaCl
3. Fe(OH) 2 + 2HCl → FeCl2 + 2H2O
4. 2FeCl2 + Cl2 → 2FeCl3
5. FeCl3 + 3AgNO3 → Fe(NO3)3 + 3AgCl
B. Bài tập trắc nghiệm
-
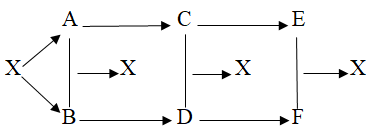
Câu 1. Cho sơ đồ:
Viết các phản ứng xảy ra theo sơ đồ trên với X là NaCl.
Câu 2. Hoà tan khí Cl2 vào dung dịch KOH đặc, nóng, dư. Dung dịch thu được có các chất thuộc dãy nào dưới đây ?
A. KCl, KClO3, Cl2. B. KCl, KClO3, KOH, H2O.
C. KCl, KClO, KOH, H2O. D. KCl, KClO3.
Câu 3. Hoà tan khí Cl2 vào dung dịch KOH loãng, nguội, dư. Dung dịch thu được có các chất thuộc dãy nào dưới đây ?
A. KCl, KClO3, Cl2. B. KCl, KClO3, KOH, H2O.
C. KCl, KClO, KOH, H2O. D. KCl, KClO3.
Câu 4. Cho các chất sau : KOH (1), Zn (2), Ag (3), Al(OH)3 (4), KMnO4 (5), K2SO4 (6). Axit HCl tác dụng được với các chất :
A. (1), (2), (4), (5). B. (3), (4), (5), (6).
C. (1), (2), (3), (4). D. (1), (2), (3), (5).
Câu 5. Cho các chất sau : CuO (1), Zn (2), Ag (3), Al(OH)3 (4), KMnO4 (5), PbS (6), MgCO3 (7), AgNO3 (8), MnO2 (9), FeS (10). Axit HCl không tác dụng được với các chất :
A. (1), (2). B. (3), (4). C. (5), (6). D. (3), (6).
Câu 6. Cho các phản ứng :
(1) O3 + dung dịch KI →
(2) F2 + H2O -to→
(3) MnO2 + HCl đặc -to→
(4) Cl2 + dung dịch H2S →
Các phản ứng tạo ra đơn chất là :
A. (1), (2), (3). B. (1), (3), (4).
C. (2), (3), (4). D. (1), (2), (4).
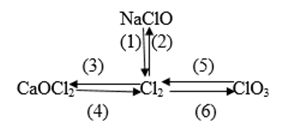
Câu 7. Cho sơ đồ chuyển hóa:
Fe3O4 + dung dịch HI (dư) X + Y + H2O
Biết X và Y là sản phẩm cuối cùng của quá trình chuyển hóa. Các chất X và Y là :
A. Fe và I2. B. FeI3 và FeI2.
C. FeI2 và I2. D. FeI3 và I2.
-
-
Câu 8. Viết phương trình hóa học của phản ứng thực hiện các biến hóa dưới đây, ghi tên các chất và điều kiện của phản ứng.