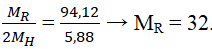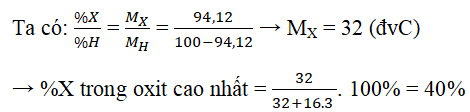Cách xác định nguyên tố thông qua nguyên tử khối hay, chi tiết
Cách xác định nguyên tố thông qua nguyên tử khối hay, chi tiết Hóa học lớp 10 với đầy đủ lý thuyết, phương pháp giải và bài tập có lời giải cho tiết sẽ giúp học sinh nắm được Cách xác định nguyên tố thông qua nguyên tử khối hay, chi tiết
Cách xác định nguyên tố thông qua nguyên tử khối hay, chi tiết
-
A. Phương pháp & Ví dụ
Lý thuyết và Phương pháp giải
Muốn xác định tên nguyên tố cần tìm được M dựa vào thành phần phần trăm nguyên tố M trong hỗn hợp; dựa vào các phản ứng hóa học, các tính chất của M.….
-
Ví dụ minh họa

Ví dụ 1. Oxit cao nhất của một nguyên tố ứng với công thức RO3. Hợp chất của nó với hidro có 5,88% H về khối lượng. Xác định R.
Hướng dẫn:
Oxit cao nhất là RO3 → R thuộc nhóm VIA.
Hợp chất với hidro có dạng RH2.
Đó là nguyên tố lưu huỳnh (S).
Ví dụ 2: Nguyên tử của nguyên tố C có cấu hình electron lớp ngoài cùng là ns2np4. Trong hợp chất khí của X với hidro, X chiếm 94,12% khối lượng. Phần trăm khối lượng của nguyên tố X trong oxit cao nhất là:
A.50,00% B.27,27% C.60,00% D.40,00%
Hướng dẫn:
X: ns2np4 → X thuộc nhóm IVA → hợp chất khí với H là XH2 → oxit cao nhất là XO3.
-
Ví dụ 3. Cho 10 gam kim loại A (thuộc nhóm IIA) tác dụng với nước, thu được 6,11 lit khí hiđro (đo ở 25oC và 1 atm).
a. Hãy xác định tên của kim loại M đã dùng.
b. Cho 4 gam kim loại A vào cốc đựng 2,5lit dung dịch HCl 0,06M thu được dung dịch B.
Hướng dẫn:
A + 2H2O → A(OH)2 + H2
a a
Số mol khí H2 = 0,25 (mol) ⇒ a = 0,25
Ta có: MA = 10/0,25 = 40 (Ca).
b. Số mol Ca = 4/40 = 0,1 mol. Các phương trình phản ứng:
Ca + 2HCl → CaCl2 + H2
(mol): 0,075 0,15 0,075
Ca + 2H2O → Ca(OH)2 + H2
(mol): 0,025 0,025
Dung dịch B gồm: CaCl2 = 0,075 mol và Ca(OH)2 = 0,025 mol.
-
B. Bài tập trắc nghiệm
Câu 1: Hòa tan hết a gam oxit kim loại M (thuộc nhóm IIA) bằng một lượng vừa đủ dung dịch H2SO4 17,5% thu được dung dịch muối có nồng độ 20%.Xác định công thức oxit kim loại M.
Câu 2: Oxit cao nhất của nguyên tố R có dạng R2O7. Sản phầm khí của R với hidro chứa 2,74% hidro về khối lượng. Xác định nguyên tử khối của R.
Câu 3: Cho 3 gam hỗn hợp gồm kim loại Na và một kim loại kiềm X tác dụng hết với nước thu được dung dịch A. Để trung hòa dung dịch A phải dùng dung dịch chưa 200ml dung dịch HCl 1M.
a. Xác định kim loại kiềm X.
b. Tính khối lượng mỗi kim loại trong hỗn hợp.
Câu 4: Nguyên tử Y có hóa trị cao nhất với oxi gấp 3 lần hóa trị trong hợp chất khí với hidro. Gọi X là công thức hợp chất oxit cao nhất, Z là công thức hợp chất khí với hidro của Y. Tỉ khối hơi của X đối với Z là 2,353. Xác định nguyên tố Y.
Câu 5: Muối X được tạo thành bởi một kim loại hóa trị 2 và phi kim hóa trị 1. Hòa tan 4,44 gam A vào H2O rồi chia làm hai phần bằng nhau:
- Cho phần 1 tác dụng với dung dịch AgNO3 dư thu được 5,74g kết tủa.
- Cho phần 2 tác dụng với dung dịch Na2CO3 dư thu được 2g kết tủa.
Tìm công thức muối X
Câu 6: M là kim loại thuộc nhóm IIA. Hòa tan hết 10,8 gam hỗn hợp kim loại muối cacbonat của nó trong dung dịch HCl, thu được 4,48 lít hỗn hợp khí A (đktc). Tỷ khối của A so với khí hidro là 11,5.
1. Tìm kim loại M
2. Tính % thể tích các khí trong A.
-
Câu 7: Có 5,56 gam hỗn hợp A gồm Fe và kim loại M (hóa trị n). Chia A làm hai phần bằng nhau:
Phần 1: Hòa tan hết trong dung dịch HCl được 1,568 lit khí H2.
Phần 2: Hòa tan hết trong dung dịch H2SO4 đặc nóng thu được 2,016 lit khí SO2.
Viết các phương trình phản ứng và xác định tên kim loại M. Các khí đo ở đktc.
- Câu 8: Oxit cao nhất của một nguyên tố ứng với công thức R2O5. Hợp chất của nó với hidro là một chất có thành phần không đổi với R chiếm 82,35% và H chiếm 17,65% về khối lượng. Tìm nguyên tố R.